名校
解题方法
1 . 请回答下列问题:
(1)基态Ni原子的价电子排布式为___________ ;MgCl2的电子式为___________ 。
(2) 常温下为无色液体,沸点为42.1℃,熔点为-19.3℃,难溶于水,易溶于有机溶剂。推测
常温下为无色液体,沸点为42.1℃,熔点为-19.3℃,难溶于水,易溶于有机溶剂。推测 是
是___________ 分子(填“极性”或“非极性”)。
(3)实验室常用 溶液或苯酚检验
溶液或苯酚检验 ,苯酚中碳原子杂化类型为
,苯酚中碳原子杂化类型为___________ 。
(4)配位化合物 中心原子Co的配位数为
中心原子Co的配位数为___________ ,配位原子为___________ 。
(5)第一电离能:N___________ O(填“>”、“=”或“<”,下同);电负性:Si___________ S;半径:
___________  ;还原性:
;还原性:
___________  。
。
(6)工业上用焦炭还原石英砂可以得到粗硅,其化学方程式为___________ ,将粗硅通过化学方法进一步提纯,可以得到高纯硅,高纯硅的晶体类型是___________ 晶体。
(7) 的空间结构为
的空间结构为___________ 。
(8)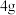 硫粉在
硫粉在 中完全燃烧生成
中完全燃烧生成 气体,放出
气体,放出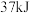 的热量,S燃烧的热化学方程式为
的热量,S燃烧的热化学方程式为___________ 。
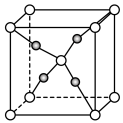
(9)一个Cu2O晶胞(如图)中,若该晶胞的棱长为a nm,阿伏加德罗常数的值为 ,则该晶体的密度为
,则该晶体的密度为___________  。(列出计算式即可)
。(列出计算式即可)
(1)基态Ni原子的价电子排布式为
(2)
 常温下为无色液体,沸点为42.1℃,熔点为-19.3℃,难溶于水,易溶于有机溶剂。推测
常温下为无色液体,沸点为42.1℃,熔点为-19.3℃,难溶于水,易溶于有机溶剂。推测 是
是(3)实验室常用
 溶液或苯酚检验
溶液或苯酚检验 ,苯酚中碳原子杂化类型为
,苯酚中碳原子杂化类型为(4)配位化合物
 中心原子Co的配位数为
中心原子Co的配位数为(5)第一电离能:N

 ;还原性:
;还原性:
 。
。(6)工业上用焦炭还原石英砂可以得到粗硅,其化学方程式为
(7)
 的空间结构为
的空间结构为(8)
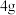 硫粉在
硫粉在 中完全燃烧生成
中完全燃烧生成 气体,放出
气体,放出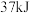 的热量,S燃烧的热化学方程式为
的热量,S燃烧的热化学方程式为(9)一个Cu2O晶胞(如图)中,若该晶胞的棱长为a nm,阿伏加德罗常数的值为
 ,则该晶体的密度为
,则该晶体的密度为 。(列出计算式即可)
。(列出计算式即可)
您最近一年使用:0次
名校
2 . 黄酮哌酯是一种解痉药,可通过如下路线合成:
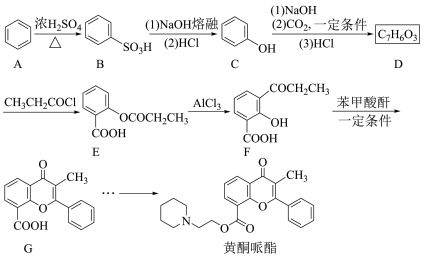
回答问题:
(1)A→B的反应类型为________ 。
(2)已知B为一元强酸,室温下B与 溶液反应的化学方程式为
溶液反应的化学方程式为________________ 。
(3)C的化学名称为________ ,D的结构简式为________ 。
(4)E和F可用________ (写出试剂)鉴别。
(5)X是F的同分异构体,符合下列条件,X可能的结构简式为________ (任写一种)。
①含有酯基 ②含有苯环 ③核磁共振氢谱有两组峰
(6)已知酸酐能与羟基化合物反应生成酯。写出下列F→G反应方程式中M和N的结构简式___________ 、____________ 。
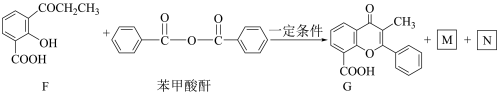
(7)参照题中信息补充完成设计路线:以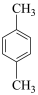 为原料合成
为原料合成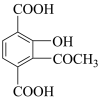 (其他试剂任选)。
(其他试剂任选)。
已知: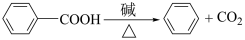

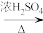
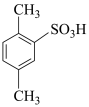

________________ 。

回答问题:
(1)A→B的反应类型为
(2)已知B为一元强酸,室温下B与
 溶液反应的化学方程式为
溶液反应的化学方程式为(3)C的化学名称为
(4)E和F可用
(5)X是F的同分异构体,符合下列条件,X可能的结构简式为
①含有酯基 ②含有苯环 ③核磁共振氢谱有两组峰
(6)已知酸酐能与羟基化合物反应生成酯。写出下列F→G反应方程式中M和N的结构简式

(7)参照题中信息补充完成设计路线:以
 为原料合成
为原料合成 (其他试剂任选)。
(其他试剂任选)。已知:
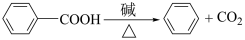

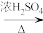


您最近一年使用:0次
名校
3 . 铁是人体必需的微量元素之一。黑木耳中的含铁量较高,为检验和测定干黑木耳样品中的铁元素,设计实验如下。回答下列问题:
Ⅰ.铁元素的检验

(1)“操作”是指________ ;上述流程中需要用到的仪器有托盘天平、烧杯、玻璃棒、酒精灯、漏斗,还有下图中的________ (填写仪器名称)。

(2)检验待测液中是否含有 、
、
Ⅱ.铁元素含量的测定
利用 标准溶液测定干黑木耳样品中铁元素的含量
标准溶液测定干黑木耳样品中铁元素的含量
步骤Ⅰ:取 待测液,加入过量铜粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。
待测液,加入过量铜粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。
步骤Ⅱ:向步骤Ⅰ所得的溶液中加入适量稀 溶液,用
溶液,用 的
的 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 溶液
溶液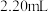 。
。
(3)步骤Ⅰ加入过量铜粉的目的是_________________________________ 。
(4)步骤Ⅱ滴加 溶液时发生反应的离子方程式为
溶液时发生反应的离子方程式为_____________________ 。
(5)用 标准溶液滴定至终点的标志是:
标准溶液滴定至终点的标志是:___________ 。
(6)黑木耳中铁的含量为________ mg/100g(即每100g黑木耳中含铁元素质量)。
(7)若步骤Ⅰ过滤后未洗涤将使测定结果________ (填“偏大”或“偏小”或“无影响”)。
Ⅰ.铁元素的检验

(1)“操作”是指

(2)检验待测液中是否含有
 、
、
| 检验试剂 | 现象 | 结论 |
| KSCN溶液 | 溶液变为红色 | 滤液中含有 |
| ① | ② | 滤液中含有 |
Ⅱ.铁元素含量的测定
利用
 标准溶液测定干黑木耳样品中铁元素的含量
标准溶液测定干黑木耳样品中铁元素的含量步骤Ⅰ:取
 待测液,加入过量铜粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。
待测液,加入过量铜粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。步骤Ⅱ:向步骤Ⅰ所得的溶液中加入适量稀
 溶液,用
溶液,用 的
的 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 溶液
溶液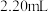 。
。(3)步骤Ⅰ加入过量铜粉的目的是
(4)步骤Ⅱ滴加
 溶液时发生反应的离子方程式为
溶液时发生反应的离子方程式为(5)用
 标准溶液滴定至终点的标志是:
标准溶液滴定至终点的标志是:(6)黑木耳中铁的含量为
(7)若步骤Ⅰ过滤后未洗涤将使测定结果
您最近一年使用:0次
2024-04-03更新
|
149次组卷
|
2卷引用:天津市宁河区芦台第一中学2024届高三下学期适应性模拟训练(3月)化学试题
名校
4 . 下列说法不正确 的是
| A.通过X射线衍射可测定青蒿素晶体的结构 |
| B.利用盐析的方法可将蛋白质从溶液中分离 |
| C.邻羟基苯甲醛在水中的溶解度高于对羟基苯甲醛在水中的溶解度 |
| D.可用新制氢氧化铜悬浊液鉴别苯、乙醇、乙醛、甲酸和醋酸溶液 |
您最近一年使用:0次
名校
解题方法
5 . TiO2和TiCl4均为重要的工业原料。已知:

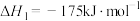 Ⅰ
Ⅰ
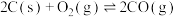
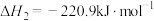 Ⅱ
Ⅱ
请回答下列问题:
(1)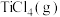 与
与 反应生成
反应生成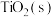 、
、 和氯气的热化学方程式为
和氯气的热化学方程式为___________ ;升高温度对该反应的影响为___________ 。
(2)若反应Ⅱ的逆反应的活化能为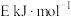 ,则E
,则E___________ (填“>”“<”或“=”)220.9。
(3)t℃时,向 恒容密闭容器中充入
恒容密闭容器中充入 和
和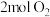 ,发生反应Ⅰ。
,发生反应Ⅰ。 时达到平衡,测得
时达到平衡,测得 的物质的量为
的物质的量为 。
。
① 内,用
内,用 表示的反应速率
表示的反应速率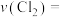
___________ 。
② 的平衡转化率为
的平衡转化率为___________ 。
③该反应的平衡常数为___________ (用分数表示)。
④下列措施,既能加快逆反应速率又能增大 平衡转化率的是
平衡转化率的是___________ (填字母)。
A.缩小容器容积 B.加入催化剂 C.分离出部分 D.增大
D.增大 浓度
浓度
(4)实验室各种浓度的硫酸是由浓硫酸稀释而得,
①以下配制过程中各操作的先后顺序是___________ 。
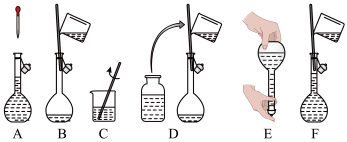
②下列情况会使配制结果偏大的是___________ 。
a.溶解后未冷却即转移、定容
b.定容时仰视容量瓶刻度线
c.用量筒量取一定体积的浓硫酸时俯视
d.将量筒、烧杯、玻璃棒洗涤2~3次,转移至容量瓶

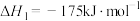 Ⅰ
Ⅰ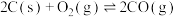
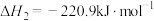 Ⅱ
Ⅱ请回答下列问题:
(1)
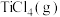 与
与 反应生成
反应生成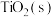 、
、 和氯气的热化学方程式为
和氯气的热化学方程式为(2)若反应Ⅱ的逆反应的活化能为
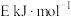 ,则E
,则E(3)t℃时,向
 恒容密闭容器中充入
恒容密闭容器中充入 和
和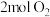 ,发生反应Ⅰ。
,发生反应Ⅰ。 时达到平衡,测得
时达到平衡,测得 的物质的量为
的物质的量为 。
。①
 内,用
内,用 表示的反应速率
表示的反应速率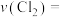
②
 的平衡转化率为
的平衡转化率为③该反应的平衡常数为
④下列措施,既能加快逆反应速率又能增大
 平衡转化率的是
平衡转化率的是A.缩小容器容积 B.加入催化剂 C.分离出部分
 D.增大
D.增大 浓度
浓度(4)实验室各种浓度的硫酸是由浓硫酸稀释而得,
①以下配制过程中各操作的先后顺序是

②下列情况会使配制结果偏大的是
a.溶解后未冷却即转移、定容
b.定容时仰视容量瓶刻度线
c.用量筒量取一定体积的浓硫酸时俯视
d.将量筒、烧杯、玻璃棒洗涤2~3次,转移至容量瓶
您最近一年使用:0次
名校
解题方法
6 . 常温下,下列溶液中各离子浓度关系一定正确的是
A.  溶液与 溶液与  溶液等体积混合: 溶液等体积混合: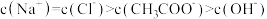 |
B. 碳酸氢钠溶液: 碳酸氢钠溶液: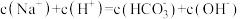 |
C.  溶液: 溶液: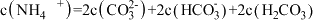 |
D.等体积、等物质的量浓度的 和弱酸 和弱酸 混合后的溶液中, 若溶液呈酸性,则有: 混合后的溶液中, 若溶液呈酸性,则有: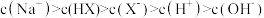 |
您最近一年使用:0次
2024-03-15更新
|
153次组卷
|
2卷引用:天津市宁河区芦台第一中学2024届高三下学期适应性模拟训练(3月)化学试题
名校
解题方法
7 . 室温下,下列指定溶液中微粒物质的量浓度关系正确的(溶液混合引起的体积变化可忽略)
A.0.20 mol/L氨水: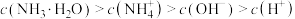 |
B.0.20 mol/L NH4F溶液(pH<7):加水稀释后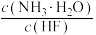 的值减小 的值减小 |
C.0.20 mol/L氨水与0.20 mol/L NH4Cl溶液等体积混合(pH=9.25):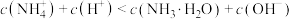 |
D.0.60 mol/L氨水和0.20 mol/L NH4HCO3溶液等体积混合: |
您最近一年使用:0次
名校
解题方法
8 . 如图,c管为上端封口的量气管,为测定乙酸溶液浓度,量取10.00 mL待测样品加入b容器中,接通电源,进行实验。下列说法正确的是
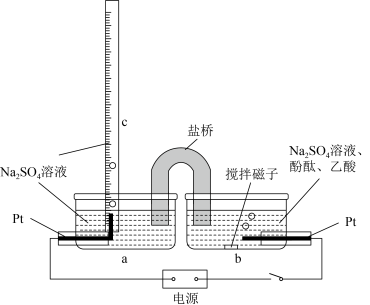

| A.左侧Pt电极连接电源的负极 |
| B.实验结束时,b中溶液红色恰好褪去 |
C.若c中收集气体11.20 mL(已折合为标准状况),则样品中乙酸浓度为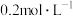 |
| D.把盐桥换为U形铜导线,不影响测定结果 |
您最近一年使用:0次
名校
解题方法
9 . 甲~戊均为短周期元素,在元素周期表中的相对位置如图所示。戊的最高价氧化物对应的水化物为强酸。下列说法不正确 的是
| 甲 | 乙 | |
| 丙 | 丁 | 戊 |
| A.原子半径:丁>戊>乙 |
| B.乙的简单氢化物的沸点一定高于戊的简单氢化物的沸点 |
| C.甲的简单氢化物遇氯化氢一定有白烟产生 |
| D.丙的最高价氧化物对应的水化物一定能与强碱反应 |
您最近一年使用:0次
名校
解题方法
10 . 北京冬奥会成功举办、神舟十三号顺利往返、“天宫课堂”如期开讲及“华龙一号”核电海外投产等,均展示了我国科技发展的巨大成就。下列相关叙述正确的是
| A.冬奥会“飞扬”火炬所用的燃料H2为氧化性气体 |
| B.飞船返回舱表层材料中的玻璃纤维属于天然有机高分子 |
| C.乙酸钠过饱和溶液析出晶体并放热的过程仅涉及化学变化 |
D.核电站反应堆所用的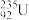 与 与 是中子数不同质子数相同的不同种核素 是中子数不同质子数相同的不同种核素 |
您最近一年使用:0次



