名校
1 . 下列所示装置或操作能达到实验目的的是
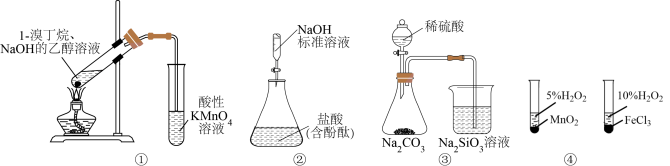

| A.图①:验证1-溴丁烷发生消去反应 |
B.图②: 标准溶液滴定盐酸 标准溶液滴定盐酸 |
| C.图③:比较硫、碳、硅三种元素的非金属性强弱 |
| D.图④:比较不同催化剂对反应速率的影响 |
您最近一年使用:0次
名校
2 . 下列装置适用于实验室制氨并验证氨的某化学性质,其中能达到实验目的的是


| A.用装置甲制取氨 |
| B.用装置乙制取并收集氨 |
| C.用装置丙除去氨中的水蒸气 |
| D.丁的原理为NH3+HCl=NH4Cl |
您最近一年使用:0次
名校
解题方法
3 . 下列设计的实验方案能达到实验目的的是( )
| 实验方案 | 实验目的 | |
| A | 取三种试剂各10mL于试管中,再分别加入5mL蒸馏水,振荡、静置,观察现象 | 鉴别苯、乙醇、四氯化碳三种无色液体 |
| B | 向MgCl2、FeCl3的混合溶液中滴加少量NaOH溶液,观察现象 | 比较Ksp[Fe(OH)3]、Ksp[Mg(OH)2]的大小 |
| C | 取溶液少许,向其中滴加BaCl2溶液,向所得沉淀中加入足量稀硫酸,观察现象 | 检验久置的亚硫酸钠溶液是否变质 |
| D | 向苯酚稀溶液中加入过量的饱和溴水,充分反应后静置,向上层清液中滴加硝酸银溶液,观察现象 | 证明苯酚与溴水反应是取代反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 . 比较乙酸、碳酸、苯酚的酸性强弱的实验如图所示,下列说法正确的是
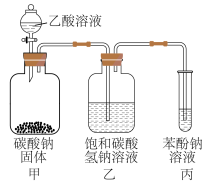
A.甲中反应:2H++CO =H2O+CO2↑ =H2O+CO2↑ |
| B.乙中的NaHCO3溶液可改为NaOH溶液 |
| C.丙中出现浑浊说明碳酸的酸性强于苯酚的 |
| D.去除乙装置仍可达到该实验目的 |
您最近一年使用:0次
2022-11-05更新
|
479次组卷
|
5卷引用:天津市天津中学2023-2024学年高三下学期期初检测化学试卷
名校
5 . 回答下列问题:
(1)下列为用氯化铁固体制备氢氧化铁胶体的相关实验,可以达到实验目的的是___________。
(2)磷的一种化合物叫亚磷酸(H3PO3)。已知:
Ⅰ.0.1mol/LH3PO3溶液的pH=1.7;
Ⅱ.H3PO3与NaOH反应只生成Na2HPO3和NaH2PO3两种盐;
Ⅲ.H3PO3和碘水反应,碘水棕黄色褪去,再加AgNO3有黄色沉淀生成。
①关于H3PO3的说法:①强酸;②弱酸;③二元酸;④三元酸;⑤氧化性酸;⑥还原性酸,其中正确的是___________ 。
A.②④⑥ B.②③⑥ C.①④⑤ D.②③⑤
②写出H3PO3与过量NaOH溶液反应的离子方程式___________ 。
(3)H3PO2(次磷酸)是一元中强酸,H3PO2及NaH2PO2均可将溶液中的 还原为银,从而可用于化学镀银。
还原为银,从而可用于化学镀银。
①NaH2PO2属于___________ (填“正盐”“酸式盐”或“碱式盐”)。
②利用H3PO2化学镀银,反应中氧化剂与还原剂的物质的量之比为4∶1,则氧化产物为___________ (写化学式)。
(1)下列为用氯化铁固体制备氢氧化铁胶体的相关实验,可以达到实验目的的是___________。
| A | B | C | D |
| 配制FeCl3溶液制备 | Fe(OH)3胶体 | 观察胶体的丁达尔效应 | 分离Fe(OH)3胶体与溶液 |
 |  |  | 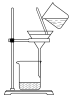 |
| A.A | B.B | C.C | D.D |
Ⅰ.0.1mol/LH3PO3溶液的pH=1.7;
Ⅱ.H3PO3与NaOH反应只生成Na2HPO3和NaH2PO3两种盐;
Ⅲ.H3PO3和碘水反应,碘水棕黄色褪去,再加AgNO3有黄色沉淀生成。
①关于H3PO3的说法:①强酸;②弱酸;③二元酸;④三元酸;⑤氧化性酸;⑥还原性酸,其中正确的是
A.②④⑥ B.②③⑥ C.①④⑤ D.②③⑤
②写出H3PO3与过量NaOH溶液反应的离子方程式
(3)H3PO2(次磷酸)是一元中强酸,H3PO2及NaH2PO2均可将溶液中的
 还原为银,从而可用于化学镀银。
还原为银,从而可用于化学镀银。①NaH2PO2属于
②利用H3PO2化学镀银,反应中氧化剂与还原剂的物质的量之比为4∶1,则氧化产物为
您最近一年使用:0次
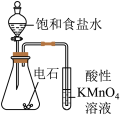
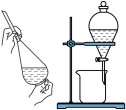
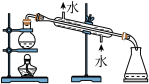
6 . 用下图所示装置及药品进行实验,能达到对应实验目的的是
 |  |
| 图1 | 图2 |
 |  |
| 图3 | 图4 |
| A.图1:实验室制氨气 | B.图2:检验乙炔具有还原性 |
| C.图3:用乙醇萃取碘水中的I2 | D.图4:用海水制取蒸馏水 |
您最近一年使用:0次
2021-01-23更新
|
523次组卷
|
5卷引用:天津市武清区杨村一中2023-2024学年高三上学期开学检测化学试题
名校
解题方法
7 . 草酸亚铁晶体( ,相对分子质量为180)呈淡黄色,可用作照相显影剂。某实验小组对其进行了一系列探究。
,相对分子质量为180)呈淡黄色,可用作照相显影剂。某实验小组对其进行了一系列探究。
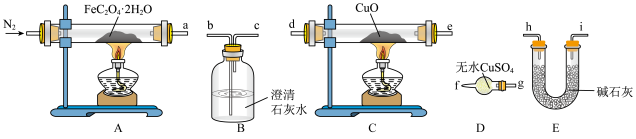
I.纯净草酸亚铁晶体热分解产物的探究
(1)气体产物成分的探究。小组成员采用如下装置(可重复选用)进行实验:
①装置D的名称为___________ 。
②按照气流从左到右的方向,上述装置的连接顺序为___________ →尾气处理装置(填仪器接口的字母编号)。
③实验前先通入一段时间 ,其目的为
,其目的为___________ 。
④实验证明气体产物中含有CO,依据的实验现象为___________ 。
(2)固体产物成分的探究。充分反应后,A处以应管中残留黑色固体。查阅资料可知,黑色固体可能为Fe或FeO。小组成员设计实验证明了其成分只有FeO,其操作及现象为___________ 。
(3)依据(1)和(2)中结论,可知A处反应管中发生反应的化学方程式为___________ 。
II.草酸亚铁晶体样品纯度的测定
工业制得的草酸亚铁晶体中常含有 杂质,测定其纯度的步骤如下:
杂质,测定其纯度的步骤如下:
步骤1:称取m g草酸亚铁晶体样品并溶于稀 中,配成250mL溶液;
中,配成250mL溶液;
步骤2:取上述溶液25.00mL,用c
 标准液滴定至终点,消耗标准液
标准液滴定至终点,消耗标准液 mL;
mL;
步骡3:向反应后溶液中加入适量锌粉,充分反应后,加入适量稀 ,再用c
,再用c
 标准溶液滴定至终点,消耗标准液
标准溶液滴定至终点,消耗标准液 mL。
mL。
(4)步骤3中加入锌粉的目的为___________ 。
(5)草酸亚铁晶体样品的纯度为___________ (列出计算式即可,不必化简);
若步骤1配制溶液时部分 被氧化,则测定结果将
被氧化,则测定结果将___________ (填“偏高”“偏低”或“不变”)。
 ,相对分子质量为180)呈淡黄色,可用作照相显影剂。某实验小组对其进行了一系列探究。
,相对分子质量为180)呈淡黄色,可用作照相显影剂。某实验小组对其进行了一系列探究。
I.纯净草酸亚铁晶体热分解产物的探究
(1)气体产物成分的探究。小组成员采用如下装置(可重复选用)进行实验:
①装置D的名称为
②按照气流从左到右的方向,上述装置的连接顺序为
③实验前先通入一段时间
 ,其目的为
,其目的为④实验证明气体产物中含有CO,依据的实验现象为
(2)固体产物成分的探究。充分反应后,A处以应管中残留黑色固体。查阅资料可知,黑色固体可能为Fe或FeO。小组成员设计实验证明了其成分只有FeO,其操作及现象为
(3)依据(1)和(2)中结论,可知A处反应管中发生反应的化学方程式为
II.草酸亚铁晶体样品纯度的测定
工业制得的草酸亚铁晶体中常含有
 杂质,测定其纯度的步骤如下:
杂质,测定其纯度的步骤如下:步骤1:称取m g草酸亚铁晶体样品并溶于稀
 中,配成250mL溶液;
中,配成250mL溶液;步骤2:取上述溶液25.00mL,用c

 标准液滴定至终点,消耗标准液
标准液滴定至终点,消耗标准液 mL;
mL;步骡3:向反应后溶液中加入适量锌粉,充分反应后,加入适量稀
 ,再用c
,再用c
 标准溶液滴定至终点,消耗标准液
标准溶液滴定至终点,消耗标准液 mL。
mL。(4)步骤3中加入锌粉的目的为
(5)草酸亚铁晶体样品的纯度为
若步骤1配制溶液时部分
 被氧化,则测定结果将
被氧化,则测定结果将
您最近一年使用:0次
8 . 利用如图所示装置(夹持装置略)进行实验,b中现象不能 证明a中产物生成的是
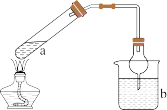
| a中反应 | b中检测试剂及现象 | |
| A | 浓 分解生成 分解生成 | 淀粉 溶液变蓝 溶液变蓝 |
| B |  与浓 与浓 生成 生成 | 品红溶液褪色 |
| C | 浓 与 与 溶液生成 溶液生成 | 酚酞溶液变红 |
| D | 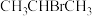 与 与 乙醇溶液生成丙烯 乙醇溶液生成丙烯 | 溴水褪色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-07-01更新
|
9754次组卷
|
25卷引用:天津市耀华中学2023-2024学年高三下学期开学验收考化学试卷
天津市耀华中学2023-2024学年高三下学期开学验收考化学试卷(已下线)2022年北京市高考真题化学试题(部分试题)(已下线)考点53 化学实验方案设计与评价-备战2023年高考化学一轮复习考点帮(全国通用)2022年北京市高考真题化学试题(已下线)2022年北京高考真题变式题1-14(已下线)微专题43 常见物质的分离、提纯和鉴别-备战2023年高考化学考点微专题(全国版)浙江省东阳市横店高级中学2022-2023学年高三上学期10月份检测化学试题(已下线)热点情景汇编-专题四 元素及其化合物福建省福州第十五中学2022-2023学年高三上学期11月线上限时训练化学试题突破超重点 牢固掌握实验重点 超重点4 物质检验与鉴别的方法(已下线)专题23 化学实验基础性选择题-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)素养卷07 微型物质制备方案设计-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)回归教材重难点10 再现常考化学实验基础知识-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)(已下线)2022年北京高考真题化学试题变式题(选择题6-10)北京市第八十中学2023届高三下学期二模适应考试化学试题江苏省苏州市苏州高新区第一中学2022-2023学年高一下学期5月月考化学试题(已下线)专题07 无机物的转化 微型工艺流程-2023年高考化学真题题源解密(全国通用)(已下线)考点44 化学实验基础(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)考点2 物质的分离、提纯、检验与鉴别 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)考点3 物质的制备与性质实验 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)第3讲 卤代烃、醇、酚(已下线)第3讲 物质制备实验的设计与评价北京汇文中学2023-2024学年高三上学期11月期中考试化学试题北京市第十四中学2023-2024学年高三下学期三模化学试题北京师范大学附属中学2024届高三下学期三模化学试题
名校
9 . 烟道气中含氧NO、 、
、 等多种有害气体,合理治理烟道气中具有重要意义。
等多种有害气体,合理治理烟道气中具有重要意义。
(1)烟道气中的氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:


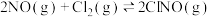

则反应: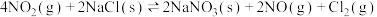

___________ (用含 、
、 的式子表示)。
的式子表示)。
(2)利用CO可将NO转化为无害的 ,其反应为:
,其反应为: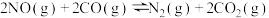 。在容积均为2L的甲、乙两个恒温(反应温度分别为
。在容积均为2L的甲、乙两个恒温(反应温度分别为 ℃、
℃、 ℃)恒容密闭容器中,分别加入物质的量之比为1∶1的NO和CO,测得各容器中
℃)恒容密闭容器中,分别加入物质的量之比为1∶1的NO和CO,测得各容器中 随反应时间t的变化情况如下表所示:
随反应时间t的变化情况如下表所示:
①已知 ,则该反应的△H
,则该反应的△H___________ 0(填“>”或“<”)。
②甲容器达平衡时,体系的压强与反应开始时体系的压强之比为___________ 。
(3)对烟道气中的 进行回收再利用具有较高的社会价值和经济价值。
进行回收再利用具有较高的社会价值和经济价值。
其反应为: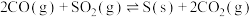
①写出该反应平衡常数表达式___________ 。
②由 和CO反应生成S和
和CO反应生成S和 的能量变化如图甲所示,在恒温恒容的密闭容器中进行反应,对此反应下列说法正确的是
的能量变化如图甲所示,在恒温恒容的密闭容器中进行反应,对此反应下列说法正确的是___________ 。
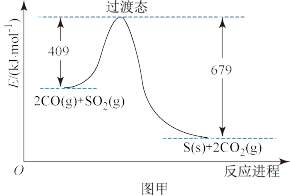
a.若混合气体密度保持不变,则已达平衡状态
b.从反应开始到平衡,容器内气体的压强保持不变
c.达平衡后若再充入一定量 ,新平衡体系混合气体中CO的体积分数增大
,新平衡体系混合气体中CO的体积分数增大
d.分离出一部分S,正、逆反应速率均保持不变
(4)用电化学法模拟工业处理对烟道气中的 。如图乙装置(电极均为惰性材料)进行实验,可用于制备硫酸,同时获得电能。
。如图乙装置(电极均为惰性材料)进行实验,可用于制备硫酸,同时获得电能。
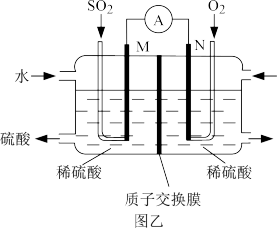
①M极发生的电极反应式为___________ 。
②当外电路通过0.2mol电子时,质子交换膜右侧的溶液质量___________ (填“增大”或“减小”),___________ g。
 、
、 等多种有害气体,合理治理烟道气中具有重要意义。
等多种有害气体,合理治理烟道气中具有重要意义。(1)烟道气中的氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:


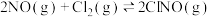

则反应:
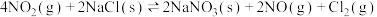

 、
、 的式子表示)。
的式子表示)。(2)利用CO可将NO转化为无害的
 ,其反应为:
,其反应为: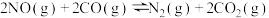 。在容积均为2L的甲、乙两个恒温(反应温度分别为
。在容积均为2L的甲、乙两个恒温(反应温度分别为 ℃、
℃、 ℃)恒容密闭容器中,分别加入物质的量之比为1∶1的NO和CO,测得各容器中
℃)恒容密闭容器中,分别加入物质的量之比为1∶1的NO和CO,测得各容器中 随反应时间t的变化情况如下表所示:
随反应时间t的变化情况如下表所示:t/min /mol /mol | 0 | 10 | 20 | 30 | 40 |
甲( ℃) ℃) | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
乙( ℃) ℃) | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
 ,则该反应的△H
,则该反应的△H②甲容器达平衡时,体系的压强与反应开始时体系的压强之比为
(3)对烟道气中的
 进行回收再利用具有较高的社会价值和经济价值。
进行回收再利用具有较高的社会价值和经济价值。其反应为:
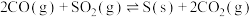
①写出该反应平衡常数表达式
②由
 和CO反应生成S和
和CO反应生成S和 的能量变化如图甲所示,在恒温恒容的密闭容器中进行反应,对此反应下列说法正确的是
的能量变化如图甲所示,在恒温恒容的密闭容器中进行反应,对此反应下列说法正确的是
a.若混合气体密度保持不变,则已达平衡状态
b.从反应开始到平衡,容器内气体的压强保持不变
c.达平衡后若再充入一定量
 ,新平衡体系混合气体中CO的体积分数增大
,新平衡体系混合气体中CO的体积分数增大d.分离出一部分S,正、逆反应速率均保持不变
(4)用电化学法模拟工业处理对烟道气中的
 。如图乙装置(电极均为惰性材料)进行实验,可用于制备硫酸,同时获得电能。
。如图乙装置(电极均为惰性材料)进行实验,可用于制备硫酸,同时获得电能。
①M极发生的电极反应式为
②当外电路通过0.2mol电子时,质子交换膜右侧的溶液质量
您最近一年使用:0次
名校
解题方法
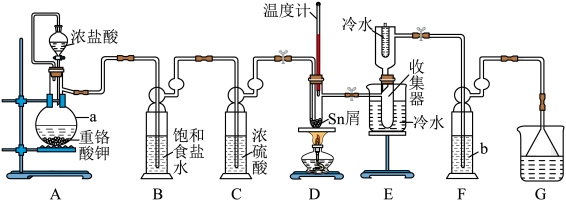
10 . 无水四氯化锡( )常用作有机合成的氯化催化剂。实验室可用熔融的锡(熔点为232℃)与
)常用作有机合成的氯化催化剂。实验室可用熔融的锡(熔点为232℃)与 反应制备
反应制备 ,装置如图所示。
,装置如图所示。
已知:① 在潮湿空气中极易水解生成
在潮湿空气中极易水解生成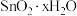
②各物质熔沸点:
(1)仪器a的名称为___________ ,重铬酸钾( )与浓盐酸反应时,还原产物是
)与浓盐酸反应时,还原产物是 ,装置A中发生反应的离子方程式为
,装置A中发生反应的离子方程式为___________ 。
(2)F装置中试剂b为___________ ,其作用是___________ 。
(3)锡屑中含铜杂质导致D中产生 ,但不影响E中产品的纯度,原因是
,但不影响E中产品的纯度,原因是___________ 。
(4)E所得产品 中常溶有少量
中常溶有少量 杂质,可用
杂质,可用___________ 方法提纯。
(5)制得的 产品中常含有
产品中常含有 ,可用如下方法测定产品纯度:先准确称量7.60g产品于锥形瓶中,再加过量的
,可用如下方法测定产品纯度:先准确称量7.60g产品于锥形瓶中,再加过量的 溶液,发生反应:
溶液,发生反应: ,再用
,再用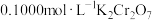 标准溶液滴定生成的
标准溶液滴定生成的 ,此时还原产物为
,此时还原产物为 ,消耗标准溶液20.00mL,则
,消耗标准溶液20.00mL,则 产品的纯度为
产品的纯度为___________ 。
 )常用作有机合成的氯化催化剂。实验室可用熔融的锡(熔点为232℃)与
)常用作有机合成的氯化催化剂。实验室可用熔融的锡(熔点为232℃)与 反应制备
反应制备 ,装置如图所示。
,装置如图所示。
已知:①
 在潮湿空气中极易水解生成
在潮湿空气中极易水解生成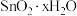
②各物质熔沸点:
| 物质 | 熔点/℃ | 沸点/℃ |
 | 246 | 652 |
 | -33 | 114 |
 | 620 | 993 |
 )与浓盐酸反应时,还原产物是
)与浓盐酸反应时,还原产物是 ,装置A中发生反应的离子方程式为
,装置A中发生反应的离子方程式为(2)F装置中试剂b为
(3)锡屑中含铜杂质导致D中产生
 ,但不影响E中产品的纯度,原因是
,但不影响E中产品的纯度,原因是(4)E所得产品
 中常溶有少量
中常溶有少量 杂质,可用
杂质,可用(5)制得的
 产品中常含有
产品中常含有 ,可用如下方法测定产品纯度:先准确称量7.60g产品于锥形瓶中,再加过量的
,可用如下方法测定产品纯度:先准确称量7.60g产品于锥形瓶中,再加过量的 溶液,发生反应:
溶液,发生反应: ,再用
,再用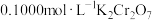 标准溶液滴定生成的
标准溶液滴定生成的 ,此时还原产物为
,此时还原产物为 ,消耗标准溶液20.00mL,则
,消耗标准溶液20.00mL,则 产品的纯度为
产品的纯度为
您最近一年使用:0次



