1 . 一定温度下,AgCl和 的沉淀溶解平衡曲线如图所示。
的沉淀溶解平衡曲线如图所示。
 的沉淀溶解平衡曲线如图所示。
的沉淀溶解平衡曲线如图所示。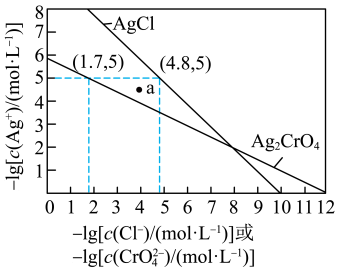
A.a点为 的不饱和溶液 的不饱和溶液 |
B.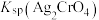 的数量级等于 的数量级等于 |
C.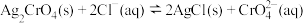 的平衡常数 的平衡常数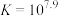 |
D.向NaCl、 均为 均为 的混合溶液中滴加 的混合溶液中滴加 溶液,先产生 溶液,先产生 沉淀 沉淀 |
您最近一年使用:0次
2 . 下列离子方程式书写正确的是
A.向NaOH溶液中滴加 溶液: 溶液: |
B.向AgCl悬浊液中滴加过量 溶液: 溶液: |
C.向 溶液中滴加氨水: 溶液中滴加氨水: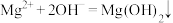 |
D.泡沫灭火器的反应原理: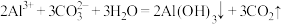 |
您最近一年使用:0次
解题方法
3 . 反应物(S)转化为产物(P或P·Z)的能量与反应进程的关系如下图所示:
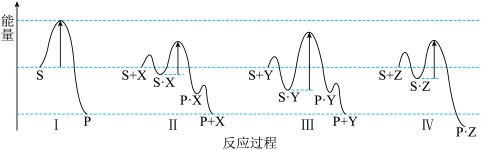
| A.进程Ⅰ是吸热反应 |
| B.生成P的速率:Ⅱ>Ⅲ |
| C.平衡时P的产率:Ⅱ>Ⅰ |
| D.进程Ⅳ中,Z有催化作用 |
您最近一年使用:0次
解题方法
4 . 利用NaOH标准溶液滴定食醋中醋酸的浓度,下列操作正确的是
| A.锥形瓶洗净后需要用待测食醋润洗 |
| B.碱式滴定管用NaOH标准溶液润洗后,润洗液应从滴定管上口倒出 |
| C.滴定读数时,应双手一上一下持滴定管 |
| D.在使用前,若酸式滴定管旋塞处存在轻微漏水现象;可在旋塞处涂抹适量凡士林 |
您最近一年使用:0次
解题方法
5 . 在恒温恒容密闭容器中充入一定量W(g),发生如下反应:反应②和③的速率方程分别为 和
和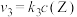 ,其中
,其中 、
、 分别为反应②和③的速率常数。测得c(W)的浓度随时间t的变化如下表。
分别为反应②和③的速率常数。测得c(W)的浓度随时间t的变化如下表。
下列说法正确的是
 和
和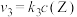 ,其中
,其中 、
、 分别为反应②和③的速率常数。测得c(W)的浓度随时间t的变化如下表。
分别为反应②和③的速率常数。测得c(W)的浓度随时间t的变化如下表。
 | 0 | 1 | 2 | 3 | 4 | 5 | …… |
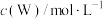 | 0.160 | 0.113 | 0.080 | 0.056 | 0.040 | 0.028 | …… |
A.0~4min内, |
| B.若增大容器容积,平衡时W的转化率增大 |
C.若 ,平衡时 ,平衡时 |
| D.达到平衡后,再充入一定量的W(g),混合气体的平均摩尔质量增大 |
您最近一年使用:0次
6 . 常温下,下列有关氨水的说法正确的是
| A.等物质的量浓度的氨水与NaOH溶液,导电能力相同 |
B.往氨水中加水稀释, 逐渐减小 逐渐减小 |
C.pH均为10的氨水与 溶液中, 溶液中, 相等 相等 |
| D.pH=11的氨水与pH=3的盐酸等体积混合后溶液显酸性 |
您最近一年使用:0次
7 . 化学与生活、生产和社会息息相关,下列说法不正确的是
| A.聚合硫酸铁具有氧化性,可用于自来水杀菌消毒 |
B.将 溶液加热、蒸干、灼烧,可得到 溶液加热、蒸干、灼烧,可得到 固体 固体 |
C.牙膏中添加氟化物,可将 转化为更难溶的 转化为更难溶的 抵抗酸的侵蚀 抵抗酸的侵蚀 |
D.侯氏制碱法中将精制的饱和食盐水先氨化再碳酸化,以获得更多的 沉淀 沉淀 |
您最近一年使用:0次
8 . 近年来,人类航天科技事业取得了辉煌的成就。下列说法错误的是
| A.某型长征运载火箭以液氧和煤油为推进剂,液氧分子间靠范德华力聚集在一起 |
B.聚乳酸可用于航天、汽车领域,其合成原料乳酸(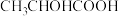 )具有旋光性 )具有旋光性 |
C.“嫦娥石”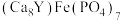 是我国在月壤中发现的新型矿物,所含的磷位于元素周期表中的p区 是我国在月壤中发现的新型矿物,所含的磷位于元素周期表中的p区 |
| D.航天员出舱服应用了碳纤维复合材料,所含基态碳原子核外电子空间运动状态有6种 |
您最近一年使用:0次
名校
解题方法
9 . 已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用,请回答下列问题:

(1)该“84消毒液”的物质的量浓度约为_______ mol/L。(保留两位有效数字)。
(2)在配制过程中,除需要烧杯、托盘天平外还必需的仪器有__________ (写三种)。
(3)某同学取100mL该“84消毒液”稀释后用于消毒,稀释后的溶液中c(Na+)=________ mol/L。
(4)配制时,其正确的操作顺序是_________________ (字母表示,每个字母只能用一次)。
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需浓消毒液的体积,倒入烧杯中再慢慢沿杯壁注入少量水,用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的溶液沿玻璃棒注入一定体积的容量瓶中
D.将容量瓶盖紧,颠倒摇匀
E.继续往容量瓶内小心加水,直到液面接近刻度线1~2cm处
(5)“84消毒液”和空气中的某种气体接触,具有强消毒能力,试用化学方程式解释原因:______________ 。
(6)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480mL含NaClO质量分数为25%的消毒液。下列说法正确的是________(填字母)。


(1)该“84消毒液”的物质的量浓度约为
(2)在配制过程中,除需要烧杯、托盘天平外还必需的仪器有
(3)某同学取100mL该“84消毒液”稀释后用于消毒,稀释后的溶液中c(Na+)=
(4)配制时,其正确的操作顺序是
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需浓消毒液的体积,倒入烧杯中再慢慢沿杯壁注入少量水,用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的溶液沿玻璃棒注入一定体积的容量瓶中
D.将容量瓶盖紧,颠倒摇匀
E.继续往容量瓶内小心加水,直到液面接近刻度线1~2cm处
(5)“84消毒液”和空气中的某种气体接触,具有强消毒能力,试用化学方程式解释原因:
(6)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480mL含NaClO质量分数为25%的消毒液。下列说法正确的是________(填字母)。

| A.如图所示的仪器中,有三种是不需要的,还需要一种玻璃仪器 |
| B.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制 |
| C.定容后,摇匀时发现少量液体渐出,对浓度无影响 |
| D.需要称量NaClO固体的质量为149.0g |
您最近一年使用:0次
名校
解题方法
10 . 研究实验发现硝酸的浓度越稀,硝酸发生氧化还原反应时,对应还原产物中氮元素的化合价越低。现有一定量的铝粉和铁粉的混合物与一定量很稀的硝酸充分反应,反应过程中无气体放出,在反应结束后的溶液中逐滴加入5mol/LNaOH溶液,所加NaOH溶液的体积与产生沉淀的物质的量关系如图所示,下列说法不正确的是


| A.该稀硝酸与铝粉、铁粉反应,其还原产物为硝酸铵 |
| B.c点对应NaOH溶液的体积为40mL |
| C.b点与a点的差值为0.03mol |
| D.样品中铝粉和铁粉的物质的量之比为3∶5 |
您最近一年使用:0次



