1 . 一定温度下,AgCl和 的沉淀溶解平衡曲线如图所示。
的沉淀溶解平衡曲线如图所示。
 的沉淀溶解平衡曲线如图所示。
的沉淀溶解平衡曲线如图所示。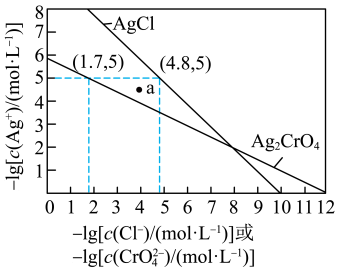
A.a点为 的不饱和溶液 的不饱和溶液 |
B.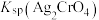 的数量级等于 的数量级等于 |
C.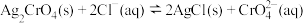 的平衡常数 的平衡常数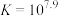 |
D.向NaCl、 均为 均为 的混合溶液中滴加 的混合溶液中滴加 溶液,先产生 溶液,先产生 沉淀 沉淀 |
您最近一年使用:0次
2 . 下列离子方程式书写正确的是
A.向NaOH溶液中滴加 溶液: 溶液: |
B.向AgCl悬浊液中滴加过量 溶液: 溶液: |
C.向 溶液中滴加氨水: 溶液中滴加氨水: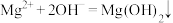 |
D.泡沫灭火器的反应原理: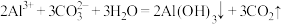 |
您最近一年使用:0次
解题方法
3 . 反应物(S)转化为产物(P或P·Z)的能量与反应进程的关系如下图所示:
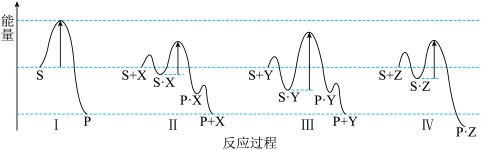
| A.进程Ⅰ是吸热反应 |
| B.生成P的速率:Ⅱ>Ⅲ |
| C.平衡时P的产率:Ⅱ>Ⅰ |
| D.进程Ⅳ中,Z有催化作用 |
您最近一年使用:0次
解题方法
4 . 利用NaOH标准溶液滴定食醋中醋酸的浓度,下列操作正确的是
| A.锥形瓶洗净后需要用待测食醋润洗 |
| B.碱式滴定管用NaOH标准溶液润洗后,润洗液应从滴定管上口倒出 |
| C.滴定读数时,应双手一上一下持滴定管 |
| D.在使用前,若酸式滴定管旋塞处存在轻微漏水现象;可在旋塞处涂抹适量凡士林 |
您最近一年使用:0次
解题方法
5 . 在恒温恒容密闭容器中充入一定量W(g),发生如下反应:反应②和③的速率方程分别为 和
和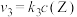 ,其中
,其中 、
、 分别为反应②和③的速率常数。测得c(W)的浓度随时间t的变化如下表。
分别为反应②和③的速率常数。测得c(W)的浓度随时间t的变化如下表。
下列说法正确的是
 和
和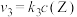 ,其中
,其中 、
、 分别为反应②和③的速率常数。测得c(W)的浓度随时间t的变化如下表。
分别为反应②和③的速率常数。测得c(W)的浓度随时间t的变化如下表。
 | 0 | 1 | 2 | 3 | 4 | 5 | …… |
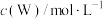 | 0.160 | 0.113 | 0.080 | 0.056 | 0.040 | 0.028 | …… |
A.0~4min内, |
| B.若增大容器容积,平衡时W的转化率增大 |
C.若 ,平衡时 ,平衡时 |
| D.达到平衡后,再充入一定量的W(g),混合气体的平均摩尔质量增大 |
您最近一年使用:0次
6 . 常温下,下列有关氨水的说法正确的是
| A.等物质的量浓度的氨水与NaOH溶液,导电能力相同 |
B.往氨水中加水稀释, 逐渐减小 逐渐减小 |
C.pH均为10的氨水与 溶液中, 溶液中, 相等 相等 |
| D.pH=11的氨水与pH=3的盐酸等体积混合后溶液显酸性 |
您最近一年使用:0次
7 . 化学与生活、生产和社会息息相关,下列说法不正确的是
| A.聚合硫酸铁具有氧化性,可用于自来水杀菌消毒 |
B.将 溶液加热、蒸干、灼烧,可得到 溶液加热、蒸干、灼烧,可得到 固体 固体 |
C.牙膏中添加氟化物,可将 转化为更难溶的 转化为更难溶的 抵抗酸的侵蚀 抵抗酸的侵蚀 |
D.侯氏制碱法中将精制的饱和食盐水先氨化再碳酸化,以获得更多的 沉淀 沉淀 |
您最近一年使用:0次
8 . 近年来,人类航天科技事业取得了辉煌的成就。下列说法错误的是
| A.某型长征运载火箭以液氧和煤油为推进剂,液氧分子间靠范德华力聚集在一起 |
B.聚乳酸可用于航天、汽车领域,其合成原料乳酸(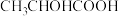 )具有旋光性 )具有旋光性 |
C.“嫦娥石”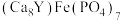 是我国在月壤中发现的新型矿物,所含的磷位于元素周期表中的p区 是我国在月壤中发现的新型矿物,所含的磷位于元素周期表中的p区 |
| D.航天员出舱服应用了碳纤维复合材料,所含基态碳原子核外电子空间运动状态有6种 |
您最近一年使用:0次
解题方法
9 . X、Y、Z、Q、R、T、U分别代表原子数依次增大的短周期主族元素,在周期表的短周期在族元素中,X的原子半径最小,X与R的最外层电子数相等;Y的内层电子数是最外层电子数的一半,U的最高化合价和最低化合价的代数和为6;Z与Q相邻,两者原子序数之和为15;R和Q可形成原子个数之比为1:1和2:1的两种化合物;R、T、U三者的最高价氧化物对应的水化物两两之间能发生化学反应。请回答下列问题:
(1)Z元素在周期表中的位置是_______ 。
(2)Q、R、T三种元素的简单离子半径由小到大的顺序为_______ (填离子符号)。
(3)T、U两元素最高价氧化物对应的水化物反应的离子方程式为_______ 。
(4)下列可以判断R和T的金属性强弱的是_______。
(5)Z元素对应的最高价氧化物对应的水化物的化合物类型是_______ 。(填“离子化合物”或“共价化合物”):Z2X4的电子式是_______ 。
(6)在托盘天平的两盘上,分别放有两个质量相同的烧杯,各盛有6mol/L盐酸100mL,使天平达到平衡。分别向两烧杯加入均不超过5g的镁和T,若要使其充分反应后天平仍然保持平衡,则加入的镁和T的质量之比是_______ 。
(1)Z元素在周期表中的位置是
(2)Q、R、T三种元素的简单离子半径由小到大的顺序为
(3)T、U两元素最高价氧化物对应的水化物反应的离子方程式为
(4)下列可以判断R和T的金属性强弱的是_______。
| A.单质的熔点:R比T低 |
| B.单质与酸反应时,失电子数R比T少 |
| C.单质与水反应:R比T更易 |
| D.最高价氧化物对应水化物的碱性:R比T强 |
(5)Z元素对应的最高价氧化物对应的水化物的化合物类型是
(6)在托盘天平的两盘上,分别放有两个质量相同的烧杯,各盛有6mol/L盐酸100mL,使天平达到平衡。分别向两烧杯加入均不超过5g的镁和T,若要使其充分反应后天平仍然保持平衡,则加入的镁和T的质量之比是
您最近一年使用:0次
10 . 某班同学用如下实验探究Fe2+与Fe3+的转化,回答下列问题,
(1)实验I:Fe3+转化为Fe2+
实验步骤及现象:甲组同学将少量铜粉加入1mL0.lmol/LFeCl3溶液中,观察到铜粉消失,溶液黄色变浅,加入蒸馏水后无明显现象:乙组同学将过量铜粉加入1mL0.lmol/LFeCl3溶液中,观察到铜粉有剩余,溶液黄色褪去,加入蒸馏水后出现白色沉淀;丙组同学将过量铜粉加入lmL0.05mol/LFe2(SO4)3溶液中,观察到铜粉有剩余,溶液黄色褪去,变成蓝色,测入蒸馏水后无白色沉淀。
①分别取三组实验反应后的溶液于三支试管中加入几滴K3[Fe(CN)6]溶液,出现蓝色沉淀,证明生成了Fe2+;分析三组实验结果,实验中均发生的反应离子方程式为_______ 。
②对比三组实验,说明加入蒸馏水后沉淀的产生与_______ 有关。
③向丙组实验后的溶液中加入饱和NaCl溶液可能出现的现象为_______ 。
④丙组在检验反应后的溶液中是否存在Fe3+时,取反应后上层清液于试管中,滴加3滴KSCN溶液,结果出现白色沉淀,查阅资料:i.SCN-的化学性质与I-相似,CuSCN为白色固体;ii.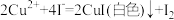 ,写出该实验中出现白色沉淀的离子方程式为
,写出该实验中出现白色沉淀的离子方程式为_______ 。
(2)实验II:Fe2+转化为Fe3+
实验步骤及现象:向3mL0.1mol/LFeSO4溶液中加入稍过量稀硝酸,溶液变为棕色,放置一段时间后,棕色消失,溶液变为黄色,已知硝酸具有氧化性, (棕色):
(棕色):
⑤使用的FeSO4溶液中存在少量铁屑,其目的是_______ 。
⑥实验中产生NO的原因为_______ (用离子方程式表示)。
(1)实验I:Fe3+转化为Fe2+
实验步骤及现象:甲组同学将少量铜粉加入1mL0.lmol/LFeCl3溶液中,观察到铜粉消失,溶液黄色变浅,加入蒸馏水后无明显现象:乙组同学将过量铜粉加入1mL0.lmol/LFeCl3溶液中,观察到铜粉有剩余,溶液黄色褪去,加入蒸馏水后出现白色沉淀;丙组同学将过量铜粉加入lmL0.05mol/LFe2(SO4)3溶液中,观察到铜粉有剩余,溶液黄色褪去,变成蓝色,测入蒸馏水后无白色沉淀。
①分别取三组实验反应后的溶液于三支试管中加入几滴K3[Fe(CN)6]溶液,出现蓝色沉淀,证明生成了Fe2+;分析三组实验结果,实验中均发生的反应离子方程式为
②对比三组实验,说明加入蒸馏水后沉淀的产生与
③向丙组实验后的溶液中加入饱和NaCl溶液可能出现的现象为
④丙组在检验反应后的溶液中是否存在Fe3+时,取反应后上层清液于试管中,滴加3滴KSCN溶液,结果出现白色沉淀,查阅资料:i.SCN-的化学性质与I-相似,CuSCN为白色固体;ii.
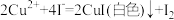 ,写出该实验中出现白色沉淀的离子方程式为
,写出该实验中出现白色沉淀的离子方程式为(2)实验II:Fe2+转化为Fe3+
实验步骤及现象:向3mL0.1mol/LFeSO4溶液中加入稍过量稀硝酸,溶液变为棕色,放置一段时间后,棕色消失,溶液变为黄色,已知硝酸具有氧化性,
 (棕色):
(棕色):⑤使用的FeSO4溶液中存在少量铁屑,其目的是
⑥实验中产生NO的原因为
您最近一年使用:0次



