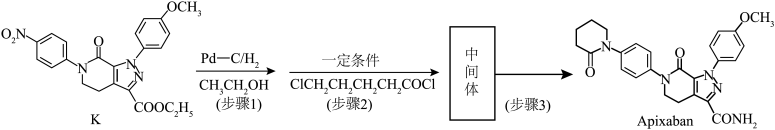
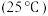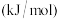1 . 阿哌沙班(Apixaban)可用于预防膝关节置换手术患者静脉血栓栓塞的发生。下图是阿哌沙班中间体K的一种合成路线:
ii.RCOOR′
______ 。
(2)B→C的化学方程式是
(3)D的分子式为C7H12O4,D的结构简式是______
(4)G→H的化学方程式是______
(5)与F含有相同官能团的同分异构体有______ 种(不考虑手性异构,不含F)
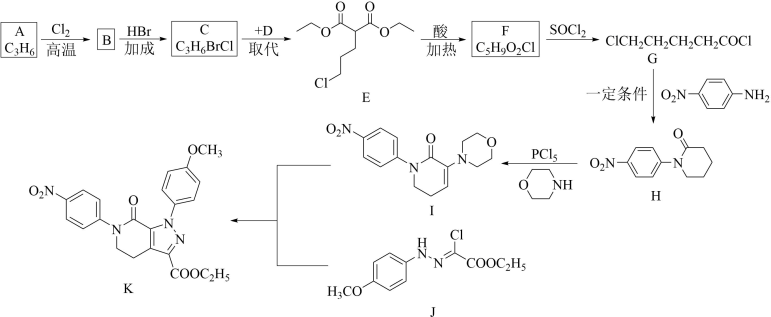
(6)K经多步合成阿哌沙班,结合K的合成路线图,写出中间体的结构简式______ ,步骤3的试剂和反应条件是______ 。
____________________________________________________

ii.RCOOR′

ⅲ.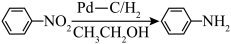
(2)B→C的化学方程式是
(3)D的分子式为C7H12O4,D的结构简式是
(4)G→H的化学方程式是
(5)与F含有相同官能团的同分异构体有
(6)K经多步合成阿哌沙班,结合K的合成路线图,写出中间体的结构简式
元素 | H | C | O |
电负性 | 2.1 | 2.5 | 3.5 |
您最近一年使用:0次
2 . I.硅、锗(32Ge,熔点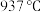 )和镓(32Ga)都是重要的半导体材料,在航空航天测控、核物理探测、光纤通讯、红外光学、太阳能电池、化学催化剂、生物医学等领域都有广泛而重要的应用。锗与硅是同主族元素。
)和镓(32Ga)都是重要的半导体材料,在航空航天测控、核物理探测、光纤通讯、红外光学、太阳能电池、化学催化剂、生物医学等领域都有广泛而重要的应用。锗与硅是同主族元素。
(1)硅在元素周期表中的位置是_______ 。
(2)硅和锗与氯元素都能形成氯化物RCl4(R代表Si和Ge)从原子结构角度解释原因
(3)镓(31Ga)是化学史上第一种先经过理论预言,后在自然界中被发现并验证的元素。基态Ga原子中,核外电子占据的最高能层的符号是______ 。
Ⅱ.氮化硼(BN)是-种高硬度、耐高温、耐腐蚀、高绝缘性的材料。一种获得氮化硼的方法如下:

已知:1.电负性:H 2.1 B 2.0 N 3.0 O 3.5
2.SiC与BN晶体的熔点和硬度数据如下:
(4)NaBH4被认为是有机化学上的“万能还原剂”。从化合价角度分析NaBH4具有强还原性的原因:______ 。
(5)硼酸的化学式为B(OH)3是一元弱酸。
硼酸产生H+过程为: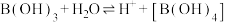
①硼酸分子的空间构型为______ 。
②硼酸具有弱酸性是由于B与水中的OH-形成配位键,描述配位键的形成过程______ 。
(6)某一种氮化硼晶体的晶胞结构如下图:
①B原子的轨道杂化类型为______ 。
②该种氮化硼的熔点和硬度均高于SiC的原因是:______ 。
③已知该晶体的密度为 ,阿伏伽德罗常数为NA,则晶胞的边长为
,阿伏伽德罗常数为NA,则晶胞的边长为______ cm(列计算式)。
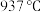 )和镓(32Ga)都是重要的半导体材料,在航空航天测控、核物理探测、光纤通讯、红外光学、太阳能电池、化学催化剂、生物医学等领域都有广泛而重要的应用。锗与硅是同主族元素。
)和镓(32Ga)都是重要的半导体材料,在航空航天测控、核物理探测、光纤通讯、红外光学、太阳能电池、化学催化剂、生物医学等领域都有广泛而重要的应用。锗与硅是同主族元素。(1)硅在元素周期表中的位置是
(2)硅和锗与氯元素都能形成氯化物RCl4(R代表Si和Ge)从原子结构角度解释原因
(3)镓(31Ga)是化学史上第一种先经过理论预言,后在自然界中被发现并验证的元素。基态Ga原子中,核外电子占据的最高能层的符号是
Ⅱ.氮化硼(BN)是-种高硬度、耐高温、耐腐蚀、高绝缘性的材料。一种获得氮化硼的方法如下:

已知:1.电负性:H 2.1 B 2.0 N 3.0 O 3.5
2.SiC与BN晶体的熔点和硬度数据如下:
物质 | 熔点/ | 硬度 |
碳化硅(SiC) | 2830 | 9-9.5 |
氮化棚(BN) | 3000 | 9.5 |
(5)硼酸的化学式为B(OH)3是一元弱酸。
硼酸产生H+过程为:
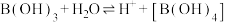
①硼酸分子的空间构型为
②硼酸具有弱酸性是由于B与水中的OH-形成配位键,描述配位键的形成过程
(6)某一种氮化硼晶体的晶胞结构如下图:
①B原子的轨道杂化类型为
②该种氮化硼的熔点和硬度均高于SiC的原因是:
③已知该晶体的密度为
 ,阿伏伽德罗常数为NA,则晶胞的边长为
,阿伏伽德罗常数为NA,则晶胞的边长为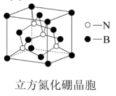
您最近一年使用:0次
3 . 烟气脱硫脱硝技术是环境科学研究的热点。某小组模拟O3氧化结合(NH4)2SO3溶液吸收法同时脱除SO2和NO。气体反应器中的主要反应原理及相关数据如下表。
不正确 的是
反应 | 平衡常数 | 活化能/ |
 |  | 24.6 |
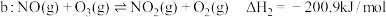 | 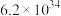 | 3.17 |
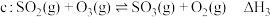 | 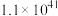 | 58.17 |
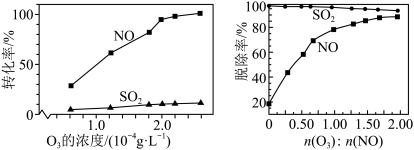
A.已知: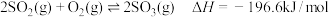 则 则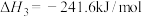 |
| B.其他条件不变,在相同时间内,SO2和NO的转化率均随温度升高而降低 |
| C.其他条件不变,在相同时间内,随O3浓度的升高,NO的转化率远远高于SO2的转化率 |
| D.其他条件不变,在相同时间内,O3的浓度很低时,SO2的脱除率远高于NO的脱除率,因为反应c速率大于反应b |
您最近一年使用:0次
4 . 下列事实能用平衡移动原理解释的是
| A.合成氨工业中使用铁触媒作催化剂 |
B.铁钉放入浓 中不再变化后,加热能产生大量红棕色气体 中不再变化后,加热能产生大量红棕色气体 |
C.氯碱工业中阳极区的溶液用盐酸调pH为2~3,促进 的产生 的产生 |
D.锌片与稀 反应过程中,加入少量 反应过程中,加入少量 固体,促进 固体,促进 的产生 的产生 |
您最近一年使用:0次
名校
解题方法
5 . 治疗心力衰竭药物沙库巴曲的合成路线如下:_______ 。
(2)A→B的反应中,已知NaClO被还原为NaCl,理论上反应 物质A,至少需要NaClO的物质的量为
物质A,至少需要NaClO的物质的量为_______ 。
(3)B的结构简式是_______ 。
(4)D→E中步骤i反应的化学方程式是_______ 。
(5)E→F反应类型是_______ ,F→G反应类型是_______ 。
(6)G与H生成沙库巴曲的反应原子利用率为100%,H分子中只有一种化学环境的氢。
①下列关于H的说法正确的是_______ (填字母序号)。
a.分子式为C4H4O3
b.分子中所有碳原子的杂化类型均相同
c.官能团为酯基和酮羰基
d.存在同时含有碳碳三键、羧基和羟基的同分异构体
已知i.
ⅱ.C2H2与甲醛反应和苯酚与甲醛反应类型相同,且产物中包含相同种类官能团。
请参照题干合成路线的表示方法,设计以C2H2、HCHO为有机原料(无机原料任选)合成H的路线_______ 。
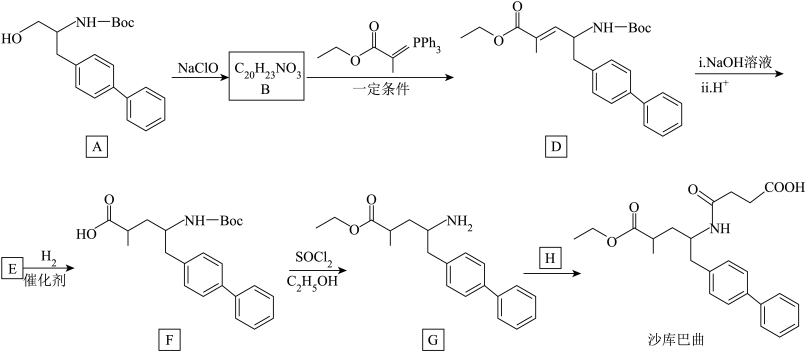
已知:-Boc结构简式为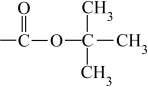
(2)A→B的反应中,已知NaClO被还原为NaCl,理论上反应
 物质A,至少需要NaClO的物质的量为
物质A,至少需要NaClO的物质的量为(3)B的结构简式是
(4)D→E中步骤i反应的化学方程式是
(5)E→F反应类型是
(6)G与H生成沙库巴曲的反应原子利用率为100%,H分子中只有一种化学环境的氢。
①下列关于H的说法正确的是
a.分子式为C4H4O3
b.分子中所有碳原子的杂化类型均相同
c.官能团为酯基和酮羰基
d.存在同时含有碳碳三键、羧基和羟基的同分异构体
②H与另一有机物I在一定条件下可以反应生成聚合物PBS(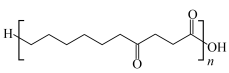 ),写出该反应的化学方程式
),写出该反应的化学方程式
已知i.

ⅱ.C2H2与甲醛反应和苯酚与甲醛反应类型相同,且产物中包含相同种类官能团。
请参照题干合成路线的表示方法,设计以C2H2、HCHO为有机原料(无机原料任选)合成H的路线

您最近一年使用:0次
名校
6 . 实验室研究从医用废感光胶片中回收银的方法。
(1)银的浸出 溶液与
溶液与 溶液直接混合能发生氧化还原反应:
溶液直接混合能发生氧化还原反应:
ii. 。
。
① 溶液将胶片上的单质银转化为
溶液将胶片上的单质银转化为 ,其离子方程式是
,其离子方程式是___________ 。
② 溶液能溶解
溶液能溶解 并得到含
并得到含 的浸出液。结合平衡移动原理解释
的浸出液。结合平衡移动原理解释 溶解的原因:
溶解的原因:___________ 。
Ⅱ.一步法:用水溶解 和乙二胺四乙酸二钠(用
和乙二胺四乙酸二钠(用 表示)的混合固体,调节
表示)的混合固体,调节 形成
形成 溶液,再加入一定量
溶液,再加入一定量 ,配成浸取液。将废感光胶片浸入浸取液中,发生反应:
,配成浸取液。将废感光胶片浸入浸取液中,发生反应:
 。
。
③从物质氧化性或还原性的角度分析加入 的作用:
的作用:___________ 。
(2)银的还原
调节(1)所得浸出液 ,向其中加入
,向其中加入 溶液(B的化合价为
溶液(B的化合价为 )至不再产生黑色沉淀,过滤得到粗银:滤液中的
)至不再产生黑色沉淀,过滤得到粗银:滤液中的 可以循环使用。补全离子方程式:
可以循环使用。补全离子方程式:___________ 。

(3)银浸出率的测定
称取 洗净干燥的原胶片,灼烧灰化后用
洗净干燥的原胶片,灼烧灰化后用 溶解,过滤。滤液用
溶解,过滤。滤液用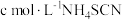 标准溶液滴定至终点,消耗标准溶液
标准溶液滴定至终点,消耗标准溶液 。另取
。另取 洗净干燥的浸取后胶片,用同样方法处理,滴定,消耗
洗净干燥的浸取后胶片,用同样方法处理,滴定,消耗 标准溶液
标准溶液 。(已知:
。(已知: )
)
银的浸出率
___________ (列出计算表达式)。
(1)银的浸出
I、两步法:
 溶液与
溶液与 溶液直接混合能发生氧化还原反应:
溶液直接混合能发生氧化还原反应:ii.
 。
。①
 溶液将胶片上的单质银转化为
溶液将胶片上的单质银转化为 ,其离子方程式是
,其离子方程式是②
 溶液能溶解
溶液能溶解 并得到含
并得到含 的浸出液。结合平衡移动原理解释
的浸出液。结合平衡移动原理解释 溶解的原因:
溶解的原因:Ⅱ.一步法:用水溶解
 和乙二胺四乙酸二钠(用
和乙二胺四乙酸二钠(用 表示)的混合固体,调节
表示)的混合固体,调节 形成
形成 溶液,再加入一定量
溶液,再加入一定量 ,配成浸取液。将废感光胶片浸入浸取液中,发生反应:
,配成浸取液。将废感光胶片浸入浸取液中,发生反应: 。
。③从物质氧化性或还原性的角度分析加入
 的作用:
的作用:(2)银的还原
调节(1)所得浸出液
 ,向其中加入
,向其中加入 溶液(B的化合价为
溶液(B的化合价为 )至不再产生黑色沉淀,过滤得到粗银:滤液中的
)至不再产生黑色沉淀,过滤得到粗银:滤液中的 可以循环使用。补全离子方程式:
可以循环使用。补全离子方程式:
(3)银浸出率的测定
称取
 洗净干燥的原胶片,灼烧灰化后用
洗净干燥的原胶片,灼烧灰化后用 溶解,过滤。滤液用
溶解,过滤。滤液用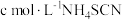 标准溶液滴定至终点,消耗标准溶液
标准溶液滴定至终点,消耗标准溶液 。另取
。另取 洗净干燥的浸取后胶片,用同样方法处理,滴定,消耗
洗净干燥的浸取后胶片,用同样方法处理,滴定,消耗 标准溶液
标准溶液 。(已知:
。(已知: )
)银的浸出率

您最近一年使用:0次
名校
7 . 随着科学的发展,氟及其化合物的用途日益广泛。
I.离子液体具有电导率高、化学稳定性高等优点,在电化学领域用途广泛。某离子液体的结构简式如图。 是制备此离子液体的原料。
是制备此离子液体的原料。
(1)微粒中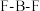 键角:
键角:
___________  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(2) 可以与
可以与 反应生成
反应生成 的原因是
的原因是___________ 。
Ⅱ.氟化镁钾( )是一种具有优良光学性能的材料,其晶胞结构如下。以该晶胞结构为基础,将相似离子取代或部分取代,可合成多种新型材料。
)是一种具有优良光学性能的材料,其晶胞结构如下。以该晶胞结构为基础,将相似离子取代或部分取代,可合成多种新型材料。 晶体中,每个
晶体中,每个 周围有
周围有___________ 个距离最近的F。
(4) 半径与
半径与 接近,将
接近,将 部分由
部分由 取代,可以带来电荷不平衡性和反应活性。从而合成新型催化剂材料。
取代,可以带来电荷不平衡性和反应活性。从而合成新型催化剂材料。
①基态 价电子的轨道表示式为
价电子的轨道表示式为___________ 。
②某实验室合成新型催化剂材料 (
( 是平衡电荷引入的填隙阴离子,不破坏原有晶胞结构)。已知晶胞棱长为
是平衡电荷引入的填隙阴离子,不破坏原有晶胞结构)。已知晶胞棱长为 。若要合成厚度为
。若要合成厚度为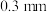 、面积为
、面积为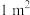 的催化剂材料,理论上需要掺杂的
的催化剂材料,理论上需要掺杂的 约为
约为___________  (
(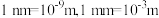 ,阿伏加德罗常数约为
,阿伏加德罗常数约为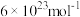 )。
)。
(5)我国科研工作者以 晶体结构为框架,依据“体积匹配原则”合成了具有独特电学性能的
晶体结构为框架,依据“体积匹配原则”合成了具有独特电学性能的 晶体。其框架中的
晶体。其框架中的 由
由 取代,
取代, 位置嵌入有机阳离子
位置嵌入有机阳离子 ,
, 位置沿棱方向嵌入直线型
位置沿棱方向嵌入直线型 。已知
。已知 与
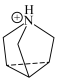
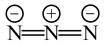
与 的结构简式如下:
的结构简式如下: 中N原子的杂化方式为
中N原子的杂化方式为___________ , 中心N原子的杂化方式为
中心N原子的杂化方式为___________ 。
② 的转动不会影响晶体骨架,这是因为除离子键外,该晶体中微粒间还存在着其他相互作用。如邻近的
的转动不会影响晶体骨架,这是因为除离子键外,该晶体中微粒间还存在着其他相互作用。如邻近的 与
与 还存在着
还存在着___________ ,上述相互作用不会随 的转动改变。
的转动改变。
I.离子液体具有电导率高、化学稳定性高等优点,在电化学领域用途广泛。某离子液体的结构简式如图。
 是制备此离子液体的原料。
是制备此离子液体的原料。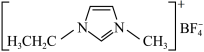
(1)微粒中
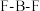 键角:
键角:
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。(2)
 可以与
可以与 反应生成
反应生成 的原因是
的原因是Ⅱ.氟化镁钾(
 )是一种具有优良光学性能的材料,其晶胞结构如下。以该晶胞结构为基础,将相似离子取代或部分取代,可合成多种新型材料。
)是一种具有优良光学性能的材料,其晶胞结构如下。以该晶胞结构为基础,将相似离子取代或部分取代,可合成多种新型材料。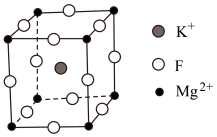
 晶体中,每个
晶体中,每个 周围有
周围有(4)
 半径与
半径与 接近,将
接近,将 部分由
部分由 取代,可以带来电荷不平衡性和反应活性。从而合成新型催化剂材料。
取代,可以带来电荷不平衡性和反应活性。从而合成新型催化剂材料。①基态
 价电子的轨道表示式为
价电子的轨道表示式为②某实验室合成新型催化剂材料
 (
( 是平衡电荷引入的填隙阴离子,不破坏原有晶胞结构)。已知晶胞棱长为
是平衡电荷引入的填隙阴离子,不破坏原有晶胞结构)。已知晶胞棱长为 。若要合成厚度为
。若要合成厚度为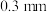 、面积为
、面积为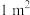 的催化剂材料,理论上需要掺杂的
的催化剂材料,理论上需要掺杂的 约为
约为 (
(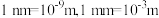 ,阿伏加德罗常数约为
,阿伏加德罗常数约为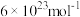 )。
)。(5)我国科研工作者以
 晶体结构为框架,依据“体积匹配原则”合成了具有独特电学性能的
晶体结构为框架,依据“体积匹配原则”合成了具有独特电学性能的 晶体。其框架中的
晶体。其框架中的 由
由 取代,
取代, 位置嵌入有机阳离子
位置嵌入有机阳离子 ,
, 位置沿棱方向嵌入直线型
位置沿棱方向嵌入直线型 。已知
。已知 与
与 的结构简式如下:
的结构简式如下: :
:
 :
:
 中N原子的杂化方式为
中N原子的杂化方式为 中心N原子的杂化方式为
中心N原子的杂化方式为②
 的转动不会影响晶体骨架,这是因为除离子键外,该晶体中微粒间还存在着其他相互作用。如邻近的
的转动不会影响晶体骨架,这是因为除离子键外,该晶体中微粒间还存在着其他相互作用。如邻近的 与
与 还存在着
还存在着 的转动改变。
的转动改变。
您最近一年使用:0次
名校
8 . 具有单双键交替结构的有机分子结构称为共轭体系,有独特的稳定性,如1,3-环己二烯。组成相同、结构相似的共轭烯烃与孤立烯烃分别与等量氢气加成,释放的能量差称为共轭烯烃的稳定化能。已知相关反应的反应热如下:
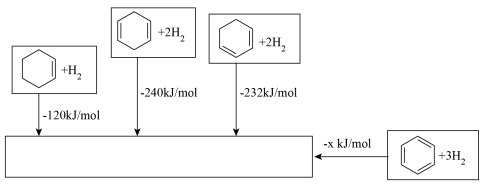
A.标况下 环己烷脱氢获得环己烯的过程将吸收 环己烷脱氢获得环己烯的过程将吸收 的能量 的能量 |
B.1,3-环己二烯的稳定化能为 |
C.1,4-环己二烯与1,3-环己二烯分别与 加成,产物结构一定不同 加成,产物结构一定不同 |
D.综合上述信息推断 |
您最近一年使用:0次
名校
9 . 某同学设计利用废铝箔(除了含 物质,还含少量
物质,还含少量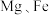 等)制备明矾
等)制备明矾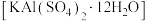 的流程如下图所示。
的流程如下图所示。
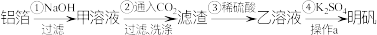
下列说法正确的是
 物质,还含少量
物质,还含少量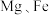 等)制备明矾
等)制备明矾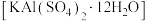 的流程如下图所示。
的流程如下图所示。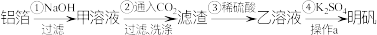
下列说法正确的是
A.①中可能发生的离子反应只有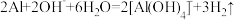 |
| B.该制备流程可以省略步骤②,直接向甲溶液中加入稀硫酸以简化步骤 |
| C.操作a是蒸发结晶,用到的仪器有蒸发皿、酒精灯、玻璃棒等 |
D.步骤④选择加入饱和 溶液以利于明矾生成,可以用平衡移动原理解释 溶液以利于明矾生成,可以用平衡移动原理解释 |
您最近一年使用:0次
名校
10 . 脱除汽车尾气中 和
和 包括以下两个反应:
包括以下两个反应:
①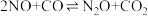
②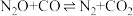
将恒定组成的 和
和 混合气通入不同温度的反应器,相同时间内检测物质浓度,结果如下。
混合气通入不同温度的反应器,相同时间内检测物质浓度,结果如下。 的脱除率
的脱除率
下列分析不正确的是
 和
和 包括以下两个反应:
包括以下两个反应:①
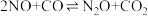
②
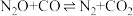
将恒定组成的
 和
和 混合气通入不同温度的反应器,相同时间内检测物质浓度,结果如下。
混合气通入不同温度的反应器,相同时间内检测物质浓度,结果如下。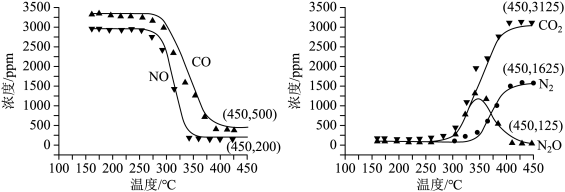
 的脱除率
的脱除率
下列分析不正确的是
A.低温不利于 和 和 的脱除 的脱除 |
B.高温下 和 和 主要脱除反应可以写为: 主要脱除反应可以写为: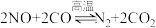 |
C.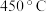 ,该时间段内 ,该时间段内 的脱除率约为 的脱除率约为 |
D.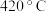 ,该时间段内几乎不发生反应①,主要发生反应② ,该时间段内几乎不发生反应①,主要发生反应② |
您最近一年使用:0次