解题方法
1 . 杭州亚运会主火炬使用了废碳 再生的甲醇
再生的甲醇 作燃料,助力打造碳中和亚运会。甲醇属于
作燃料,助力打造碳中和亚运会。甲醇属于
 再生的甲醇
再生的甲醇 作燃料,助力打造碳中和亚运会。甲醇属于
作燃料,助力打造碳中和亚运会。甲醇属于
| A.有机化合物 | B.高分子 | C.氧化物 | D.混合物 |
您最近一年使用:0次
解题方法
2 . 分析原电池的工作原理,制作简易电池。
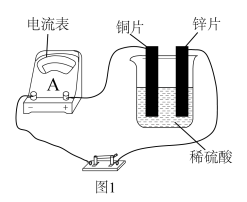
(1)某原电池实验装置如图1所示。_______ (填“铜片”或“锌片”)。
②写出铜片上发生的电极反应:_______ 。
(2)小组同学制作的水果电池如图2所示。_______ (填字母)。
a.水果汁中含有自由移动的离子
b.该装置使氧化反应和还原反应分别在两极进行
②电流表指针偏转,说明该装置实现了化学能向_______ 的转化。
(1)某原电池实验装置如图1所示。
②写出铜片上发生的电极反应:
(2)小组同学制作的水果电池如图2所示。

a.水果汁中含有自由移动的离子
b.该装置使氧化反应和还原反应分别在两极进行
②电流表指针偏转,说明该装置实现了化学能向
您最近一年使用:0次
解题方法
3 . 探究 和
和 的性质,进行如下实验。
的性质,进行如下实验。
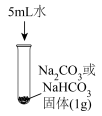
(1)实验Ⅰ, 固体完全溶解,
固体完全溶解, 固体有剩余。相同条件下,在水中的溶解能力:
固体有剩余。相同条件下,在水中的溶解能力:
_______  (填“>”或“<”)。
(填“>”或“<”)。
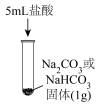
(2)实验Ⅱ,观察到均有气体产生,该气体是_______ 。
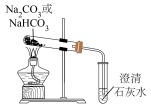
(3)实验Ⅲ,加热 固体,澄清石灰水中无明显变化;加热
固体,澄清石灰水中无明显变化;加热 固体,澄清石灰水变浑浊,写出
固体,澄清石灰水变浑浊,写出 受热分解的化学方程式:
受热分解的化学方程式:_______ 。
(4)下列说法中,正确的是_______ (填字母)。
a.可用盐酸除去 固体中少量的
固体中少量的
b.可用加热的方法鉴别 和
和 两种固体
两种固体
 和
和 的性质,进行如下实验。
的性质,进行如下实验。实验序号 | Ⅰ | Ⅱ | Ⅲ |
实验装置 |
|
|
|
(1)实验Ⅰ,
 固体完全溶解,
固体完全溶解, 固体有剩余。相同条件下,在水中的溶解能力:
固体有剩余。相同条件下,在水中的溶解能力:
 (填“>”或“<”)。
(填“>”或“<”)。(2)实验Ⅱ,观察到均有气体产生,该气体是
(3)实验Ⅲ,加热
 固体,澄清石灰水中无明显变化;加热
固体,澄清石灰水中无明显变化;加热 固体,澄清石灰水变浑浊,写出
固体,澄清石灰水变浑浊,写出 受热分解的化学方程式:
受热分解的化学方程式:(4)下列说法中,正确的是
a.可用盐酸除去
 固体中少量的
固体中少量的
b.可用加热的方法鉴别
 和
和 两种固体
两种固体
您最近一年使用:0次
4 . 乙酸的分子结构模型如下图所示。下列关于乙酸的说法中,不正确 的是
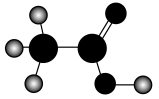
| A.官能团是羧基 | B.由三种元素组成 |
C.结构简式为 | D.分子中的原子之间均以单键结合 |
您最近一年使用:0次
5 . 小组同学探究 与水的反应。
与水的反应。
在注射器中充入 ,然后吸入10mL水,用乳胶管和弹簧夹封住管口,振荡注射器,静置,实验结果如图1所示。一天后,无色气体明显增多,实验结果如图2所示;打开弹簧夹,吸入空气后夹上弹簧夹,无色气体变为红棕色。
,然后吸入10mL水,用乳胶管和弹簧夹封住管口,振荡注射器,静置,实验结果如图1所示。一天后,无色气体明显增多,实验结果如图2所示;打开弹簧夹,吸入空气后夹上弹簧夹,无色气体变为红棕色。_______ 。
(2)进一步探究无色气体增多的原因。
【查阅资料】
ⅰ. 与水反应:
与水反应: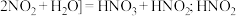 不稳定,分解产生气体。
不稳定,分解产生气体。
ⅱ. 能与KI反应生成
能与KI反应生成 。
。
【提出猜想】溶液A中含有 。
。
【进行实验】
①实验Ⅰ的目的是_______ 。
②实验Ⅱ中选择 溶液的依据是
溶液的依据是_______ (填字母)。
a. 具有氧化性,
具有氧化性, 具有还原性
具有还原性
b. 溶液有颜色,反应前后溶液颜色有变化
溶液有颜色,反应前后溶液颜色有变化
③甲同学认为,实验Ⅲ不能证明溶液A中含有 ,理由是
,理由是_______ 。
【实验反思】
本实验条件下, 与水反应生成了
与水反应生成了 ;
; 分解产生气体,且速率较小。
分解产生气体,且速率较小。
 与水的反应。
与水的反应。在注射器中充入
 ,然后吸入10mL水,用乳胶管和弹簧夹封住管口,振荡注射器,静置,实验结果如图1所示。一天后,无色气体明显增多,实验结果如图2所示;打开弹簧夹,吸入空气后夹上弹簧夹,无色气体变为红棕色。
,然后吸入10mL水,用乳胶管和弹簧夹封住管口,振荡注射器,静置,实验结果如图1所示。一天后,无色气体明显增多,实验结果如图2所示;打开弹簧夹,吸入空气后夹上弹簧夹,无色气体变为红棕色。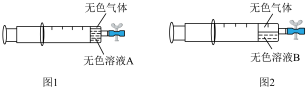
(2)进一步探究无色气体增多的原因。
【查阅资料】
ⅰ.
 与水反应:
与水反应: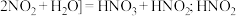 不稳定,分解产生气体。
不稳定,分解产生气体。ⅱ.
 能与KI反应生成
能与KI反应生成 。
。【提出猜想】溶液A中含有
 。
。【进行实验】
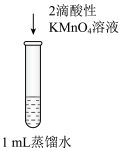
实验序号 | Ⅰ | Ⅱ | Ⅲ |
实验操作 |
|
|
|
实验现象 | 液体颜色变为浅红色 | 溶液颜色仍为无色 | 溶液颜色变为蓝色 |
②实验Ⅱ中选择
 溶液的依据是
溶液的依据是a.
 具有氧化性,
具有氧化性, 具有还原性
具有还原性b.
 溶液有颜色,反应前后溶液颜色有变化
溶液有颜色,反应前后溶液颜色有变化③甲同学认为,实验Ⅲ不能证明溶液A中含有
 ,理由是
,理由是【实验反思】
本实验条件下,
 与水反应生成了
与水反应生成了 ;
; 分解产生气体,且速率较小。
分解产生气体,且速率较小。
您最近一年使用:0次
6 . 一条技术路线可将氯化铵分解实现产物的有效分离,其物质转化关系如下。不正确 的是
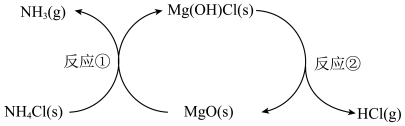
| A.反应①属于氧化还原反应 |
| B.反应②生成MgO和HCl的物质的量之比为1∶1 |
C.该转化的总反应为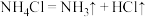 |
D.直接加热 得到的产物难以分离,温度降低又结合成 得到的产物难以分离,温度降低又结合成 |
您最近一年使用:0次
7 . 从海带浸泡液(碘元素主要以 存在)中获取
存在)中获取 ,含碘物质的转化过程如下。
,含碘物质的转化过程如下。 的作用为
的作用为_______ (填“氧化剂”或“还原剂”)。
(2)为提高①的化学反应速率,可采取的措施是_______ (写出一条即可)。
(3)补全②的离子方程式:_______ 。
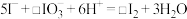
(4)②中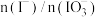 和pH对碘离子的氧化率的影响如下图所示。
和pH对碘离子的氧化率的影响如下图所示。
分析图中信息,选择最佳条件:_______ 。
 存在)中获取
存在)中获取 ,含碘物质的转化过程如下。
,含碘物质的转化过程如下。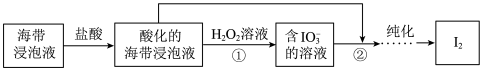
 的作用为
的作用为(2)为提高①的化学反应速率,可采取的措施是
(3)补全②的离子方程式:
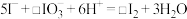
(4)②中
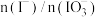 和pH对碘离子的氧化率的影响如下图所示。
和pH对碘离子的氧化率的影响如下图所示。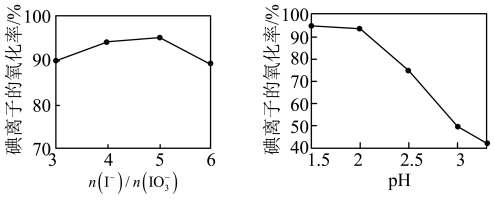
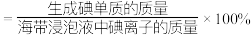
分析图中信息,选择最佳条件:
您最近一年使用:0次
解题方法
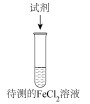
8 . 为检验 溶液是否变质,设计并完成如下实验。其中能说明
溶液是否变质,设计并完成如下实验。其中能说明 溶液变质的是
溶液变质的是
 溶液是否变质,设计并完成如下实验。其中能说明
溶液是否变质,设计并完成如下实验。其中能说明 溶液变质的是
溶液变质的是| 选项 | 实验操作及现象 | 实验装置 |
| A | 滴入 溶液,产生白色沉淀 溶液,产生白色沉淀 |
|
| B | 滴入KSCN溶液,溶液变为红色 | |
| C | 先滴入氯水,再滴入KSCN溶液,溶液变为红色 | |
| D | 滴入NaOH溶液,生成白色絮状沉淀,沉淀迅速变成灰绿色,最终变成红褐色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
9 . 补齐物质与其用途之间的连线_______ 。
| 物质 用途 A.乙酸――――――a.清除水垢 B.氧化铁 b.作供氧剂 C.次氯酸钠 c.作红色颜料 D.过氧化钠 d.作消毒剂 |
您最近一年使用:0次
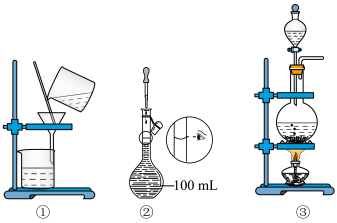
10 . 选择完成下列实验的装置。 浓盐酸的混合物制
浓盐酸的混合物制 ,选用
,选用_______ (填序号,下同)。
(2)用 溶液和
溶液和 制取
制取 后,若回收
后,若回收 选用
选用_______ 。
(3)配制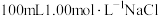 溶液,选用
溶液,选用_______ 。
 浓盐酸的混合物制
浓盐酸的混合物制 ,选用
,选用(2)用
 溶液和
溶液和 制取
制取 后,若回收
后,若回收 选用
选用(3)配制
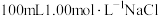 溶液,选用
溶液,选用
您最近一年使用:0次