名校
解题方法
1 . AlN新型材料应用前景广泛,其制备与性质研究成为热点。
相关数据如下:
(1)AlN的制备。
① 化学气相沉积法。
Ⅰ.一定温度下,以AlCl3气体和NH3为原料制备AlN,反应的化学方程式是____________________ 。
Ⅱ.上述反应适宜的温度范围是______ ℃(填字母)。
a.75~100 b.600~1100 c.2000~2300
② 铝粉直接氮化法。
Al与N2可直接化合为AlN固体,AlN能将Al包裹,反应难以继续进行。控制温度,在Al粉中均匀掺入适量Mg粉,可使Al几乎全部转化为AlN固体。该过程发生的反应有:__________________ 、_________ 和2Al + N2  2AlN。
2AlN。
③碳热还原法。
以Al2O3、C(石墨)和N2为原料,在高温下制备AlN。
已知:ⅰ. 2Al2O3(s) ⇌ 4Al(g) + 3O2(g) ∆H 1 =+3351 kJ·mol-1
ⅱ. 2C(石墨,s) + O2(g) = 2CO(g) ∆H 2 =-221 kJ·mol-1
ⅲ. 2Al(g) + N2(g) = 2AlN(s) ∆H 3 =-318 kJ·mol-1
运用平衡移动原理分析反应ⅱ对反应ⅰ的可能影响:______________________________________ 。
(2)AlN的性质。AlN粉末可发生水解。相同条件下,不同粒径的AlN粉末水解时溶液pH的变化如图所示。
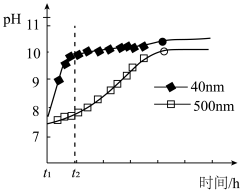
① AlN粉末水解的化学方程式是____________________________________ 。
② 解释t1-t2时间内两条曲线差异的可能原因:_______________________________ 。
(3)AlN含量检测。向a g AlN样品中加入足量浓NaOH溶液,然后通入水蒸气将NH3全部蒸出,将NH3用过量的v1 mL c1 mol·L-1 H2SO4溶液吸收完全,剩余的H2SO4用v2 mL c2 mol·L-1 NaOH溶液恰好中和,则样品中AlN的质量分数是________________________________ 。
相关数据如下:
| 物质 | 熔点/℃ | 沸点/℃ | 与N2反应温度/℃ | 相应化合物分解温度/℃ |
| Al | 660 | 2467 | >800 | AlN:>2000 (>1400升华) AlCl3:(>181升华) |
| Mg | 649 | 1090 | >300 | Mg3N2:>800 |
① 化学气相沉积法。
Ⅰ.一定温度下,以AlCl3气体和NH3为原料制备AlN,反应的化学方程式是
Ⅱ.上述反应适宜的温度范围是
a.75~100 b.600~1100 c.2000~2300
② 铝粉直接氮化法。
Al与N2可直接化合为AlN固体,AlN能将Al包裹,反应难以继续进行。控制温度,在Al粉中均匀掺入适量Mg粉,可使Al几乎全部转化为AlN固体。该过程发生的反应有:
 2AlN。
2AlN。③碳热还原法。
以Al2O3、C(石墨)和N2为原料,在高温下制备AlN。
已知:ⅰ. 2Al2O3(s) ⇌ 4Al(g) + 3O2(g) ∆H 1 =+3351 kJ·mol-1
ⅱ. 2C(石墨,s) + O2(g) = 2CO(g) ∆H 2 =-221 kJ·mol-1
ⅲ. 2Al(g) + N2(g) = 2AlN(s) ∆H 3 =-318 kJ·mol-1
运用平衡移动原理分析反应ⅱ对反应ⅰ的可能影响:
(2)AlN的性质。AlN粉末可发生水解。相同条件下,不同粒径的AlN粉末水解时溶液pH的变化如图所示。

① AlN粉末水解的化学方程式是
② 解释t1-t2时间内两条曲线差异的可能原因:
(3)AlN含量检测。向a g AlN样品中加入足量浓NaOH溶液,然后通入水蒸气将NH3全部蒸出,将NH3用过量的v1 mL c1 mol·L-1 H2SO4溶液吸收完全,剩余的H2SO4用v2 mL c2 mol·L-1 NaOH溶液恰好中和,则样品中AlN的质量分数是
您最近一年使用:0次
2020-01-23更新
|
326次组卷
|
4卷引用:北京市2020普通高中学业水平考试等级性抽样测试化学试题
2 . 阅读短文,回答问题。
氢是宇宙中最轻的元素,同时也是宇宙中含量最多的元素。
氢气蕴含的能量非常高,燃烧氢气释放的能量是相同质量化石燃料的3倍左右。地球上的氢元素主要以水的形式存在,氢气可以由水制取,原料充足。氢气燃烧后的产物是水,绿色环保。
氢能源可以广泛应用在交通运输、发电等领域,被视为21世纪最具发展潜力的清洁能源。除此之外,氢气也是多个化工领域的原料。但是,氢气在制备、存储、运输等环节还存在一些有待解决的问题。科学家预测,一旦氢能实现产业化,我们的生活也将随之发生巨大变化。
(1)氢是宇宙中最轻、含量最多的元素。(___________)
(2)燃烧相同质量的氢气和化石燃料,氢气释放的能量少。(___________)
(3)制取氢气的原料充足,氢气燃烧后的产物是水,绿色环保。(___________)
(4)氢能源可以广泛应用在交通运输、发电等领域。(___________)
氢是宇宙中最轻的元素,同时也是宇宙中含量最多的元素。
氢气蕴含的能量非常高,燃烧氢气释放的能量是相同质量化石燃料的3倍左右。地球上的氢元素主要以水的形式存在,氢气可以由水制取,原料充足。氢气燃烧后的产物是水,绿色环保。
氢能源可以广泛应用在交通运输、发电等领域,被视为21世纪最具发展潜力的清洁能源。除此之外,氢气也是多个化工领域的原料。但是,氢气在制备、存储、运输等环节还存在一些有待解决的问题。科学家预测,一旦氢能实现产业化,我们的生活也将随之发生巨大变化。

(1)氢是宇宙中最轻、含量最多的元素。(___________)
(2)燃烧相同质量的氢气和化石燃料,氢气释放的能量少。(___________)
(3)制取氢气的原料充足,氢气燃烧后的产物是水,绿色环保。(___________)
(4)氢能源可以广泛应用在交通运输、发电等领域。(___________)
您最近一年使用:0次
2024-03-06更新
|
32次组卷
|
2卷引用:2023年北京市第二次普通高中学业水平测试高一下学期化学试题
名校
解题方法
3 . 氮元素在海洋中的循环,是整个海洋生态系统的基础和关键。海洋中无机氮的循环过程可用如图表示,下列关于海洋氮循环的说法中正确的是
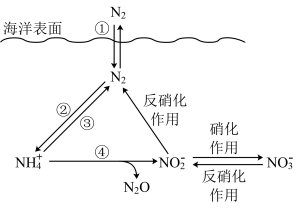
| A.海洋中不存在游离态的氮 |
| B.②中的含氮物质转化属于氮的固定 |
| C.④中的含氮物质转化属于氮的还原 |
D.向海洋中排放含 的废水不会影响 的废水不会影响 的含量 的含量 |
您最近一年使用:0次
2021-08-03更新
|
1158次组卷
|
21卷引用:北京市海淀区2018-2019学年高一学业水平合格性考试适应练习化学试题
北京市海淀区2018-2019学年高一学业水平合格性考试适应练习化学试题北京市海淀区首师大附属育新学校中部2019-2020学年高一下学期期末考试化学试题北京市平谷区2019-2020学年高一下学期期末质量检测化学试题北京市育才学校2023-2024学年高一下学期3月月考化学(合格考)试题江西省南昌市八一中学2019-2020学年高一下学期期中考试化学试题辽宁省大连市旅顺口区2019-2020学年高一下学期期末考试化学试题辽宁省大连市2019-2020学年高一下学期期末考试化学试题(已下线)第12讲 氮及其化合物-2021年高考化学一轮复习名师精讲练山西省大同一中2019-2020学年高一下学期6月月考化学试题辽宁省六校协作体2020-2021学年高二上学期期初考试化学试题人教版2019必修第二册 第五章 第二节 第1课时 氮气与氮的固定 一氧化氮和二氧化氮福建省福州第三中学2020-2021学年高一下学期期中考化学试题四川省达州市2019-2020学年高一下学期期末检测化学试题(已下线)《新教材变化解读及考法剖析 》—第五章 化工生产中的重要非金属元素(人教版2019必修第二册)黑龙江省西北部八校2021-2022学年高一下学期期中联考化学试题湖北省竹溪县第二高级中学2021-2022学年高一下学期第一次月考化学试题安徽省合肥市第一中学2022-2023学年高一下学期第一次月考化学试题7.1.2自然固氮(课中)-2019苏教版必修2课前课中课后7.1.2自然固氮(课后)-2019苏教版必修2课前课中课后7.1.3人工固氮(课后)-2019苏教版必修2课前课中课后云南省曲靖市第一中学2022-2023学年高一下学期期末考试化学试题
4 . 某同学在学习元素化合物知识的过程中,发现含有相同元素的物质间在一定条件下存在转化规律。含甲元素的部分物质可发生如下转化。

其中,A、B、C中甲元素的化合价依次升高;B,C为同类物质,且所含元素种类相同。请回答:
(1)若A是空气中含量最多的气体,C为红棕色气体。
①甲元素在元素周期表中的位置是______ 。
②下列说法正确的是______ (填字母)。
(2)若A为金属单质,C溶液遇KSCN溶液呈红色,F为黄绿色气体。
①B溶液与F反应的离子方程式是______ 。
②当5.6gA全部转化为D时,转移电子的物质的量为______ mol。

其中,A、B、C中甲元素的化合价依次升高;B,C为同类物质,且所含元素种类相同。请回答:
(1)若A是空气中含量最多的气体,C为红棕色气体。
①甲元素在元素周期表中的位置是
②下列说法正确的是
a.E、F可为氧气 b.常温下,B可为无色气体 c.③中甲元素的化合价发生了变化
(2)若A为金属单质,C溶液遇KSCN溶液呈红色,F为黄绿色气体。
①B溶液与F反应的离子方程式是
②当5.6gA全部转化为D时,转移电子的物质的量为
您最近一年使用:0次
解题方法
5 . 明矾石是一种硫酸盐矿物,其主要成分是K2SO4·Al2(SO4)3·2Al2O3·6H2O,还含有杂质Fe2O3。某研究小组用明矾石制取Al(OH)3和氮钾复合肥,设计了如图流程。

请回答:
(1)①②所涉及的实验操作方法中,属于过滤的是__ (填序号)。
(2)①中发生反应的离子方程式是___ 。
(3)下列说法正确的是__ (填字母)。
a.试剂1为NaOH溶液或氨水
b.溶液1中含有的阳离子主要是K+、NH
c.②中发生的反应属于氧化还原反应
(4)为测定氮钾复合肥中钾元素含量,设计如下实验方案:将ag氮钾复合肥溶于水,加入足量X溶液,产生白色沉淀,经过滤、洗涤、干燥,得到bg固体,其中X是__ 。

请回答:
(1)①②所涉及的实验操作方法中,属于过滤的是
(2)①中发生反应的离子方程式是
(3)下列说法正确的是
a.试剂1为NaOH溶液或氨水
b.溶液1中含有的阳离子主要是K+、NH

c.②中发生的反应属于氧化还原反应
(4)为测定氮钾复合肥中钾元素含量,设计如下实验方案:将ag氮钾复合肥溶于水,加入足量X溶液,产生白色沉淀,经过滤、洗涤、干燥,得到bg固体,其中X是
您最近一年使用:0次
6 . 某同学在学习元素化合物知识的过程中,发现含有相同元素的物质间在一定条件下存在转化规律,绘制出如图转化关系图,图中A、B、C、D是由短周期元素组成的物质。并用于研究的性质及其变化。

请回答:
(1)若A为单质,其焰色试验为黄色,C为淡黄色固体。
①组成A的元素在周期表中的位置是___ 。
②下列说法正确的是___ (填字母)。
a.A可经一步反应转化为D
b.B、C均可作呼吸面具的供氧剂
c.B、C、D均可与CO2反应
(2)若A为能使红色石蕊试纸变蓝的气体,C为红棕色气体。
①A→B反应的化学方程式是__ 。
②A与C反应生成E和水,E是空气中含量最多的气体。当生成19.6gE时,转移电子的物质的量为__ mol。

请回答:
(1)若A为单质,其焰色试验为黄色,C为淡黄色固体。
①组成A的元素在周期表中的位置是
②下列说法正确的是
a.A可经一步反应转化为D
b.B、C均可作呼吸面具的供氧剂
c.B、C、D均可与CO2反应
(2)若A为能使红色石蕊试纸变蓝的气体,C为红棕色气体。
①A→B反应的化学方程式是
②A与C反应生成E和水,E是空气中含量最多的气体。当生成19.6gE时,转移电子的物质的量为
您最近一年使用:0次
7 . 太阳能是理想的能源,通过Zn和ZnO的热化学循环可以利用太阳能,其转化关系如图所示。下列说法中,不正确 的是( )
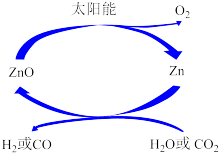

| A.Zn与H2O或者CO2反应时作还原剂 |
| B.利用该过程可以降低环境中CO2的含量 |
| C.利用该过程可以生产氢能源,实现太阳能向化学能的转化 |
| D.该过程需要不断补充Zn才能持续进行 |
您最近一年使用:0次
8 . 某同学采用硫铁矿焙烧后的烧渣(主要成分为Fe2O3、 SiO2、A12O3,不考虑其他杂质)制取绿碱FeSO4・7H2O),设计了如下流程(部分物质已略去)。

请回答:
(1)①一④所涉及的实验操作方法中,包含过滤的有____ (写序号)。
(2)写出①中反应的离子方程式:____ 。
(3)下列说法正确的是___ (填字母)。
a.固体x为铁粉
b.溶液B中含有的阳离子主要是Fe2+、Fe3+、Al3+
c.从溶液C到绿矾的过程中,须控制条件防止其氧化
(4)为测定烧渣中Fe2O3的含量,甲同学通过实验测得如下数据:烧渣的质量为ag,固体x的质量为bg,固体B的质量为cg。乙同学认为仅利用以上数据不能 计算出烧渣中Fe2O3的含量,其理由是____ 。

请回答:
(1)①一④所涉及的实验操作方法中,包含过滤的有
(2)写出①中反应的离子方程式:
(3)下列说法正确的是
a.固体x为铁粉
b.溶液B中含有的阳离子主要是Fe2+、Fe3+、Al3+
c.从溶液C到绿矾的过程中,须控制条件防止其氧化
(4)为测定烧渣中Fe2O3的含量,甲同学通过实验测得如下数据:烧渣的质量为ag,固体x的质量为bg,固体B的质量为cg。乙同学认为仅利用以上数据
您最近一年使用:0次
2019-06-28更新
|
377次组卷
|
2卷引用:北京市2019年普通高中学业水平合格性考试模拟化学试题
名校
9 . 绿矾可用作除草剂、净水剂或抗贫血药等.某研究小组同学采用硫铁矿焙烧后的烧渣(主要成分为Fe2O3、Al2O3和SiO2,不考虑其他杂质)制备绿矾,设计了如下流程.

请回答:
(1)①~③所涉及的实验操作方法中,用到过滤的是__________ (填序号).
(2)③中发生反应的离子方程式是____________________________ .
(3)下列说法正确的是(填字母)_____ .
a.①中可选用盐酸,③中只能用硫酸
b.溶液B中含有OH﹣、SiO32﹣、AlO2﹣等阴离子
c.④中发生了氧化还原反应,固体C做还原剂
(4)原烧渣中Fe2O3的质量分数为_________________ .

请回答:
(1)①~③所涉及的实验操作方法中,用到过滤的是
(2)③中发生反应的离子方程式是
(3)下列说法正确的是(填字母)
a.①中可选用盐酸,③中只能用硫酸
b.溶液B中含有OH﹣、SiO32﹣、AlO2﹣等阴离子
c.④中发生了氧化还原反应,固体C做还原剂
(4)原烧渣中Fe2O3的质量分数为
您最近一年使用:0次
2016-12-09更新
|
346次组卷
|
2卷引用:2016年北京市普通高中学业水平化学试卷
10 . 自然界的硫循环如右图所示,下列说法不正确 的是


| A.大量石油等化石燃料的燃烧导致了酸雨的形成 |
| B.土壤或水体中的SO42-部分来自于降水 |
| C.火山喷发不会增加大气中SO2的含量 |
| D.含硫有机物和含硫无机物可相互转化 |
您最近一年使用:0次



