名校
解题方法
1 . 工业上以辉铋矿粉(主要成分是 ,含少量
,含少量 、
、 、
、 等杂质)为原料制备
等杂质)为原料制备 (铋酸钠,浅黄色不溶于冷水的固体,是常用试剂),流程如下:
(铋酸钠,浅黄色不溶于冷水的固体,是常用试剂),流程如下: 难溶于水;
难溶于水;
②酸浸后,矿粉中的硫元素完全变为硫单质;
回答下列问题:
(1) 中Cu的化合价为
中Cu的化合价为___________ ,酸浸过程中, 反应的离子方程式
反应的离子方程式___________ 。
(2)检验“酸浸”液中是否含 ,可选择
,可选择 溶液。能证明不存在
溶液。能证明不存在 的实验现象是
的实验现象是___________ 。
(3)氧化后,从反应体系中分离出 粗产品的操作名称是
粗产品的操作名称是___________ 。
(4)上述流程中,基态原子未成对电子数最多的金属元素名称是___________ 。
(5)向 和
和 混合溶液中通入氯气制备
混合溶液中通入氯气制备 的离子方程式
的离子方程式___________ 。
(6)已知常温下, ,调节FeCl3溶液至
,调节FeCl3溶液至 ,所得溶液中c(Fe3+)=
,所得溶液中c(Fe3+)=___________ 。
 ,含少量
,含少量 、
、 、
、 等杂质)为原料制备
等杂质)为原料制备 (铋酸钠,浅黄色不溶于冷水的固体,是常用试剂),流程如下:
(铋酸钠,浅黄色不溶于冷水的固体,是常用试剂),流程如下: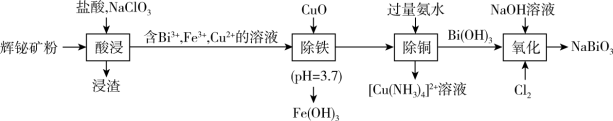
 难溶于水;
难溶于水;②酸浸后,矿粉中的硫元素完全变为硫单质;
回答下列问题:
(1)
 中Cu的化合价为
中Cu的化合价为 反应的离子方程式
反应的离子方程式(2)检验“酸浸”液中是否含
 ,可选择
,可选择 溶液。能证明不存在
溶液。能证明不存在 的实验现象是
的实验现象是(3)氧化后,从反应体系中分离出
 粗产品的操作名称是
粗产品的操作名称是(4)上述流程中,基态原子未成对电子数最多的金属元素名称是
(5)向
 和
和 混合溶液中通入氯气制备
混合溶液中通入氯气制备 的离子方程式
的离子方程式(6)已知常温下,
 ,调节FeCl3溶液至
,调节FeCl3溶液至 ,所得溶液中c(Fe3+)=
,所得溶液中c(Fe3+)=
您最近半年使用:0次
2 . “科学探究与创新意识”是化学学科核心素养之一、某研究小组用下图装置进行探究实验。下列说法正确的是
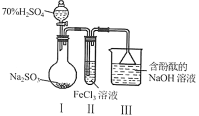
A.Ⅰ中70% 在反应中作氧化剂 在反应中作氧化剂 |
B.取少量反应后Ⅱ中溶液加入 溶液有蓝色沉淀生成 溶液有蓝色沉淀生成 |
C.Ⅱ中发生反应的离子方程式为: |
D.Ⅲ中溶液褪色,说明 具有漂白性 具有漂白性 |
您最近半年使用:0次
解题方法
3 . 铁是人类应用较早,当前应用量最大的金属元素。下列有关铁及其化合物的说法正确的是
A.将 浓溶液滴加到饱和的 浓溶液滴加到饱和的 溶液中,制备 溶液中,制备 胶体 胶体 |
B. 溶液腐蚀 溶液腐蚀 刻制印刷电路板,说明铁比铜金属性强 刻制印刷电路板,说明铁比铜金属性强 |
C.用酸性 溶液检验 溶液检验 溶液中是否含有 溶液中是否含有 |
D. 在高温下和水蒸气反应、 在高温下和水蒸气反应、 在空气中受热均能得到 在空气中受热均能得到 |
您最近半年使用:0次
4 . Ⅰ.某小组利用数字化实验模拟制备Fe(OH)2并探究其相关性质。
(1)模拟制备Fe(OH)2装置如图:打开右瓶上方空气过滤器的气阀(平衡压强,便于FeSO4溶液能够进入右瓶);然后,依次打开鲁尔阀、推动注射器,将注射器中的FeSO4溶液加入左瓶的溶液中,促使左瓶中的FeSO4溶液流入右瓶;当右瓶中明显有白色沉淀生成时,停止加液,依次关闭鲁尔阀、关闭右瓶上方的空气过滤器的气阀、打开左瓶上方的空气过滤器的气阀。实验证明制备Fe(OH)2最佳pH是6~8,氨水代替NaOH溶液效果更好的原因是_____ ,Na2SO3的作用是_____ 。
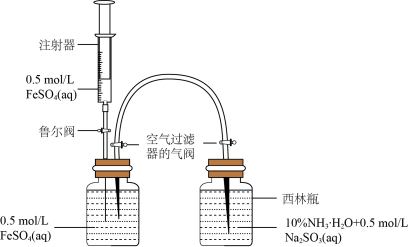
(2)探究原材料FeSO4的相关性质。向50mL蒸馏水中加入FeSO4·7H2O晶体搅拌以加快溶解,用溶解氧传感器测定液体中溶解氧浓度随时间的变化, 点时加入NaOH溶液所得曲线如图。
点时加入NaOH溶液所得曲线如图。

对比ab、bc段溶解氧的消耗速率,可以得出什么结论_____ 。
(3)已知:在 时溶液中,
时溶液中, 被氧化成
被氧化成 的过程中会产生
的过程中会产生 ,且
,且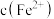 降低量大于
降低量大于 增加量,
增加量, 几乎不变,用总离子方程式说明原因
几乎不变,用总离子方程式说明原因_____ ,检验反应后的溶液中是否存在 ,可以选择的试剂是
,可以选择的试剂是_____ 。
A.NaOH溶液 B.K3[Fe(CN)6] C.KSCN D.KMnO4
Ⅱ.
(4)用氢氧化钠固体配制实验所需的NaOH溶液,下列图示对应的操作规范的是_____
(5)用NaOH固体配制实验所需的NaOH溶液时,下列操作会导致所配溶液浓度偏高的是_____ 。
A.未冷却至室温就定容
B.容量瓶用蒸馏水洗净后未干燥
C.定容时俯视读取刻度
D.定容时液面超过了刻度线,并将多余溶液吸出
E.称量NaOH时用了生锈的砝码
(1)模拟制备Fe(OH)2装置如图:打开右瓶上方空气过滤器的气阀(平衡压强,便于FeSO4溶液能够进入右瓶);然后,依次打开鲁尔阀、推动注射器,将注射器中的FeSO4溶液加入左瓶的溶液中,促使左瓶中的FeSO4溶液流入右瓶;当右瓶中明显有白色沉淀生成时,停止加液,依次关闭鲁尔阀、关闭右瓶上方的空气过滤器的气阀、打开左瓶上方的空气过滤器的气阀。实验证明制备Fe(OH)2最佳pH是6~8,氨水代替NaOH溶液效果更好的原因是

(2)探究原材料FeSO4的相关性质。向50mL蒸馏水中加入FeSO4·7H2O晶体搅拌以加快溶解,用溶解氧传感器测定液体中溶解氧浓度随时间的变化,
 点时加入NaOH溶液所得曲线如图。
点时加入NaOH溶液所得曲线如图。
对比ab、bc段溶解氧的消耗速率,可以得出什么结论
(3)已知:在
 时溶液中,
时溶液中, 被氧化成
被氧化成 的过程中会产生
的过程中会产生 ,且
,且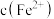 降低量大于
降低量大于 增加量,
增加量, 几乎不变,用总离子方程式说明原因
几乎不变,用总离子方程式说明原因 ,可以选择的试剂是
,可以选择的试剂是A.NaOH溶液 B.K3[Fe(CN)6] C.KSCN D.KMnO4
Ⅱ.
(4)用氢氧化钠固体配制实验所需的NaOH溶液,下列图示对应的操作规范的是_____
 |  | 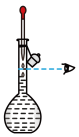 | 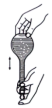 |
| A.称量 | B.转移 | C、定容 | D、摇匀 |
| A.A | B.B | C.C | D.D |
(5)用NaOH固体配制实验所需的NaOH溶液时,下列操作会导致所配溶液浓度偏高的是
A.未冷却至室温就定容
B.容量瓶用蒸馏水洗净后未干燥
C.定容时俯视读取刻度
D.定容时液面超过了刻度线,并将多余溶液吸出
E.称量NaOH时用了生锈的砝码
您最近半年使用:0次
解题方法
5 . 部分含Fe物质的分类与相应化合价的关系如图所示。下列推断不合理的是

| A.可存在a→e→b的转化 | B.e溶液可与KSCN溶液反应生成红色沉淀 |
| C.能用a制作的容器运输浓硫酸 | D.a可与稀硝酸恰好反应,生成只含b的溶液 |
您最近半年使用:0次
6 . I.某实验小组采用下列实验探究外界条件对化学反应速率及其化学平衡的影响。
(1)室温下,向盛有 溶液的试管中加入
溶液的试管中加入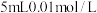 的
的 溶液,溶液变为
溶液,溶液变为_________ 色。发生反应的离子方程式为____________________________________________________ 。
(2)现将上述溶液均分为两份置于甲、乙两支试管中;
①向甲试管中加入4滴饱和 溶液,平衡
溶液,平衡______ (填“正向移动”、“逆向移动”或“不移动”);溶液中的 浓度
浓度
______ (填“增大”、“减小”或“不变”,下同),重新达到平衡时 转化率
转化率______ 。
②向乙试管中加入 固体,平衡
固体,平衡______ (填“正向移动”、“逆向移动”或“不移动”)。
II.该实验小组还利用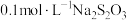 溶液和
溶液和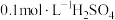 溶液为反应物,探究外界条件对化学反应速率的影响,实验记录如表。请结合表中信息,回答有关问题:
溶液为反应物,探究外界条件对化学反应速率的影响,实验记录如表。请结合表中信息,回答有关问题:
(3)该反应的离子方程式为____________________________________________ 。
(4)在比较某一因素对实验产生的影响时,必须排除其他因素的变动和干扰,即需要控制好与实验有关的各项反应条件,其中:
①能说明温度对该反应速率影响的组合是______ (填实验序号,下同);
②实验Ⅱ和Ⅲ探究的是_______ (填外部因素)对化学反应速率的影响,其中实验Ⅲ中 =
=_______ 。
(1)室温下,向盛有
 溶液的试管中加入
溶液的试管中加入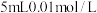 的
的 溶液,溶液变为
溶液,溶液变为(2)现将上述溶液均分为两份置于甲、乙两支试管中;
①向甲试管中加入4滴饱和
 溶液,平衡
溶液,平衡 浓度
浓度
 转化率
转化率②向乙试管中加入
 固体,平衡
固体,平衡II.该实验小组还利用
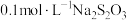 溶液和
溶液和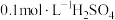 溶液为反应物,探究外界条件对化学反应速率的影响,实验记录如表。请结合表中信息,回答有关问题:
溶液为反应物,探究外界条件对化学反应速率的影响,实验记录如表。请结合表中信息,回答有关问题:实验序号 | 反应温度 |
|
|
| 出现沉淀所需的时间 |
I | 0℃ | 5mL | 5mL | 10mL | 12s |
II | 30℃ | 5mL | 10mL | 5mL | 8s |
III | 30℃ | 5mL | 7mL |
| 10s |
IV | 30℃ | 5mL | 5mL | 10mL | 10s |
(4)在比较某一因素对实验产生的影响时,必须排除其他因素的变动和干扰,即需要控制好与实验有关的各项反应条件,其中:
①能说明温度对该反应速率影响的组合是
②实验Ⅱ和Ⅲ探究的是
 =
=
您最近半年使用:0次
名校
7 . 根据要求完成下列填空。
(1)画出氯原子结构示意图______ 。
(2)写出氨气和氢氧化钠的电子式:氨气_______ ,氢氧化钠______ 。
(3)写出氯化铁和铁反应的离子方程式_________ 。
(4)除去 固体中混入的
固体中混入的 杂质最佳方法是
杂质最佳方法是____ ,化学方程式为________ 。
(1)画出氯原子结构示意图
(2)写出氨气和氢氧化钠的电子式:氨气
(3)写出氯化铁和铁反应的离子方程式
(4)除去
 固体中混入的
固体中混入的 杂质最佳方法是
杂质最佳方法是
您最近半年使用:0次
名校
解题方法
8 . 某变质的废铜屑主要成分为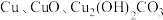 (其他杂质不参加化学反应),为将其转化为铜单质,同时制备绿矾,某实验小组设计如图所示流程。下列说法错误的是
(其他杂质不参加化学反应),为将其转化为铜单质,同时制备绿矾,某实验小组设计如图所示流程。下列说法错误的是

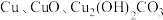 (其他杂质不参加化学反应),为将其转化为铜单质,同时制备绿矾,某实验小组设计如图所示流程。下列说法错误的是
(其他杂质不参加化学反应),为将其转化为铜单质,同时制备绿矾,某实验小组设计如图所示流程。下列说法错误的是
A.基态铜原子的价层电子排布式为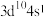 |
B.滤液1的溶质主要成分为 |
C.若分铜过程生成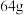 铜,则浸泡过程理论上有 铜,则浸泡过程理论上有 电子转移 电子转移 |
D.可用铁氰化钾溶液检验滤液2中 的存在 的存在 |
您最近半年使用:0次
解题方法
9 . 下列过程中的化学反应,相应的离子方程式错误的是
A. 加入水中: 加入水中: |
B.用碳酸钠溶液处理水垢中的硫酸钙: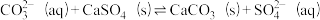 |
C.电解精炼铜的阳极电极反应式: |
D. 溶液滴入 溶液滴入 溶液中: 溶液中: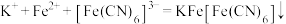 |
您最近半年使用:0次
解题方法
10 . 化学技术在铁材料研发改进方面发挥着重要作用。
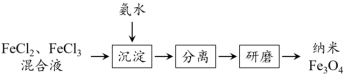
I.纳米 是一种多功能磁性材料,在高科技领域有特殊的用途,工业上可通过如下过程制得:
是一种多功能磁性材料,在高科技领域有特殊的用途,工业上可通过如下过程制得:
(1)在实验室中,同学们做了如下实验:
①将红热铁丝伸到盛有氯气的集气瓶中制 ,反应的化学方程式为
,反应的化学方程式为___________ 。
②将 通入
通入 溶液制
溶液制 ,观察到的实验现象为
,观察到的实验现象为___________ 。
③将 溶液滴入
溶液滴入 溶液中,观察到产生白色絮状沉淀迅速变为灰绿色,最后转成红褐色。白色和红褐色沉淀的成分分别是
溶液中,观察到产生白色絮状沉淀迅速变为灰绿色,最后转成红褐色。白色和红褐色沉淀的成分分别是___________ 、___________ (填化学式)。
(2)流程中,产生“沉淀”的离子方程式为:___________
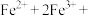 ___________
___________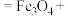 ___________
___________ ___________
___________
(3)同学们认为 和
和 的混合溶液中
的混合溶液中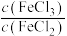 应略小于2,原因是
应略小于2,原因是___________ 。
Ⅱ.某同学查阅资料得知还可以用纳米铁粉与水蒸气反应制得纳米 。
。
(4)纳米铁粉___________ (填“属于”或“不属于”)胶体。
(5)该同学设计了以下方案证明产物为 。
。
①完善表格:ii___________ ;iii___________ 。
②有同学认为该方案不能证明产物为 ,其理由是
,其理由是___________ 。
I.纳米
 是一种多功能磁性材料,在高科技领域有特殊的用途,工业上可通过如下过程制得:
是一种多功能磁性材料,在高科技领域有特殊的用途,工业上可通过如下过程制得:
(1)在实验室中,同学们做了如下实验:
①将红热铁丝伸到盛有氯气的集气瓶中制
 ,反应的化学方程式为
,反应的化学方程式为②将
 通入
通入 溶液制
溶液制 ,观察到的实验现象为
,观察到的实验现象为③将
 溶液滴入
溶液滴入 溶液中,观察到产生白色絮状沉淀迅速变为灰绿色,最后转成红褐色。白色和红褐色沉淀的成分分别是
溶液中,观察到产生白色絮状沉淀迅速变为灰绿色,最后转成红褐色。白色和红褐色沉淀的成分分别是(2)流程中,产生“沉淀”的离子方程式为:
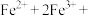 ___________
___________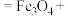 ___________
___________ ___________
___________
(3)同学们认为
 和
和 的混合溶液中
的混合溶液中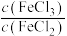 应略小于2,原因是
应略小于2,原因是Ⅱ.某同学查阅资料得知还可以用纳米铁粉与水蒸气反应制得纳米
 。
。(4)纳米铁粉
(5)该同学设计了以下方案证明产物为
 。
。| 编号 | 实验方案 | 实验现象 | 实验结论 | |
| ⅰ | 取反应后的固体,加稀硫酸充分振荡溶解 | / | / | |
| ⅱ | 向 溶液中滴加 溶液中滴加 所得溶液 所得溶液 | ___________ | 溶液中含 | 产物为 |
| ⅲ | 取i所得溶液,滴加___________溶液 | 溶液变血红色 | 溶液中含 | |
②有同学认为该方案不能证明产物为
 ,其理由是
,其理由是
您最近半年使用:0次