名校
解题方法
1 . 下列物质中,与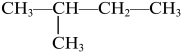 互为同分异构体的是
互为同分异构体的是
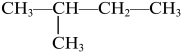 互为同分异构体的是
互为同分异构体的是A. | B.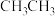 | C. | D.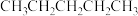 |
您最近一年使用:0次
2023-07-11更新
|
410次组卷
|
9卷引用:北京市2021-2022学年高三年级下学期合格考(第一次)化学试题
解题方法
2 . 选择完成下列实验的装置。

(1)除去粗盐水中的泥沙,用_______ (填序号,下同)。
(2)配制100 mL 1.00 mol·L−1 NaCl溶液,用_______ 。
(3)加热MnO2和浓盐酸的混合物制Cl2,用_______ 。

(1)除去粗盐水中的泥沙,用
(2)配制100 mL 1.00 mol·L−1 NaCl溶液,用
(3)加热MnO2和浓盐酸的混合物制Cl2,用
您最近一年使用:0次
3 . 补齐物质与其用途之间的连线_______ 。
| 物质 | 用途 |
| A.氧化铁 | a.作红色颜料 |
| B.乙烯 | b.作食用碱 |
| C.乙醇 | c.制塑料 |
| D.碳酸钠 | d.作医用消毒剂 |
您最近一年使用:0次
4 . 某实验小组欲通过加热蒸发KNO3溶液的方法获得KNO3固体。已知KNO3固体在一定温度下能够发生反应:2KNO3 2KNO2 + O2↑。为了探究加热蒸发所得固体X中是否含有KNO2,小组同学分别设计并完成了以下实验。
2KNO2 + O2↑。为了探究加热蒸发所得固体X中是否含有KNO2,小组同学分别设计并完成了以下实验。
【查阅资料】
ⅰ.AgNO2是微溶于水的白色(略带黄色)固体
ⅱ.KNO2能在酸性条件下与KI反应,生成I2
【实验过程】
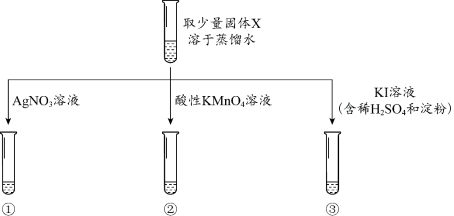
【分析解释】
(1)实验①中,观察到有少量白色沉淀生成,该白色沉淀是_______ 。
(2)实验②中,观察到酸性KMnO4溶液紫红色褪去,利用对比实验排除了稀释对溶液颜色变化的影响。补全该反应的离子方程式:2MnO + 5NO
+ 5NO + 6H+ = 2Mn2+ +
+ 6H+ = 2Mn2+ +_______ + 3H2O
(3)实验③中,观察到溶液变为蓝色。实验③中选择KI溶液的依据是_______ (填字母)。
a.KNO2具有氧化性,KI具有还原性
b.KNO2具有还原性,KI具有氧化性
【反思评价】
(4)综合上述实验,甲同学认为,实验①、②、③均可以证明固体X中含有KNO2;乙同学认为,通过实验③不能证明固体X中含有KNO2。乙同学的理由是_______ 。
 2KNO2 + O2↑。为了探究加热蒸发所得固体X中是否含有KNO2,小组同学分别设计并完成了以下实验。
2KNO2 + O2↑。为了探究加热蒸发所得固体X中是否含有KNO2,小组同学分别设计并完成了以下实验。【查阅资料】
ⅰ.AgNO2是微溶于水的白色(略带黄色)固体
ⅱ.KNO2能在酸性条件下与KI反应,生成I2
【实验过程】

【分析解释】
(1)实验①中,观察到有少量白色沉淀生成,该白色沉淀是
(2)实验②中,观察到酸性KMnO4溶液紫红色褪去,利用对比实验排除了稀释对溶液颜色变化的影响。补全该反应的离子方程式:2MnO
 + 5NO
+ 5NO + 6H+ = 2Mn2+ +
+ 6H+ = 2Mn2+ +(3)实验③中,观察到溶液变为蓝色。实验③中选择KI溶液的依据是
a.KNO2具有氧化性,KI具有还原性
b.KNO2具有还原性,KI具有氧化性
【反思评价】
(4)综合上述实验,甲同学认为,实验①、②、③均可以证明固体X中含有KNO2;乙同学认为,通过实验③不能证明固体X中含有KNO2。乙同学的理由是
您最近一年使用:0次
2022-04-15更新
|
290次组卷
|
2卷引用:北京市2021-2022学年高三年级下学期合格考(第一次)化学试题
名校
5 . 碘及其化合物广泛用于医药、染料等方面。从含I-废水中可提取碘单质,其主要工艺流程如下:
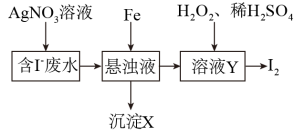
(1)已知:AgI难溶于水。写出AgNO3溶液与废水中I-反应的离子方程式_______ 。
(2)Fe与悬浊液反应时,采用铁粉可增大化学反应速率,其原因是_______ 。
(3)Fe与悬浊液反应后,溶液Y中的溶质主要是FeI2,则沉淀X为反应剩余的Fe和_______ 。
(4)向溶液Y中加入H2O2的目的是_______ 。

(1)已知:AgI难溶于水。写出AgNO3溶液与废水中I-反应的离子方程式
(2)Fe与悬浊液反应时,采用铁粉可增大化学反应速率,其原因是
(3)Fe与悬浊液反应后,溶液Y中的溶质主要是FeI2,则沉淀X为反应剩余的Fe和
(4)向溶液Y中加入H2O2的目的是
您最近一年使用:0次
2022-04-15更新
|
186次组卷
|
2卷引用:北京市2021-2022学年高三年级下学期合格考(第一次)化学试题
解题方法
6 . 海洋是巨大的化学资源宝库。从海水中可以制取氯、溴、镁等多种化工产品。
(1)Mg在元素周期表中的位置是第_______ 周期、第IIA族。
(2)Cl的最高价氧化物对应的水化物为HClO4,其中氯元素的化合价是_______ 。
(3)金属性Na强于Mg,用原子结构解释原因:Na和Mg位于同一周期,原子核外电子层数相同,_______ ,原子半径Na大于Mg,失电子能力Na强于Mg。
(4)在元素周期表中,溴(Br)位于第4周期,与Cl同主族。下列实验或事实能说明得电子能力Cl强于Br的是_______ (填字母)。
a.将Cl2通入KBr溶液中可制得Br2
b.常温常压下,Cl2为气态,Br2为液态
c.HBr约500℃开始分解,HCl约1000℃开始缓慢分解
(1)Mg在元素周期表中的位置是第
(2)Cl的最高价氧化物对应的水化物为HClO4,其中氯元素的化合价是
(3)金属性Na强于Mg,用原子结构解释原因:Na和Mg位于同一周期,原子核外电子层数相同,
(4)在元素周期表中,溴(Br)位于第4周期,与Cl同主族。下列实验或事实能说明得电子能力Cl强于Br的是
a.将Cl2通入KBr溶液中可制得Br2
b.常温常压下,Cl2为气态,Br2为液态
c.HBr约500℃开始分解,HCl约1000℃开始缓慢分解
您最近一年使用:0次
名校
解题方法
7 . 阅读短文,回答问题。
我国科研团队在人工合成淀粉方面取得重要进展,在实验室实现从二氧化碳到淀粉的全合成。

人工合成淀粉是如何实现的?科研团队利用催化剂将高浓度二氧化碳在氢气作用下还原成碳一化合物,然后将碳一化合物聚合成碳三化合物,又将碳三化合物聚合成碳六化合物,再进一步合成淀粉。
人工合成淀粉有多大意义?检测发现,人工合成淀粉分子与天然淀粉分子的组成结构一致。如果人工合成淀粉产业化成功,全球性的粮食危机有望得到彻底解决。同时合成过程中使用大量的二氧化碳,引起全球变暖的最主要温室气体将被有效利用。
请依据以上短文,判断下列说法是否正确(填“对”或“错”)。
(1)二氧化碳和淀粉都属于含碳物质。_______
(2)从碳一化合物逐步合成淀粉的过程中,碳链逐渐增长。_______
(3)人工合成淀粉分子与天然淀粉分子的组成结构不同。_______
(4)人工合成淀粉产业化,有利于解决粮食危机和缓解温室效应。_______
我国科研团队在人工合成淀粉方面取得重要进展,在实验室实现从二氧化碳到淀粉的全合成。

人工合成淀粉是如何实现的?科研团队利用催化剂将高浓度二氧化碳在氢气作用下还原成碳一化合物,然后将碳一化合物聚合成碳三化合物,又将碳三化合物聚合成碳六化合物,再进一步合成淀粉。
人工合成淀粉有多大意义?检测发现,人工合成淀粉分子与天然淀粉分子的组成结构一致。如果人工合成淀粉产业化成功,全球性的粮食危机有望得到彻底解决。同时合成过程中使用大量的二氧化碳,引起全球变暖的最主要温室气体将被有效利用。
请依据以上短文,判断下列说法是否正确(填“对”或“错”)。
(1)二氧化碳和淀粉都属于含碳物质。
(2)从碳一化合物逐步合成淀粉的过程中,碳链逐渐增长。
(3)人工合成淀粉分子与天然淀粉分子的组成结构不同。
(4)人工合成淀粉产业化,有利于解决粮食危机和缓解温室效应。
您最近一年使用:0次
2022-04-15更新
|
227次组卷
|
3卷引用:北京市2021-2022学年高三年级下学期合格考(第一次)化学试题
名校
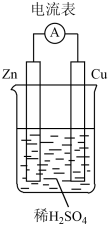
8 . 根据原电池原理,人们研制出了性能各异的化学电池。
(1)如图装置中,Zn片作_______ (填“正极”或“负极”),Cu片上发生反应的电极反应式为_______ ,能证明化学能转化为电能的实验现象是_______ 。 = Mg2+ + 3Br-。下列说法正确的是
= Mg2+ + 3Br-。下列说法正确的是_______ (填字母)。
(1)如图装置中,Zn片作
 = Mg2+ + 3Br-。下列说法正确的是
= Mg2+ + 3Br-。下列说法正确的是
您最近一年使用:0次
2022-04-15更新
|
210次组卷
|
3卷引用:北京市2021-2022学年高三年级下学期合格考(第一次)化学试题
9 . 某小组同学利用以下实验装置研究SO2的性质(经检验,装置的气密性良好)。

(1)①中的现象是_______ 。
(2)②中石蕊溶液变红,说明SO2与H2O反应生成了酸性物质。写出该反应的化学方程式:_______ 。
(3)③中产生淡黄色浑浊,体现了SO2的_______ (填字母)。
a.氧化性 b.还原性
(4)④用于吸收多余的SO2,可选用的试剂是_______ 。

(1)①中的现象是
(2)②中石蕊溶液变红,说明SO2与H2O反应生成了酸性物质。写出该反应的化学方程式:
(3)③中产生淡黄色浑浊,体现了SO2的
a.氧化性 b.还原性
(4)④用于吸收多余的SO2,可选用的试剂是
您最近一年使用:0次
2022-04-15更新
|
227次组卷
|
3卷引用:北京市2021-2022学年高三年级下学期合格考(第一次)化学试题
名校
解题方法
10 . 木炭与浓硫酸发生反应:C+2H2SO4(浓) CO2↑+2SO2↑+2H2O。
CO2↑+2SO2↑+2H2O。
(1)作还原剂的物质是_______ ,硫元素的化合价_______ (填“升高”或“降低”)。
(2)反应中每生成1mol CO2,消耗C的物质的量是_______ mol,转移电子的物质的量是_______ mol。
 CO2↑+2SO2↑+2H2O。
CO2↑+2SO2↑+2H2O。(1)作还原剂的物质是
(2)反应中每生成1mol CO2,消耗C的物质的量是
您最近一年使用:0次
2022-04-15更新
|
290次组卷
|
3卷引用:北京市2021-2022学年高三年级下学期合格考(第一次)化学试题



