海洋是巨大的化学资源宝库。从海水中可以制取氯、溴、镁等多种化工产品。
(1)Mg在元素周期表中的位置是第_______ 周期、第IIA族。
(2)Cl的最高价氧化物对应的水化物为HClO4,其中氯元素的化合价是_______ 。
(3)金属性Na强于Mg,用原子结构解释原因:Na和Mg位于同一周期,原子核外电子层数相同,_______ ,原子半径Na大于Mg,失电子能力Na强于Mg。
(4)在元素周期表中,溴(Br)位于第4周期,与Cl同主族。下列实验或事实能说明得电子能力Cl强于Br的是_______ (填字母)。
a.将Cl2通入KBr溶液中可制得Br2
b.常温常压下,Cl2为气态,Br2为液态
c.HBr约500℃开始分解,HCl约1000℃开始缓慢分解
(1)Mg在元素周期表中的位置是第
(2)Cl的最高价氧化物对应的水化物为HClO4,其中氯元素的化合价是
(3)金属性Na强于Mg,用原子结构解释原因:Na和Mg位于同一周期,原子核外电子层数相同,
(4)在元素周期表中,溴(Br)位于第4周期,与Cl同主族。下列实验或事实能说明得电子能力Cl强于Br的是
a.将Cl2通入KBr溶液中可制得Br2
b.常温常压下,Cl2为气态,Br2为液态
c.HBr约500℃开始分解,HCl约1000℃开始缓慢分解
更新时间:2022-04-15 21:36:19
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】下面是元素周期表的草图,表中所列字母代号分别代表某一种元素,请回答:

(1)表中的实线表示元素周期表的左右边界,请用实线补全元素周期表的上下边界。________
(2)表中最活泼的金属与最活泼的非金属形成的物质是________ (填化学式)。
(3)由a、d两种元素可形成两种化合物,写出其中一种化合物分解生成另一种化合物的化学方程式:_______ ,这两种化合物中所含的化学键有______ (填字母)。
A.极性共价键 B.非极性共价键 C.离子键
(4) e、f、k、m对应的单原子离子的半径由大到小的顺序为____________ (填离子符号)。
(5) d、m对应的离子还原性由强到弱顺序为__________ (填离子符号)。
(6) d、e、m的气态氢化物中,最不稳定的是__________ (填分子式)。

(1)表中的实线表示元素周期表的左右边界,请用实线补全元素周期表的上下边界。
(2)表中最活泼的金属与最活泼的非金属形成的物质是
(3)由a、d两种元素可形成两种化合物,写出其中一种化合物分解生成另一种化合物的化学方程式:
A.极性共价键 B.非极性共价键 C.离子键
(4) e、f、k、m对应的单原子离子的半径由大到小的顺序为
(5) d、m对应的离子还原性由强到弱顺序为
(6) d、e、m的气态氢化物中,最不稳定的是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】我国的四大发明之一黑火药,爆炸时发生反应的化学方程式为: S+2KNO3+3C=K2S+3CO2↑+N2↑。
请根据其中所含的元素回答下列问题:
(1)如图所示为元素周期表中钾元素框图,
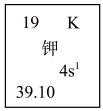
数据“39.10”表示的是___________ ;钾元素在周期表中的位置为___________ 。
(2)上述元素中,简单离子半径最大的元素,已知其氧化物中一种对应水化物能与氯单质反应,该反应的化学方程式是___________ 。
(3)上述反应生成物中,属于非电解质的是___________ (写结构式);生成物中含有离子键的物质电子式是___________ 。
(4)上述化学方程式的元素中,属于同周期元素的原子半径由大到小顺序为___________ ,它们的非金属性由强到弱的顺序为___________ ;列举一条能证明S和O非金属性强弱的实验事实___________ 。
请根据其中所含的元素回答下列问题:
(1)如图所示为元素周期表中钾元素框图,

数据“39.10”表示的是
(2)上述元素中,简单离子半径最大的元素,已知其氧化物中一种对应水化物能与氯单质反应,该反应的化学方程式是
(3)上述反应生成物中,属于非电解质的是
(4)上述化学方程式的元素中,属于同周期元素的原子半径由大到小顺序为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】下表是元素周期表的一部分,回答下列有关问题:
(1)①-⑪中,属于长周期的元素是______  填序号
填序号 。
。
(2)①-⑪中,最活泼的金属元素是______  填元素符号
填元素符号 ,在空气中燃烧的产物是
,在空气中燃烧的产物是______  写出电子式
写出电子式 。
。
(3)①-⑪中,最不活泼的元素其原子结构示意图为______ 。
(4)③④⑤三种元素对应的简单阳离子中,半径最大的离子结构示意图为______ 。
(5)在这些元素的最高价氧化物对应水化物中,呈两性的氢氧化物是______  写化学式
写化学式 。
。
(6)若将④⑤的单质用导线相连插入稀硫酸溶液中形成原电池,则该原电池的负极反应式______ 。
周期 族 | ⅠA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 |
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
4 | ⑩ | ⑪ |
 填序号
填序号 。
。(2)①-⑪中,最活泼的金属元素是
 填元素符号
填元素符号 ,在空气中燃烧的产物是
,在空气中燃烧的产物是 写出电子式
写出电子式 。
。(3)①-⑪中,最不活泼的元素其原子结构示意图为
(4)③④⑤三种元素对应的简单阳离子中,半径最大的离子结构示意图为
(5)在这些元素的最高价氧化物对应水化物中,呈两性的氢氧化物是
 写化学式
写化学式 。
。(6)若将④⑤的单质用导线相连插入稀硫酸溶液中形成原电池,则该原电池的负极反应式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】元素在周期表中的位置,反映了元素的原子结构和元素的性质。下图是元素周期表的一部分。请用元素符号或化学式填空:

(1)所示元素中
①非金属性最强的元素是:_________
②金属性最强的元素是:___________
③原子半径最小的是:___________
④最高价含氧酸酸性最强的是______________
⑤经常用作半导体材料的元素是:___________ (只写一种)
⑥阴影部分属于元素周期表中的_________ 族,该族元素的最高正价均为_________
(2)根据元素周期律,推导:
①酸性强弱: H3AsO4_________ H3PO4(用“>”或“<”表示,下同);
②稳定性:H2S__________ HCl
③沸点:HF_____ HCl
④还原性:I-_______ Br-
⑤在O、F、S、Cl四种元素中,非金属性最接近的是:__________
A.O和F B.F和S C.S和Cl D.O和Cl
(3)根据同主族元素性质的相似性和递变性进行预测:
①关于Se的预测正确的是:________
A.常温下Se单质是气体
B. Se最高价氧化物的水化物能和NaOH发生反应
C. 氢化物的化学式为H2Se
D. 常见的氧化物只有SeO3
②已知Cl2在水溶液中能和SO2反应,Cl2+2H2O+SO2==H2SO4+2HCl,写出Br2在水溶液中和SO2反应的离子反应方程式___________________________________

(1)所示元素中
①非金属性最强的元素是:
②金属性最强的元素是:
③原子半径最小的是:
④最高价含氧酸酸性最强的是
⑤经常用作半导体材料的元素是:
⑥阴影部分属于元素周期表中的
(2)根据元素周期律,推导:
①酸性强弱: H3AsO4
②稳定性:H2S
③沸点:HF
④还原性:I-
⑤在O、F、S、Cl四种元素中,非金属性最接近的是:
A.O和F B.F和S C.S和Cl D.O和Cl
(3)根据同主族元素性质的相似性和递变性进行预测:
①关于Se的预测正确的是:
A.常温下Se单质是气体
B. Se最高价氧化物的水化物能和NaOH发生反应
C. 氢化物的化学式为H2Se
D. 常见的氧化物只有SeO3
②已知Cl2在水溶液中能和SO2反应,Cl2+2H2O+SO2==H2SO4+2HCl,写出Br2在水溶液中和SO2反应的离子反应方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】请用一个离子方程式说明钠与铝的金属性强弱__________________________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】硒(Se)是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光(AIE)效应以来,AIE在发光材料、生物医学等领域引起了广泛关注。
(1)Se与S是相邻周期的同主族元素,则Se在元素周期表中的位置为___________ ,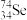 和
和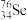 这两种原子的中子数之差的绝对值为
这两种原子的中子数之差的绝对值为___________ 。
(2)H2Se是一种有恶臭的气体,与H2O相比,沸点:H2Se___________ H2O(填“>”或“<”,下同),热稳定性:H2Se___________ H2O。
(3)较高浓度的Na2SeO3能促进细胞DNA的增殖活性,延缓细胞衰老,但无机硒的毒性逐渐成为限制它使用的一个非常重要的因素。Na、Se、O形成的简单离子的半径由大到小的顺序为___________ (填离子符号)。
(4)一种合成含Se的新型AIE分子的原料结构如图:
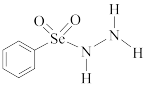
肼(N2H4)的结构与上述分子部分结构十分相似,N2H4的电子式为___________ 。
(1)Se与S是相邻周期的同主族元素,则Se在元素周期表中的位置为
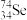 和
和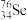 这两种原子的中子数之差的绝对值为
这两种原子的中子数之差的绝对值为(2)H2Se是一种有恶臭的气体,与H2O相比,沸点:H2Se
(3)较高浓度的Na2SeO3能促进细胞DNA的增殖活性,延缓细胞衰老,但无机硒的毒性逐渐成为限制它使用的一个非常重要的因素。Na、Se、O形成的简单离子的半径由大到小的顺序为
(4)一种合成含Se的新型AIE分子的原料结构如图:

肼(N2H4)的结构与上述分子部分结构十分相似,N2H4的电子式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】下表是元素周期表的一部分,①~⑦代表七种元素,它们在元素周期表中的位置如下。
请回答下列问题:
(1)元素⑥的原子结构示意图为___________ 。
(2)元素②~⑦最高价氧化物的水化物中,碱性最强的是___________ (填化学式)。
(3)②、③、④三种元素中,原子半径最小的是___________ (填元素符号)。
(4)元素①和⑦组成的化合物的水溶液与元素④的单质发生反应,其离子方程式为_______ 。
族 周期 | IA | 0 | ||||||
1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
2 | ② | ③ | ||||||
3 | ④ | ⑤ | ⑥ | ⑦ |
请回答下列问题:
(1)元素⑥的原子结构示意图为
(2)元素②~⑦最高价氧化物的水化物中,碱性最强的是
(3)②、③、④三种元素中,原子半径最小的是
(4)元素①和⑦组成的化合物的水溶液与元素④的单质发生反应,其离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】如表是元素周期表的一部分,根据表中给出的10种元素,按要求作答。
(1)金属性最强的元素是_______ ;
(2)F的原子结构示意图是________ ;
(3)地壳中含量最多的元素是_______ ;
(4)Ne原子的最外层电子数是_______ ;
(5)N与O原子半径较大的是_______ ;
(6)H2S与HCl热稳定性较弱的是______ ;
(7)Na2O与MgO难与水反应的是______ ;
(8)Mg(OH)2与Al(OH)3能与强碱反应的是______ ;
(9)用于制造光导纤维的物质是______ (填“Si”或“SiO2”);
(10)次氯酸(HClO)具有杀菌漂白作用,其中Cl元素的化合价为____ ,HClO不稳定,易分解生成HCl和O2,写出其在光照条件下分解的化学方程式:____ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | N | O | F | Ne | ||||
| 3 | Na | Mg | Al | Si | S | Cl |
(1)金属性最强的元素是
(2)F的原子结构示意图是
(3)地壳中含量最多的元素是
(4)Ne原子的最外层电子数是
(5)N与O原子半径较大的是
(6)H2S与HCl热稳定性较弱的是
(7)Na2O与MgO难与水反应的是
(8)Mg(OH)2与Al(OH)3能与强碱反应的是
(9)用于制造光导纤维的物质是
(10)次氯酸(HClO)具有杀菌漂白作用,其中Cl元素的化合价为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】请根据以上讨论来分析说明硫、氯两元素中哪种元素原子的得电子能力强______ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】下表是元素周期表的一部分,请参照元素①~⑩在表中的位置,回答下列问题。
(1)②的原子结构示意图是_______ 。
(2)化学性质最不活泼的元素是_______ (填元素符号)。
(3)在③、④、⑤、⑥这些元素形成的最简单离子中,离子半径由大到小的顺序是_______ (填离子符号)。
(4)表中④⑧⑨元素的氢化物的稳定性最强的为_______ (填化学式)。
(5)表中元素⑤与元素⑥金属性更强的是_______ (填化学式),这两种元素的最高价氧化物对应的水化物之间反应的离子方程式为_______ ;
(6)元素③、⑤能形成两种化合物,其中较稳定的化合物的电子式为_______
(7)在这些元素的最高价氧化物对应的水化物中,酸性最强的物质的化学式为_______ ,碱性最强的物质的化学式为_______ 。
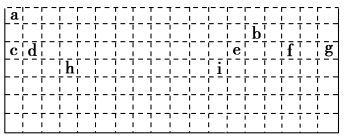
(8)下图是不完整的元素周期表,补全元素周期表的轮廓____________ 。
| 族周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)化学性质最不活泼的元素是
(3)在③、④、⑤、⑥这些元素形成的最简单离子中,离子半径由大到小的顺序是
(4)表中④⑧⑨元素的氢化物的稳定性最强的为
(5)表中元素⑤与元素⑥金属性更强的是
(6)元素③、⑤能形成两种化合物,其中较稳定的化合物的电子式为
(7)在这些元素的最高价氧化物对应的水化物中,酸性最强的物质的化学式为
(8)下图是不完整的元素周期表,补全元素周期表的轮廓

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】如表是元素周期表的一部分,根据表中列出的10种元素,回答下列问题。
(1)地壳中含量最多的元素是____ 。
(2)氯元素位于元素周期表第____ 周期VIIA族。
(3)单质的化学性质最不活泼的是____ 。
(4)HF和HCl中,热稳定性较强的是____ 。
(5)元素最高价氧化物对应的水化物中,碱性最强的是____ (填化学式)。
(6)碳元素的最高价氧化物中碳元素与氧元素的质量比m(C):m(O)=____ 。
| 周期 族 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | C | N | O | F | ||||
| 3 | Na | Al | Si | S | Cl | Ar |
(2)氯元素位于元素周期表第
(3)单质的化学性质最不活泼的是
(4)HF和HCl中,热稳定性较强的是
(5)元素最高价氧化物对应的水化物中,碱性最强的是
(6)碳元素的最高价氧化物中碳元素与氧元素的质量比m(C):m(O)=
您最近一年使用:0次



