从海带浸泡液(碘元素主要以 存在)中获取
存在)中获取 ,含碘物质的转化过程如下。
,含碘物质的转化过程如下。 的作用为
的作用为_______ (填“氧化剂”或“还原剂”)。
(2)为提高①的化学反应速率,可采取的措施是_______ (写出一条即可)。
(3)补全②的离子方程式:_______ 。
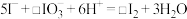
(4)②中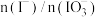 和pH对碘离子的氧化率的影响如下图所示。
和pH对碘离子的氧化率的影响如下图所示。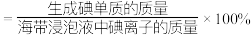
分析图中信息,选择最佳条件:_______ 。
 存在)中获取
存在)中获取 ,含碘物质的转化过程如下。
,含碘物质的转化过程如下。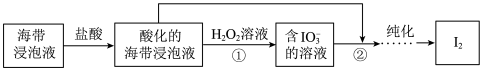
 的作用为
的作用为(2)为提高①的化学反应速率,可采取的措施是
(3)补全②的离子方程式:
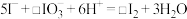
(4)②中
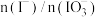 和pH对碘离子的氧化率的影响如下图所示。
和pH对碘离子的氧化率的影响如下图所示。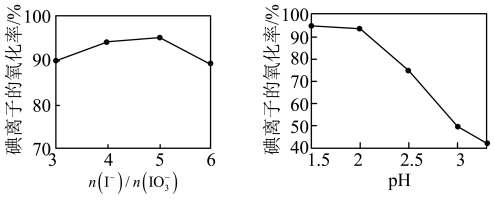
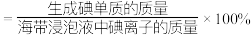
分析图中信息,选择最佳条件:
更新时间:2024-05-23 13:49:14
|
相似题推荐
【推荐1】含氯物质在日常生活中具有许多重要用途,回答下列问题:
(1)工业上常利用反应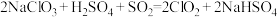 制备ClO2,其中还原剂是
制备ClO2,其中还原剂是___________ 。
(2)亚氯酸钠(NaClO2)较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的产物可能为___________(填标号)。
(3)工业上可利用ClO2制备亚氯酸钠(NaClO2),反应体系中涉及下列物质(有一种物质未列出):NaClO2、ClO2、H2O2、NaOH、O2,写出反应的化学方程式___________ 。
(4)某温度下将Cl2通入KOH溶液里,反应后得到KCl、KClO、KClO3,的混合溶液,其中ClO—与 的个数之比为11∶1,则Cl2与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为
的个数之比为11∶1,则Cl2与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为___________ 。
(5)已知还原性:I—>Fe2+>Cl—,写出少量氯气通入到FeI2溶液中的离子方程式___________ 。
(6)实验室用下列方法均可制取氯气
①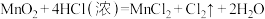
②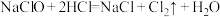
③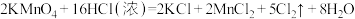
④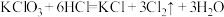
若各反应转移的电子数相同,①②③④生成的氯气质量比为___________ 。
(1)工业上常利用反应
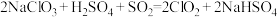 制备ClO2,其中还原剂是
制备ClO2,其中还原剂是(2)亚氯酸钠(NaClO2)较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的产物可能为___________(填标号)。
| A.NaCl、Cl2 | B.NaCl、NaClO |
| C.NaClO3、NaClO4 | D.NaCl、NaClO3 |
(4)某温度下将Cl2通入KOH溶液里,反应后得到KCl、KClO、KClO3,的混合溶液,其中ClO—与
 的个数之比为11∶1,则Cl2与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为
的个数之比为11∶1,则Cl2与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为(5)已知还原性:I—>Fe2+>Cl—,写出少量氯气通入到FeI2溶液中的离子方程式
(6)实验室用下列方法均可制取氯气
①
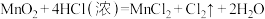
②
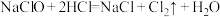
③
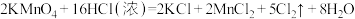
④
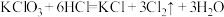
若各反应转移的电子数相同,①②③④生成的氯气质量比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】工业上用MnO2和KOH为原料制取高锰酸钾,主要生产过程分两步进行。第一步将MnO2和固体KOH粉碎,混合均匀,在空气中加热至熔化,并连续搅拌,制取K2MnO4;第二步将K2MnO4的浓溶液进行电解,制取KMnO4.试回答以下问题:
(1)制取K2MnO4的MnO2是这一氧化还原反应的_______ 剂(填“氧化”或“还原”),连续搅拌的目的是_______ 。
(2)电解K2MnO4的浓溶液时,两极发生的电极反应式为:
阴极是_______ ,
阳极是_______ ,
电解总的反应方程式是_______ 。
(1)制取K2MnO4的MnO2是这一氧化还原反应的
(2)电解K2MnO4的浓溶液时,两极发生的电极反应式为:
阴极是
阳极是
电解总的反应方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)请按要求写出下列反应的化学方程式或离子方程式:
①物质的量之比为2:5的锌与稀硝酸反应,若硝酸被还原的产物为N2O,反应结束后锌没有剩余,写出该反应的化学方程式________ 。
②ClO2常用于水的净化,工业上可用Cl2氧化Na ClO2溶液制取ClO2.写出该反应的离子方程式:__________ 。
③Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO42-,常用作脱氯剂,该反应的离子方程式为________ 。
④NaBH4是一种重要的储氢载体,能与水反应达到NaBO2,且反应前后B的化合价不变,该反应的化学方程式为_________ 。
(2)四氧化三铁(Fe3O4)磁性纳米颗粒稳定、容易生产且用途广泛,是临床诊断、生物技术和环境化学领域多种潜在应用的有力工具。水热法制备Fe3O4纳米颗粒的反应是3Fe2++2S2O32-+O2+xOH-═Fe3O4+S4O62-+2H2O。请回答下列问题。
①水热法制备Fe3O4纳米颗粒的反应中,还原剂是_________ 。反应的化学方程式中x=_________ 。
②每生成1 mol Fe3O4,反应转移的电子为________ mol,被Fe2+还原的O2的物质的量为________ mol。
①物质的量之比为2:5的锌与稀硝酸反应,若硝酸被还原的产物为N2O,反应结束后锌没有剩余,写出该反应的化学方程式
②ClO2常用于水的净化,工业上可用Cl2氧化Na ClO2溶液制取ClO2.写出该反应的离子方程式:
③Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO42-,常用作脱氯剂,该反应的离子方程式为
④NaBH4是一种重要的储氢载体,能与水反应达到NaBO2,且反应前后B的化合价不变,该反应的化学方程式为
(2)四氧化三铁(Fe3O4)磁性纳米颗粒稳定、容易生产且用途广泛,是临床诊断、生物技术和环境化学领域多种潜在应用的有力工具。水热法制备Fe3O4纳米颗粒的反应是3Fe2++2S2O32-+O2+xOH-═Fe3O4+S4O62-+2H2O。请回答下列问题。
①水热法制备Fe3O4纳米颗粒的反应中,还原剂是
②每生成1 mol Fe3O4,反应转移的电子为
您最近一年使用:0次
【推荐2】 是实验室的常用试剂,可以由
是实验室的常用试剂,可以由 为原料经过多步反应制得。
为原料经过多步反应制得。
(1) 与KOH在空气中熔融可以制得
与KOH在空气中熔融可以制得 。该反应的方程式为:
。该反应的方程式为:
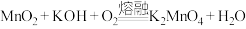 (未配平)
(未配平)
①该反应的还原剂为______ 。
②反应中每生成1 mol ,转移电子的物质的量为
,转移电子的物质的量为______ 。
③配平后的反应方程式中 前的化学计量数为
前的化学计量数为______ 。
(2)将制得的 固体溶于水,向其中通入
固体溶于水,向其中通入 .会发生如下反应:
.会发生如下反应:
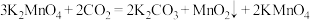 ;
;
用单线桥表示该反应中电子转移的方向和数目:______ 。
(3) 时,向
时,向 的溶液中滴加
的溶液中滴加 溶液,反应后Mn元素均转化为
溶液,反应后Mn元素均转化为 沉淀。
沉淀。
由此可知酸性条件下粒子的氧化性大小:______ >______ 。
(4)磷酸锰铵是重要的复盐,在工农业生产中具有广泛应用。实验室为了测定磷酸锰铵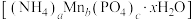 的组成,进行如下实验:①称取样品2.4480g,加水溶解后配成100.00mL溶液A;②量取25.00mL溶液A,加足量NaOH溶液并充分加热,生成(标准状况下)0.06720 L
的组成,进行如下实验:①称取样品2.4480g,加水溶解后配成100.00mL溶液A;②量取25.00mL溶液A,加足量NaOH溶液并充分加热,生成(标准状况下)0.06720 L  ;③另取25.00mL溶液A,边鼓空气边缓慢滴加氨水,控制溶液pH6~8,充分反应后,将溶液中
;③另取25.00mL溶液A,边鼓空气边缓慢滴加氨水,控制溶液pH6~8,充分反应后,将溶液中 转化为
转化为 ,得
,得 0.2290 g。通过计算确定该样品的化学式
0.2290 g。通过计算确定该样品的化学式____ (写出计算过程)。
 是实验室的常用试剂,可以由
是实验室的常用试剂,可以由 为原料经过多步反应制得。
为原料经过多步反应制得。(1)
 与KOH在空气中熔融可以制得
与KOH在空气中熔融可以制得 。该反应的方程式为:
。该反应的方程式为: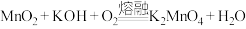 (未配平)
(未配平)①该反应的还原剂为
②反应中每生成1 mol
 ,转移电子的物质的量为
,转移电子的物质的量为③配平后的反应方程式中
 前的化学计量数为
前的化学计量数为(2)将制得的
 固体溶于水,向其中通入
固体溶于水,向其中通入 .会发生如下反应:
.会发生如下反应: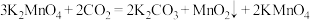 ;
;用单线桥表示该反应中电子转移的方向和数目:
(3)
 时,向
时,向 的溶液中滴加
的溶液中滴加 溶液,反应后Mn元素均转化为
溶液,反应后Mn元素均转化为 沉淀。
沉淀。由此可知酸性条件下粒子的氧化性大小:
(4)磷酸锰铵是重要的复盐,在工农业生产中具有广泛应用。实验室为了测定磷酸锰铵
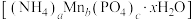 的组成,进行如下实验:①称取样品2.4480g,加水溶解后配成100.00mL溶液A;②量取25.00mL溶液A,加足量NaOH溶液并充分加热,生成(标准状况下)0.06720 L
的组成,进行如下实验:①称取样品2.4480g,加水溶解后配成100.00mL溶液A;②量取25.00mL溶液A,加足量NaOH溶液并充分加热,生成(标准状况下)0.06720 L  ;③另取25.00mL溶液A,边鼓空气边缓慢滴加氨水,控制溶液pH6~8,充分反应后,将溶液中
;③另取25.00mL溶液A,边鼓空气边缓慢滴加氨水,控制溶液pH6~8,充分反应后,将溶液中 转化为
转化为 ,得
,得 0.2290 g。通过计算确定该样品的化学式
0.2290 g。通过计算确定该样品的化学式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】利用物质类别及核心元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系。回答下列问题:
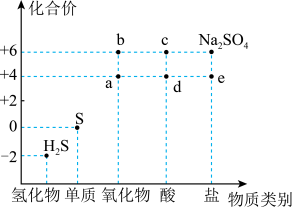
(1)质量相同的a和b,物质的量之比为___________ 。
(2)c的浓溶液能与S反应产生一种气体,该气体的化学式为___________ 。
(3)宋代著名法医学家宋慈的《洗冤集录》中有“银针验毒”的记载,“银针验毒”的原理: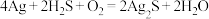 。
。 在该反应中___________(填标号)。
在该反应中___________(填标号)。
(4)将足量的a通入 溶液中,下列说法正确的是
溶液中,下列说法正确的是___________ (填标号)。
A.溶液中出现白色沉淀
B.溶液没有明显变化
C.若再通入 或
或 ,则溶液中均会出现白色沉淀
,则溶液中均会出现白色沉淀
(5)已知e为正盐,且能被酸性 氧化为
氧化为 ,
, 被还原为
被还原为 ,写出此反应的离子方程式:
,写出此反应的离子方程式:___________ 。

(1)质量相同的a和b,物质的量之比为
(2)c的浓溶液能与S反应产生一种气体,该气体的化学式为
(3)宋代著名法医学家宋慈的《洗冤集录》中有“银针验毒”的记载,“银针验毒”的原理:
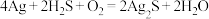 。
。 在该反应中___________(填标号)。
在该反应中___________(填标号)。| A.是氧化剂 | B.是还原剂 |
| C.既是氧化剂也是还原剂 | D.既不是氧化剂也不是还原剂 |
(4)将足量的a通入
 溶液中,下列说法正确的是
溶液中,下列说法正确的是A.溶液中出现白色沉淀
B.溶液没有明显变化
C.若再通入
 或
或 ,则溶液中均会出现白色沉淀
,则溶液中均会出现白色沉淀(5)已知e为正盐,且能被酸性
 氧化为
氧化为 ,
, 被还原为
被还原为 ,写出此反应的离子方程式:
,写出此反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】从海水中制取镁、溴、碘及其化工产品。
①海水中镁的提取
主要流程:
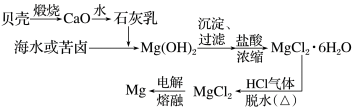
主要化学反应
制石灰乳:CaCO3 CaO+CO2↑、CaO+H2O=Ca(OH)2;
CaO+CO2↑、CaO+H2O=Ca(OH)2;
沉淀Mg2+:Mg2++Ca(OH)2=Mg(OH)2+Ca2+;
制备MgCl2:Mg(OH)2+2HCl=MgCl2+2H2O、MgCl2·6H2O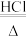 MgCl2+6H2O;
MgCl2+6H2O;
电解MgCl2:MgCl2(熔融) Mg+Cl2↑。
Mg+Cl2↑。
②海水中溴的提取
主要流程:
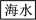
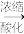
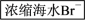

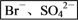
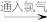
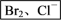
有关反应的化学方程式:__________ 、________ 、___________ 。
③海带中碘的提取
主要流程:
有关反应的离子方程式:_______ 或________
①海水中镁的提取
主要流程:

主要化学反应
制石灰乳:CaCO3
 CaO+CO2↑、CaO+H2O=Ca(OH)2;
CaO+CO2↑、CaO+H2O=Ca(OH)2;沉淀Mg2+:Mg2++Ca(OH)2=Mg(OH)2+Ca2+;
制备MgCl2:Mg(OH)2+2HCl=MgCl2+2H2O、MgCl2·6H2O
 MgCl2+6H2O;
MgCl2+6H2O;电解MgCl2:MgCl2(熔融)
 Mg+Cl2↑。
Mg+Cl2↑。②海水中溴的提取
主要流程:
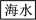
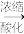
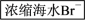
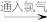
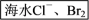

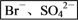
有关反应的化学方程式:
③海带中碘的提取
主要流程:

有关反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】I.海洋是生命的摇篮,浩瀚的海洋中蕴藏着丰富的资源。人们可以从海水中提取淡水和制得镁、溴等重要的化工产品。
(1)从海水中获得淡水的主要方法有蒸馏法、离子交换法和___________ 。离子交换法净化水的过程如图所示。下列说法正确的是___________ (填序号)。
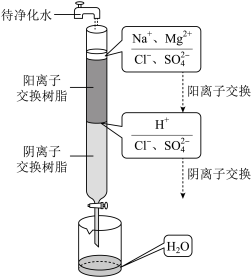
A.经过阳离子交换树脂后,水中阳离子总数
B.通过阴离子交换树脂后,水中只有 被除去
被除去
C.通过净化处理后的水,导电性增强
D.阴离子交换树脂填充段存在反应:
(2)工业上通过 制备Mg,常用的冶炼方法是
制备Mg,常用的冶炼方法是___________ 。制备溴时通入热空气可以吹出溴,是利用了溴的___________ 。
Ⅱ.海带中含有碘元素。从海带中提取碘的实验过程如下图所示:
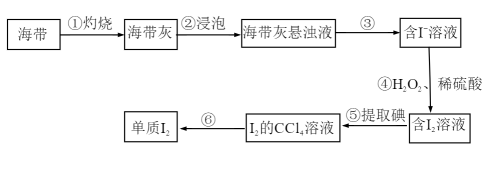
(3)实验步骤①不会用到下列仪器中的___________ (填字母)
a.泥三角 b.250ml容量瓶 c.坩埚 d.漏斗 e.酒精灯
(4)步骤③的操作名称是___________
(5)步骤④中反应的离子方程式为___________
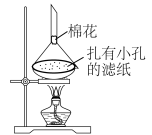
(6)利用如图装置,可以从氯化钠固体中分离出碘单质。简述原理________ ;棉花的作用是________ 。
(1)从海水中获得淡水的主要方法有蒸馏法、离子交换法和

A.经过阳离子交换树脂后,水中阳离子总数
B.通过阴离子交换树脂后,水中只有
 被除去
被除去C.通过净化处理后的水,导电性增强
D.阴离子交换树脂填充段存在反应:

(2)工业上通过
 制备Mg,常用的冶炼方法是
制备Mg,常用的冶炼方法是Ⅱ.海带中含有碘元素。从海带中提取碘的实验过程如下图所示:

(3)实验步骤①不会用到下列仪器中的
a.泥三角 b.250ml容量瓶 c.坩埚 d.漏斗 e.酒精灯
(4)步骤③的操作名称是
(5)步骤④中反应的离子方程式为
(6)利用如图装置,可以从氯化钠固体中分离出碘单质。简述原理

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】海洋资源和新型燃料电池的利用具有广阔前景。
(1)无需经过化学变化就能从海水中获得的物质是______ (填写字母)。
A. B.淡水 C.烧碱 D.食盐
B.淡水 C.烧碱 D.食盐
(2)从海水中提取溴的主要步骤是向浓缩的海水中通入氯气,将溴离子氧化,该反应的离子方程式是______ 。
(3)下圈是从海水中提取镁的简单流程。
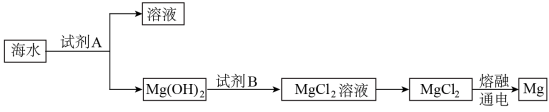
工业上常用于沉淀 的试剂
的试剂 是
是______ , 转化为
转化为 的离子方程式是
的离子方程式是______ 。
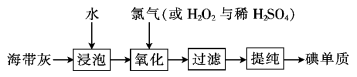
(4)海带灰中富含以碘离子形式存在的碘元素。 实验室提取 的途径如下所示,
的途径如下所示,
干海带 海带灰
海带灰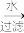 滤液
滤液
 I2
I2
①灼烧海带至灰烬时所用的主要仪器名称是______ 。
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式______ 。
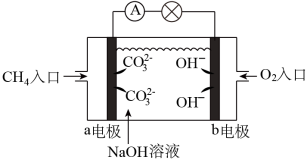
(5)甲烷燃料电池应用十分广泛。如下图,甲烷通入的一极的电极反应式为:______ ;当电路中累计有 电子通过时,消耗的氧气体积为
电子通过时,消耗的氧气体积为______  (在标准状况下)。
(在标准状况下)。
(1)无需经过化学变化就能从海水中获得的物质是
A.
 B.淡水 C.烧碱 D.食盐
B.淡水 C.烧碱 D.食盐(2)从海水中提取溴的主要步骤是向浓缩的海水中通入氯气,将溴离子氧化,该反应的离子方程式是
(3)下圈是从海水中提取镁的简单流程。

工业上常用于沉淀
 的试剂
的试剂 是
是 转化为
转化为 的离子方程式是
的离子方程式是(4)海带灰中富含以碘离子形式存在的碘元素。 实验室提取
 的途径如下所示,
的途径如下所示,干海带
 海带灰
海带灰 滤液
滤液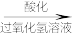
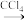
 I2
I2①灼烧海带至灰烬时所用的主要仪器名称是
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式
(5)甲烷燃料电池应用十分广泛。如下图,甲烷通入的一极的电极反应式为:
 电子通过时,消耗的氧气体积为
电子通过时,消耗的氧气体积为 (在标准状况下)。
(在标准状况下)。
您最近一年使用:0次



