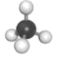
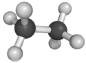
1 . 硒(Se)是动物和人体所必需的微量元素,硒单质是一种重要的工业原料。
(1)Se与S同一主族,Se在元素周期表的位置为:第4周期,___________ 。
(2)工业制备Se常用的原料含有硒化铜(CuSe),其中硒元素的化合价为___________ 。
(3)非金属性Br强于Se,用原子结构解释:Se和Br位于周期表中同一周期,原子核外电子层数相同,___________ ,___________ ,得电子能力Br大于Se.
(4)依据元素周期律,下列推断正确的是___________ (填字母)。
a.浓H2SeO4具有氧化性,可能有脱水性
b.热稳定性:H2S<H2Se<HCl
c.CuSe制备Se的过程会产生SeO2烟气,可用NaOH吸收
d.H2Se能与O2或Cl2反应生成Se单质
(1)Se与S同一主族,Se在元素周期表的位置为:第4周期,
(2)工业制备Se常用的原料含有硒化铜(CuSe),其中硒元素的化合价为
(3)非金属性Br强于Se,用原子结构解释:Se和Br位于周期表中同一周期,原子核外电子层数相同,
(4)依据元素周期律,下列推断正确的是
a.浓H2SeO4具有氧化性,可能有脱水性
b.热稳定性:H2S<H2Se<HCl
c.CuSe制备Se的过程会产生SeO2烟气,可用NaOH吸收
d.H2Se能与O2或Cl2反应生成Se单质
您最近一年使用:0次
2 . 某实验小组研究Zn单质与三价铁盐的反应。
【查阅资料】
1.25℃,pH<7溶液显酸性,pH越小,溶液中H+浓度越大,酸性越强。
2.1 mol·L-1的FeCl3溶液, pH>1时开始产生Fe(OH)3沉淀。
3.Fe2++NO [Fe(NO)]2+,[Fe(NO)]2+在溶液中呈棕色。
[Fe(NO)]2+,[Fe(NO)]2+在溶液中呈棕色。
【实验过程】
【分析解释】
(1)实验I中,经检验反应后的溶液中存在Fe2+,产生Fe2+的离子方程式为___________ 。
(2)实验II中,产生的大量气体为___________ (填化学式)。
(3)实验III中,溶液变成深棕色,NO 发生了如下反应,补全该反应的离子方程式:
发生了如下反应,补全该反应的离子方程式:___________ 。
(4)由实验I~IV可知:过量的Zn与Fe3+反应能否得到Fe单质与多种因素有关,能证明“阴离子种类”是影响因素的实验为___________ (填实验编号)。
(5)一定条件下Fe3+与过量Zn粉反应能够生成Fe单质,其原因与Zn、Fe2+、Fe还原性密切相关,三种微粒还原性由强到弱的顺序为___________
【查阅资料】
1.25℃,pH<7溶液显酸性,pH越小,溶液中H+浓度越大,酸性越强。
2.1 mol·L-1的FeCl3溶液, pH>1时开始产生Fe(OH)3沉淀。
3.Fe2++NO
 [Fe(NO)]2+,[Fe(NO)]2+在溶液中呈棕色。
[Fe(NO)]2+,[Fe(NO)]2+在溶液中呈棕色。【实验过程】
| 实验 | 编号 | 试剂 | 现象 |
| I | 0.1 mol·L-1 FeCl3溶液(pH≈1.30 ) | 黄色溶液很快变浅,有无色气泡产生,无铁产生 |
| II | 1 mol·L-1 FeCl3溶液 (pH≈0.70 ) | 片刻后有大量气体产生,出现红褐色浑浊,约半小时后,产生红褐色沉淀,溶液颜色变浅,产生少量铁 | |
| III | 1 mol·L-1 Fe(NO3)3溶液(pH≈0.70 ) | 约半小时后,溶液变为深棕色且浑浊,无铁产生 | |
| IV | 0.5 mol·L-1 Fe2(SO4)3溶液(pH≈0.70 ) | 约半小时后,溶液呈浅绿色且浑浊,产生少量铁 |
(1)实验I中,经检验反应后的溶液中存在Fe2+,产生Fe2+的离子方程式为
(2)实验II中,产生的大量气体为
(3)实验III中,溶液变成深棕色,NO
 发生了如下反应,补全该反应的离子方程式:
发生了如下反应,补全该反应的离子方程式:3Zn + NO
NO +8H+=3Zn2++
+8H+=3Zn2++ ___________+4H2O
___________+4H2O
(4)由实验I~IV可知:过量的Zn与Fe3+反应能否得到Fe单质与多种因素有关,能证明“阴离子种类”是影响因素的实验为
(5)一定条件下Fe3+与过量Zn粉反应能够生成Fe单质,其原因与Zn、Fe2+、Fe还原性密切相关,三种微粒还原性由强到弱的顺序为
您最近一年使用:0次
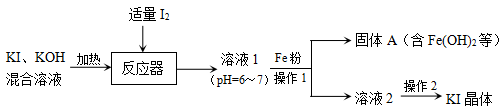
3 . KI广泛用于皮肤科、眼科等疾病的治疗,可以利用海水中获得的I2与KI、KOH的混合溶液为原料制备KI,流程如下:
ii.pH=6~7的溶液显弱酸性;
iii.KI的溶解度:
(1)溶液1中的溶质主要为KI、___________ (填化学式)。
(2)使用粉末状的铁能加快反应速率,原因是___________ 。
(3)用文字描述Fe所起的作用是___________ 。
(4)向固体A中加入稀硫酸能够制备FeSO4,该过程的离子方程式:___________ 、___________ 。
(5)操作2是___________ ,过滤,洗涤,干燥。
ii.pH=6~7的溶液显弱酸性;
iii.KI的溶解度:
| 温度/℃ | 6 | 20 | 60 | 100 |
| KI溶解度/g | 128 | 140 | 176 | 206 |
(2)使用粉末状的铁能加快反应速率,原因是
(3)用文字描述Fe所起的作用是
(4)向固体A中加入稀硫酸能够制备FeSO4,该过程的离子方程式:
(5)操作2是
您最近一年使用:0次
4 . 选择完成下列实验的装置。___________ (填序号,下同)。
(2)比较Na2CO3和NaHCO3的热稳定性,选用___________ 。
(3)加热MnO2和浓盐酸的混合物制Cl2,选用___________ 。
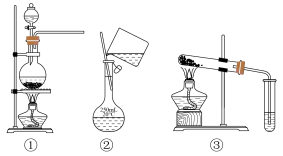
(2)比较Na2CO3和NaHCO3的热稳定性,选用
(3)加热MnO2和浓盐酸的混合物制Cl2,选用
您最近一年使用:0次
5 . 阅读短文,回答问题。
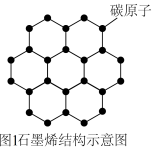
2022年北京冬奥会不仅是一次体育盛会,也是一场科技与创新的盛宴。在服装材料方面,颁奖礼仪服的内胆里添加了第二代石墨烯(如图)发热材料,能带来由内而外的温暖;速滑竞赛服使用了蜂窝样式的聚氨酯材料,以减少空气阻力。
请依据以上短文,判断下列说法是否正确(填“对”或“错”)。
(1)石墨烯中原子之间存在共价键。(___________)
(2)聚氨酯材料属于有机高分子材料。(___________)
(3)碳纤维导热性比金属材料的高。(___________)
(4)氢气是比烷烃更低碳环保的清洁能源。(___________)
2022年北京冬奥会不仅是一次体育盛会,也是一场科技与创新的盛宴。在服装材料方面,颁奖礼仪服的内胆里添加了第二代石墨烯(如图)发热材料,能带来由内而外的温暖;速滑竞赛服使用了蜂窝样式的聚氨酯材料,以减少空气阻力。
请依据以上短文,判断下列说法是否正确(填“对”或“错”)。
(1)石墨烯中原子之间存在共价键。(___________)
(2)聚氨酯材料属于有机高分子材料。(___________)
(3)碳纤维导热性比金属材料的高。(___________)
(4)氢气是比烷烃更低碳环保的清洁能源。(___________)
您最近一年使用:0次
6 . 下列实验事实得出的结论错误的是
| 选项 | 实验事实 | 结论 |
| A | 向某溶液中加入浓NaOH溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体 | 该溶液中一定含有NH |
| B | 向淀粉KI溶液中滴加溴水,溶液变蓝 | 氧化性:Br2>I2 |
| C | 氯气能使湿润的红色纸条褪色,但不能使干燥的红色纸条褪色 | 氯气与水发生了化学反应 |
| D | 向未知溶液中加入盐酸酸化的BaCl2溶液产生白色沉淀 | 该溶液中一定含有SO |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . 下列物质中,只含有离子键的是
| A.Cl2 | B.H2O | C.KCl | D.NaOH |
您最近一年使用:0次
8 . 下列烃的球棍模型中,属于“不饱和烃”的是
| 选项 | A | B | C | D |
| 球棍模型 |
|
|
|
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
9 . 化学电池的发明,改变了人们的生活方式。
(1)某原电池实验装置如图1。 片作
片作_______ (填“正极”或“负极”)。
② 片上的电极反应为
片上的电极反应为_______ 。
③能证明化学能转化为电能的实验现象是_______ 。
(2)某种氢氧燃料电池的装置如图2所示。
下列说法正确的是_______ (填字母)。
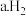 在负极发生反应
在负极发生反应  发生还原反应
发生还原反应
(1)某原电池实验装置如图1。
 片作
片作②
 片上的电极反应为
片上的电极反应为③能证明化学能转化为电能的实验现象是
(2)某种氢氧燃料电池的装置如图2所示。


下列说法正确的是
 在负极发生反应
在负极发生反应  发生还原反应
发生还原反应
您最近一年使用:0次
解题方法
10 . 为探究 与
与 的反应,小组同学选用两种不同的铁盐进行了如下实验。
的反应,小组同学选用两种不同的铁盐进行了如下实验。
【查阅资料】
ⅰ. 在水溶液中不能稳定存在。
在水溶液中不能稳定存在。
ⅱ.氯化亚铜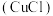 是难溶于水的白色固体。
是难溶于水的白色固体。
【分析解释】
(1)实验Ⅰ中发生反应的离子方程式是_______ 。
(2)为探究实验Ⅱ中白色固体是否为 ,小组同学设计并完成了如图实验。
,小组同学设计并完成了如图实验。 价铜的实验现象是
价铜的实验现象是_______ 。
② 中滴加
中滴加 溶液的目的是
溶液的目的是_______ 。
通过以上实验,证明了实验Ⅱ中白色固体为 。
。
【反思评价】
(3)实验Ⅰ和实验Ⅱ现象不同的原因可能是_______ 。
 与
与 的反应,小组同学选用两种不同的铁盐进行了如下实验。
的反应,小组同学选用两种不同的铁盐进行了如下实验。| 序号 | 实验操作 | 实验现象 |
| Ⅰ | 向盛有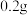 铜片的试管中加入 铜片的试管中加入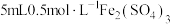 溶液 溶液 | 铜片部分溶解,溶液变为蓝色 |
| Ⅱ | 向盛有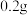 铜片的试管中加入 铜片的试管中加入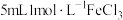 溶液 溶液 | 铜片部分溶解,溶液黄色变浅,铜片表面有白色固体出现 |
ⅰ.
 在水溶液中不能稳定存在。
在水溶液中不能稳定存在。ⅱ.氯化亚铜
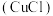 是难溶于水的白色固体。
是难溶于水的白色固体。【分析解释】
(1)实验Ⅰ中发生反应的离子方程式是
(2)为探究实验Ⅱ中白色固体是否为
 ,小组同学设计并完成了如图实验。
,小组同学设计并完成了如图实验。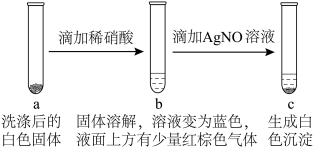
 价铜的实验现象是
价铜的实验现象是②
 中滴加
中滴加 溶液的目的是
溶液的目的是通过以上实验,证明了实验Ⅱ中白色固体为
 。
。【反思评价】
(3)实验Ⅰ和实验Ⅱ现象不同的原因可能是
您最近一年使用:0次