1 . 烟气脱硝技术是环境科学研究的热点。实验室模拟臭氧深度氧化锅炉废气中的NO为 并进一步回收含氮产品的示意图如图。深度氧化器中发生的反应有:
并进一步回收含氮产品的示意图如图。深度氧化器中发生的反应有: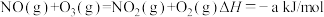
ii.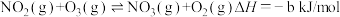
iii.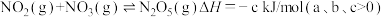
(1)NO被 深度氧化,补全热化学方程式:
深度氧化,补全热化学方程式:
___________ kJ/mol。
(2)80℃、NO初始浓度为200ppm,不同反应时间时深度氧化器中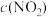 随
随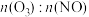 的变化如图所示(反应过程中检测到
的变化如图所示(反应过程中检测到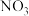 浓度极低)。由图像可以判断:反应速率vⅰ>vⅱ,做出该判断的证据是
浓度极低)。由图像可以判断:反应速率vⅰ>vⅱ,做出该判断的证据是_______ 。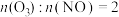 时,不同温度下
时,不同温度下 的浓度随时间变化曲线。
的浓度随时间变化曲线。 浓度不同的原因
浓度不同的原因___________ 。
②结合下图分析,100℃时2s后图中 浓度逐渐下降的可能原因
浓度逐渐下降的可能原因___________ 。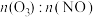 较高时,导致烟气中剩余
较高时,导致烟气中剩余 造成资源浪费和设备腐蚀,综合以上实验数据,常压下,
造成资源浪费和设备腐蚀,综合以上实验数据,常压下, 深度氧化NO的条件应选择
深度氧化NO的条件应选择___________ (填字母)。
A.80℃ B.100℃ C.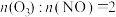 D.
D.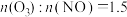
该条件下,烟气中含氮量达到排放标准所需深度氧化时间仍较长,提出解决这一问题可采取的措施及目的___________ 。
(5)深度氧化后的烟气通过吸收器完全转化为硝酸盐产品,产品浓度的测定方法如下。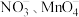 的还原产物分别是NO、
的还原产物分别是NO、 。产品中
。产品中 的物质的量浓度为
的物质的量浓度为_________ mol/L。
 并进一步回收含氮产品的示意图如图。深度氧化器中发生的反应有:
并进一步回收含氮产品的示意图如图。深度氧化器中发生的反应有: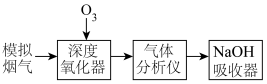
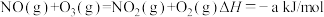
ii.
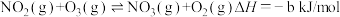
iii.
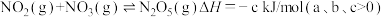
(1)NO被
 深度氧化,补全热化学方程式:
深度氧化,补全热化学方程式:
(2)80℃、NO初始浓度为200ppm,不同反应时间时深度氧化器中
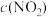 随
随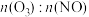 的变化如图所示(反应过程中检测到
的变化如图所示(反应过程中检测到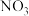 浓度极低)。由图像可以判断:反应速率vⅰ>vⅱ,做出该判断的证据是
浓度极低)。由图像可以判断:反应速率vⅰ>vⅱ,做出该判断的证据是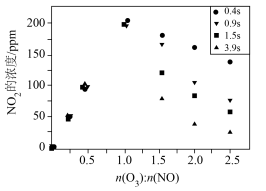
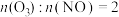 时,不同温度下
时,不同温度下 的浓度随时间变化曲线。
的浓度随时间变化曲线。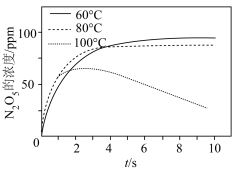
 浓度不同的原因
浓度不同的原因②结合下图分析,100℃时2s后图中
 浓度逐渐下降的可能原因
浓度逐渐下降的可能原因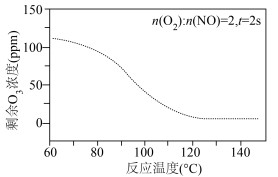
 较高时,导致烟气中剩余
较高时,导致烟气中剩余 造成资源浪费和设备腐蚀,综合以上实验数据,常压下,
造成资源浪费和设备腐蚀,综合以上实验数据,常压下, 深度氧化NO的条件应选择
深度氧化NO的条件应选择A.80℃ B.100℃ C.
 D.
D.
该条件下,烟气中含氮量达到排放标准所需深度氧化时间仍较长,提出解决这一问题可采取的措施及目的
(5)深度氧化后的烟气通过吸收器完全转化为硝酸盐产品,产品浓度的测定方法如下。
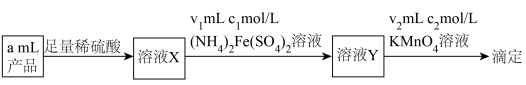
 的还原产物分别是NO、
的还原产物分别是NO、 。产品中
。产品中 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
名校
解题方法
2 . 一种环状高分子P3的合成路线如下:___________ 。
(2)B→C的反应类型是___________ 。
(3)D生成 的反应条件是
的反应条件是___________ 。
(4)上述流程中生成F的反应为酯化反应,则该反应的化学方程式是___________ 。
(5)单体Ⅱ的结构简式是___________ 。
(6)下列说法正确的是___________ (填字母)
b.P3可能的结构如上图所示
c.P2→P3的过程中有可能得到线型高分子
d.碱性条件下,P3可能彻底水解成小分子物质
(7)已知: ;;Q(C6H11NO)是用于合成单体I的中间体。下图是以苯酚为原料合成Q的流程,M→N的化学方程式是
;;Q(C6H11NO)是用于合成单体I的中间体。下图是以苯酚为原料合成Q的流程,M→N的化学方程式是___________ 。

已知:①P2的结构为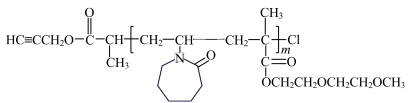
②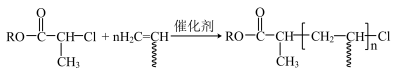 (
( 表示取代基)
表示取代基)
③RCl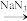 RN3
RN3
(2)B→C的反应类型是
(3)D生成
 的反应条件是
的反应条件是(4)上述流程中生成F的反应为酯化反应,则该反应的化学方程式是
(5)单体Ⅱ的结构简式是
(6)下列说法正确的是
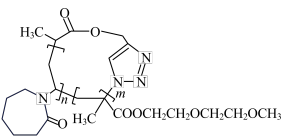
b.P3可能的结构如上图所示
c.P2→P3的过程中有可能得到线型高分子
d.碱性条件下,P3可能彻底水解成小分子物质
(7)已知:
 ;;Q(C6H11NO)是用于合成单体I的中间体。下图是以苯酚为原料合成Q的流程,M→N的化学方程式是
;;Q(C6H11NO)是用于合成单体I的中间体。下图是以苯酚为原料合成Q的流程,M→N的化学方程式是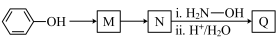
您最近一年使用:0次
名校
3 .  催化重整的反应为:①
催化重整的反应为:①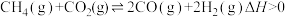 。工业上将恒定组成的
。工业上将恒定组成的 、
、 混合气体,以恒定流速通过含催化剂的反应器。并在反应器出口检测反应后剩余
混合气体,以恒定流速通过含催化剂的反应器。并在反应器出口检测反应后剩余 的含量,以计算
的含量,以计算 的瞬时转化率Ra。
的瞬时转化率Ra。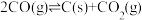 ②,是导致催化剂失活的主要原因。实验测得数据如图。下列分析正确的是
②,是导致催化剂失活的主要原因。实验测得数据如图。下列分析正确的是
 催化重整的反应为:①
催化重整的反应为:①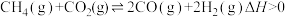 。工业上将恒定组成的
。工业上将恒定组成的 、
、 混合气体,以恒定流速通过含催化剂的反应器。并在反应器出口检测反应后剩余
混合气体,以恒定流速通过含催化剂的反应器。并在反应器出口检测反应后剩余 的含量,以计算
的含量,以计算 的瞬时转化率Ra。
的瞬时转化率Ra。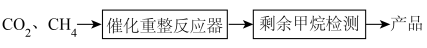
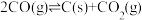 ②,是导致催化剂失活的主要原因。实验测得数据如图。下列分析正确的是
②,是导致催化剂失活的主要原因。实验测得数据如图。下列分析正确的是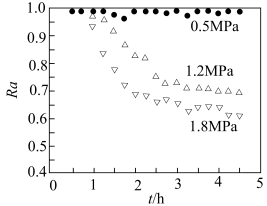
| A.压强越大,Ra降低越快,其主要原因是反应①平衡逆向移动 |
| B.保持其他条件不变,适当降低投料比n(CO2):n(CH4),可减缓Ra的衰减 |
C.研究表明“通入适量 有利于重整反应”,因为 有利于重整反应”,因为 能与C反应并放出热量 能与C反应并放出热量 |
D.初始物质浓度 与流出物质浓度c一定满足: 与流出物质浓度c一定满足: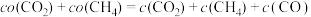 |
您最近一年使用:0次
名校
解题方法
4 . 下列实验不能达到实验目的的是
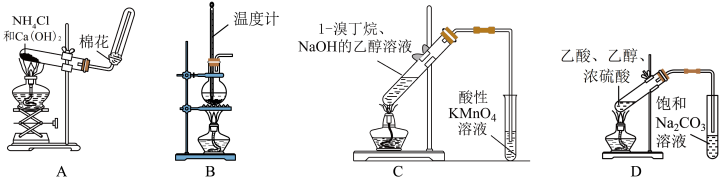
| A.实验室制取氨气 | B.实验室制备乙烯 |
| C.验证1-溴丁烷发生消去反应 | D.实验室制乙酸乙酯 |
您最近一年使用:0次
5 . 在处理NO废气的过程中,催化剂 会逐渐失活变为
会逐渐失活变为 。
。
某小组为解决这一问题,实验研究 和
和 之间的相互转化。
之间的相互转化。
资料:i.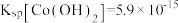 ;
;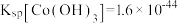 。
。
ii.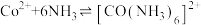
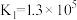 ;
;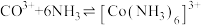
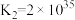 。
。
iii. 和
和 在酸性条件下均能生成
在酸性条件下均能生成 。
。
(1)探 的还原性
的还原性
实验I 粉红色的 溶液或
溶液或 溶液在空气中久置,无明显变化。
溶液在空气中久置,无明显变化。
实验Ⅱ 向 溶液中滴入2滴酸性
溶液中滴入2滴酸性 溶液,无明显变化。
溶液,无明显变化。
实验Ⅲ 按如图装置进行实验,观察到电压表指针偏转。 可以被酸性
可以被酸性 溶液氧化。乙同学补充实验IV,
溶液氧化。乙同学补充实验IV,_______ (补全实验操作及现象),否定了该观点。
②探究碱性条件下 的还原性,进行实验。
的还原性,进行实验。_______ 。
③根据氧化还原反应规律解释还原性 :
: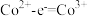 在碱性条件下,
在碱性条件下, 与
与 、
、 反应,使
反应,使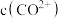 和
和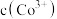 均降低,但
均降低,但_______ 降低的程度更大,还原剂的还原性增强。
(2)探究 的氧化性
的氧化性
①根据实验Ⅲ和IV推测氧化性: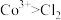 ,设计实验证明:向V中得到的棕褐色沉淀中,
,设计实验证明:向V中得到的棕褐色沉淀中,_______ (补全实验操作及现象),反应方程式为_______ 。
②向V中得到的棕褐色沉淀中,滴加 溶液,加入催化剂,产生无色气泡,该气体是
溶液,加入催化剂,产生无色气泡,该气体是_______ 。
(3)催化剂 的失活与再生
的失活与再生
①结合数据解释 能被氧化为
能被氧化为 而失活的原因:
而失活的原因:_______ 。
②根据以上实验,设计物质转化流程图 实现 的再生:
的再生:_______ 。示例:
 会逐渐失活变为
会逐渐失活变为 。
。某小组为解决这一问题,实验研究
 和
和 之间的相互转化。
之间的相互转化。资料:i.
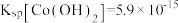 ;
;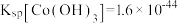 。
。ii.
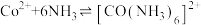
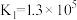 ;
;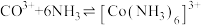
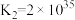 。
。iii.
 和
和 在酸性条件下均能生成
在酸性条件下均能生成 。
。(1)探
 的还原性
的还原性实验I 粉红色的
 溶液或
溶液或 溶液在空气中久置,无明显变化。
溶液在空气中久置,无明显变化。实验Ⅱ 向
 溶液中滴入2滴酸性
溶液中滴入2滴酸性 溶液,无明显变化。
溶液,无明显变化。实验Ⅲ 按如图装置进行实验,观察到电压表指针偏转。
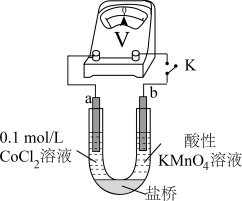
 可以被酸性
可以被酸性 溶液氧化。乙同学补充实验IV,
溶液氧化。乙同学补充实验IV,②探究碱性条件下
 的还原性,进行实验。
的还原性,进行实验。实验V: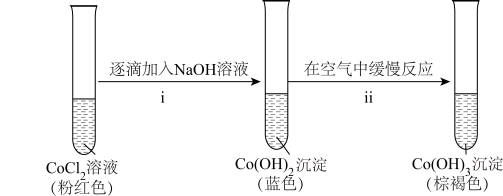
③根据氧化还原反应规律解释还原性
 :
: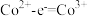 在碱性条件下,
在碱性条件下, 与
与 、
、 反应,使
反应,使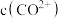 和
和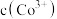 均降低,但
均降低,但(2)探究
 的氧化性
的氧化性①根据实验Ⅲ和IV推测氧化性:
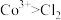 ,设计实验证明:向V中得到的棕褐色沉淀中,
,设计实验证明:向V中得到的棕褐色沉淀中,②向V中得到的棕褐色沉淀中,滴加
 溶液,加入催化剂,产生无色气泡,该气体是
溶液,加入催化剂,产生无色气泡,该气体是(3)催化剂
 的失活与再生
的失活与再生①结合数据解释
 能被氧化为
能被氧化为 而失活的原因:
而失活的原因:②根据以上实验,设计物质转化
 的再生:
的再生:
您最近一年使用:0次
名校
解题方法
6 . 一种锂离子电池的工作原理: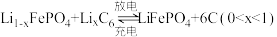 。从废旧电池再生
。从废旧电池再生 的一种流程如下,
的一种流程如下,
负极: 。
。
正极:_______ 。
(2)为保证正极材料在空气中充分反应,可采取的措施是_______ (答一条即可)。
(3)向浸出液中加入氨水调节溶液pH,有沉淀生成。pH对沉淀中Fe和P的物质的量之比 的影响如图所示。
的影响如图所示。 分别与
分别与 、
、 、
、 形成的化合物均难溶于水。
形成的化合物均难溶于水。
ii. 体系中含磷粒子的物质的量分数与pH的关系如图所示。
体系中含磷粒子的物质的量分数与pH的关系如图所示。 沉淀的最佳
沉淀的最佳 在
在_______ 左右。
②当 时,沉淀中一定有的含铁物质是
时,沉淀中一定有的含铁物质是 和
和_______ (填化学式)。
③若向 的浊液中继续加入氨水至
的浊液中继续加入氨水至 ,会导致
,会导致 的值增大,主要反应的化学方程式是
的值增大,主要反应的化学方程式是_______ 。
(4)下列关于该流程的说法正确的是_______(填序号)。
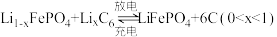 。从废旧电池再生
。从废旧电池再生 的一种流程如下,
的一种流程如下,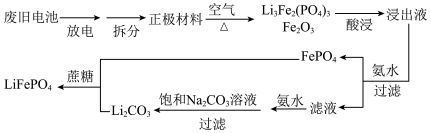
负极:
 。
。正极:
(2)为保证正极材料在空气中充分反应,可采取的措施是
(3)向浸出液中加入氨水调节溶液pH,有沉淀生成。pH对沉淀中Fe和P的物质的量之比
 的影响如图所示。
的影响如图所示。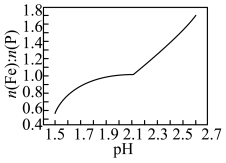
 分别与
分别与 、
、 、
、 形成的化合物均难溶于水。
形成的化合物均难溶于水。ii.
 体系中含磷粒子的物质的量分数与pH的关系如图所示。
体系中含磷粒子的物质的量分数与pH的关系如图所示。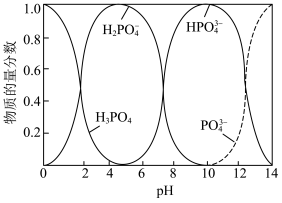
 沉淀的最佳
沉淀的最佳 在
在②当
 时,沉淀中一定有的含铁物质是
时,沉淀中一定有的含铁物质是 和
和③若向
 的浊液中继续加入氨水至
的浊液中继续加入氨水至 ,会导致
,会导致 的值增大,主要反应的化学方程式是
的值增大,主要反应的化学方程式是(4)下列关于该流程的说法正确的是_______(填序号)。
A.正极材料在空气中加热,理论上生成的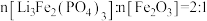 |
B.当浸出液的pH从0增大为2时,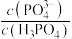 的值增大了 的值增大了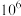 倍 倍 |
C.向滤液中加入氨水,可减少饱和 溶液的用量 溶液的用量 |
D.由 和 和 再生 再生 时,所加的蔗糖作氧化剂 时,所加的蔗糖作氧化剂 |
您最近一年使用:0次
名校
解题方法
7 . 溴及其化合物广泛应用于医药、农药和阻燃剂等生产中。一种利用空气吹出法从海水中提取溴的工艺流程如下。
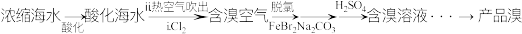
已知:i.与 反应时,
反应时, 转化为
转化为 和
和 。ii.
。ii.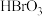 为强酸。下列说法
为强酸。下列说法不正确 的是
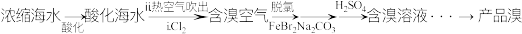
已知:i.与
 反应时,
反应时, 转化为
转化为 和
和 。ii.
。ii.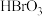 为强酸。下列说法
为强酸。下列说法A.酸化海水通入 提取溴的反应: 提取溴的反应: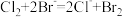 |
B.脱氯过程 和 和 均具有脱氯作用 均具有脱氯作用 |
C.用 溶液吸收足量 溶液吸收足量 蒸气后,所得产物中的含碳粒子主要是 蒸气后,所得产物中的含碳粒子主要是 |
D. 酸化后重新得到 酸化后重新得到 的反应: 的反应: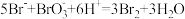 |
您最近一年使用:0次
名校
解题方法
8 . 关于离子化合物 和
和 ,下列说法
,下列说法不正确 的是
 和
和 ,下列说法
,下列说法A. 、 、 中均含有非极性共价键 中均含有非极性共价键 |
B. 、 、 中阴、阳离子个数比均为 中阴、阳离子个数比均为 |
C. 、 、 与水反应时水均不作氧化剂或还原剂 与水反应时水均不作氧化剂或还原剂 |
D.相同物质的量的 和 和 与足量的水反应,所得气体的物质的量 与足量的水反应,所得气体的物质的量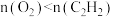 |
您最近一年使用:0次
解题方法
9 . Cu(Ⅱ)可形成多种配合物,呈现出多样化的性质和用途。
(1)向盛有硫酸铜水溶液的试管中加入少量氨水生成蓝色沉淀,继续加入过量氨水,得到深蓝色透明溶液,最后向该溶液中加入一定量的乙醇,析出 晶体。
晶体。
①产生蓝色沉淀的离子方程式是___________ 。
② 在水中电离的方程式是
在水中电离的方程式是___________ 。
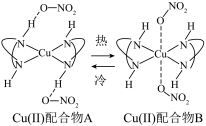
(2)如下图所示, Cu(Ⅱ)配合物A和B可发生配位构型的转变,该转变可带来颜色的变化,因此可用作热致变色材料,在温度传感器、变色涂料等领域应用广泛。 的价层电子排布式为
的价层电子排布式为___________ 。
② 、
、 、
、 的第一电离能由大到小顺序为
的第一电离能由大到小顺序为___________ 。
③A中氮原子与其它原子(或离子)之间存在的作用力类型有___________ ,氢原子与其它原子之间存在的作用力类型有___________ 。
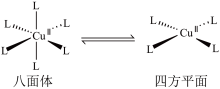
④已知:当Cu(Ⅱ)配合物A和B配位构型由八面体转变为四方平面时,吸收光谱蓝移,配合物颜色紫色变为橙色。___________ 。
(3)已知:
①
②蓝色溶液与黄色溶液混合为绿色溶液,在 溶液中加入
溶液中加入 浓溶液,颜色从蓝色变为绿色,请结合化学用语解释原因
浓溶液,颜色从蓝色变为绿色,请结合化学用语解释原因___________ 。
(4)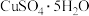 脱水过程中部分中间体的结构示意图如下图。
脱水过程中部分中间体的结构示意图如下图。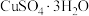 写成配合物形式为
写成配合物形式为___________ ,其转化为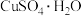 过程中,破坏的分子间作用力是
过程中,破坏的分子间作用力是___________ 。
(1)向盛有硫酸铜水溶液的试管中加入少量氨水生成蓝色沉淀,继续加入过量氨水,得到深蓝色透明溶液,最后向该溶液中加入一定量的乙醇,析出
 晶体。
晶体。①产生蓝色沉淀的离子方程式是
②
 在水中电离的方程式是
在水中电离的方程式是(2)如下图所示, Cu(Ⅱ)配合物A和B可发生配位构型的转变,该转变可带来颜色的变化,因此可用作热致变色材料,在温度传感器、变色涂料等领域应用广泛。
 的价层电子排布式为
的价层电子排布式为②
 、
、 、
、 的第一电离能由大到小顺序为
的第一电离能由大到小顺序为③A中氮原子与其它原子(或离子)之间存在的作用力类型有
④已知:当Cu(Ⅱ)配合物A和B配位构型由八面体转变为四方平面时,吸收光谱蓝移,配合物颜色紫色变为橙色。
(3)已知:
①
| 物质 | 颜色 |
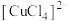 | 黄色 |
 | 蓝色 |
 溶液中加入
溶液中加入 浓溶液,颜色从蓝色变为绿色,请结合化学用语解释原因
浓溶液,颜色从蓝色变为绿色,请结合化学用语解释原因(4)
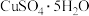 脱水过程中部分中间体的结构示意图如下图。
脱水过程中部分中间体的结构示意图如下图。
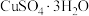 写成配合物形式为
写成配合物形式为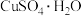 过程中,破坏的分子间作用力是
过程中,破坏的分子间作用力是
您最近一年使用:0次
名校
10 . 一种抗过敏药物中间体 的合成路线如图所示。
的合成路线如图所示。
(1) 的化学方程式是
的化学方程式是_______ 。
(2) 的反应类型是
的反应类型是_______ 。
(3) 与
与 发生取代反应生成
发生取代反应生成 (含有3个苯环且不含硫原子)。已知
(含有3个苯环且不含硫原子)。已知 中断开
中断开 键,则
键,则 中断开
中断开_______ (填“ 键”或“
键”或“ 键”)。
键”)。
(4) 的官能团有
的官能团有_______ 。
(5) 涉及的反应过程如图。
涉及的反应过程如图。 的结构简式。中间产物2:
的结构简式。中间产物2:_______ ,D:_______ 。
(6) 的结构简式是
的结构简式是_______ 。
(7)下列说法正确的是_______ )。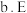 中存在手性碳原子
中存在手性碳原子
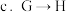 反应中为减少副反应的发生,应向过量
反应中为减少副反应的发生,应向过量 中滴加试剂
中滴加试剂
 的合成路线如图所示。
的合成路线如图所示。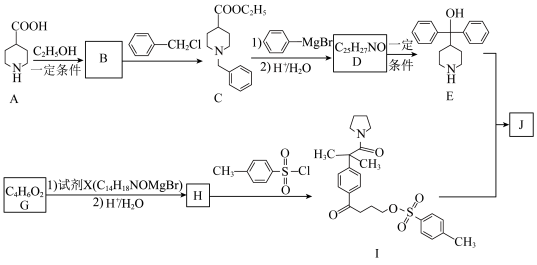
已知:ⅰ.酯或酮中的碳氧双键能与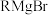 发生加成反应:
发生加成反应: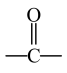 +RMgBr
+RMgBr
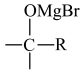

(1)
 的化学方程式是
的化学方程式是(2)
 的反应类型是
的反应类型是(3)
 与
与 发生取代反应生成
发生取代反应生成 (含有3个苯环且不含硫原子)。已知
(含有3个苯环且不含硫原子)。已知 中断开
中断开 键,则
键,则 中断开
中断开 键”或“
键”或“ 键”)。
键”)。(4)
 的官能团有
的官能团有(5)
 涉及的反应过程如图。
涉及的反应过程如图。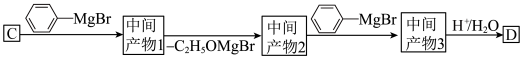
 的结构简式。中间产物2:
的结构简式。中间产物2:(6)
 的结构简式是
的结构简式是(7)下列说法正确的是
 中
中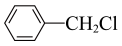 的作用是保护
的作用是保护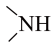
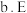 中存在手性碳原子
中存在手性碳原子 反应中为减少副反应的发生,应向过量
反应中为减少副反应的发生,应向过量 中滴加试剂
中滴加试剂
您最近一年使用:0次
2024-05-29更新
|
200次组卷
|
2卷引用:北京师范大学附属中学2023-2024学年高三下学期统练2化学试题



