23-24高三下·陕西西安·阶段练习
解题方法
1 . CdS、ZnS等硫化物与TiO2、SnO2、ZnO等进行复合,可以得到性能很好的复合半导体光催化剂。回答下列问题:
(1)Sn与C同主族,基态Sn原子的价层电子排布式为_______ ,基态Ti原子核外电子有_______ 种空间运动状态, 核外未成对电子数为
核外未成对电子数为_______ ,ZnS、ZnO中各元素的电负性由大到小的顺序为_______ 。
(2)许多具有—C═N—结构的分子及其硼配合物是较好的荧光材料,在光学探针、有机发光二极管等领域受到广泛关注,某两种含这种结构的分子如图1、图2所示。_______ ;图2中N原子会和B原子形成配位键,成键时_______ (填元素符号)原子提供空轨道。
(3)N、O、F三种元素的第一电离能由大到小的顺序为_______ (填元素符号),解释其原因:_______ 。
(4)钾冰晶石型晶体是一类新型的无机闪烁体,在核安全以及国土安全检查方面有重要的应用。如图是一种钾冰晶石型闪烁体的晶胞结构,属于立方晶系,其中A位是 、B位是
、B位是 、R位是正三价的Y(钇),X位是
、R位是正三价的Y(钇),X位是 。
。_______ 。
②若晶胞参数为anm,该晶体的密度为_______ g (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。
(1)Sn与C同主族,基态Sn原子的价层电子排布式为
 核外未成对电子数为
核外未成对电子数为(2)许多具有—C═N—结构的分子及其硼配合物是较好的荧光材料,在光学探针、有机发光二极管等领域受到广泛关注,某两种含这种结构的分子如图1、图2所示。

(3)N、O、F三种元素的第一电离能由大到小的顺序为
(4)钾冰晶石型晶体是一类新型的无机闪烁体,在核安全以及国土安全检查方面有重要的应用。如图是一种钾冰晶石型闪烁体的晶胞结构,属于立方晶系,其中A位是
 、B位是
、B位是 、R位是正三价的Y(钇),X位是
、R位是正三价的Y(钇),X位是 。
。
②若晶胞参数为anm,该晶体的密度为
 (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。
您最近一年使用:0次
23-24高三下·陕西西安·阶段练习
2 . X、Y、Z、W为原子序数依次增大的短周期主族元素,原子序数之和为37。四种元素所形成的常见单质有三种在常温下为气体,在一定条件下,Z与X、Y、W均能形成原子个数比为1∶1的离子化合物。下列说法错误的是
| A.Y的简单氢化物在同主族元素中稳定性最强 |
| B.Y、Z所形成的物质中可能含不同种化学键 |
| C.简单离子半径:W>Z>Y>X |
| D.由X、Y两种元素组成的含18电子的分子能使酸性KMnO4溶液褪色 |
您最近一年使用:0次
23-24高三下·陕西西安·阶段练习
解题方法
3 . 下列实验操作和实验分析均正确的是
| 选项 | 实验操作 | 实验分析 |
| A | 向2mL0.1mol·L-1NaBr溶液中滴加2滴0.1mol·L-1AgNO3溶液,产生淡黄色沉淀,再滴加2滴0.1mol·L-1Na2S溶液,出现黑色沉淀 | 该实验表明Ag2S的溶解度比AgBr的更小 |
| B | 用干燥洁净的pH试纸测定0.1mol·L-1的不同盐溶液的pH,如NaCl、NH4Cl、CH3COONa、NaClO的水溶液 | 该实验可以发现不同盐溶液呈现不同的酸碱性 |
| C | 做中和反应反应热的测定实验时,将酸溶液缓缓滴入碱溶液中,用温度计测定反应的最高温度 | 该实验可以同酸碱中和滴定实验一起完成 |
| D | 向蔗糖溶液中加入3~5滴稀硫酸,将混合液煮沸几分钟,冷却,向冷却液中加入银氨溶液,水浴加热,未出现银镜 | 该实验可表明蔗糖没有水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
23-24高三下·陕西西安·阶段练习
解题方法
4 . 氢气在精细化工、航空航天等方面有着广泛的应用。我国开发了最新的甲醇催化制氢技术,发生反应: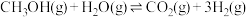
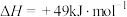 ,其反应原理如图所示:
,其反应原理如图所示:
(1)若第I步反应生成1molH2,放出热量QkJ,则第Ⅱ步反应的热化学方程式为_______ 。
(2)一定温度范围内,在两种不同催化剂a、b存在时,甲醇制氢反应的速率常数(k)与温度(T)存在如图变化关系(已知:活化能越大,相应的速率常数越小)。_______ E(b)(填“>”“=”或“<”)。
(3)已知上述制氢过程中存在副反应: 。将n(CH3OH);n(H2O):n(N2)=1:1:3的混合气体充入某恒温、恒容的密闭容器中(已知:N2不参与反应),初始压强为100kPa,发生甲醇制氢反应和副反应,达平衡时容器内的压强为132kPa,CO2分压为12kPa。
。将n(CH3OH);n(H2O):n(N2)=1:1:3的混合气体充入某恒温、恒容的密闭容器中(已知:N2不参与反应),初始压强为100kPa,发生甲醇制氢反应和副反应,达平衡时容器内的压强为132kPa,CO2分压为12kPa。
①H2O的平衡转化率为_______ 。
②用分压表示甲醇制氢反应的平衡常数
_______  (列出计算式即可)。
(列出计算式即可)。
③若初始时容器中未通入N2,n(CH3OH);n(H2O)=1:1,初始压强仍为100kPa,则H2O的平衡转化率_______ (填“增大”“减小”或“不变”),原因是_______ 。
(4)甲醇在三种催化剂(i、ii、iii)上的电氧化过程同时存在反应①( )和反应②(CH3OH→HCOOH)两种电极反应,各自决速步的活化能如下表。
)和反应②(CH3OH→HCOOH)两种电极反应,各自决速步的活化能如下表。
电氧化过程中甲醇应在_______ (填“阳极”或“阴极”)发生反应,三种催化剂中对反应①的催化活性最强的是_______ (填“i”“ii”或“iii”,下同),对反应①和反应②的选择性都较低的催化剂是_______ 。
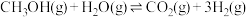
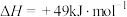 ,其反应原理如图所示:
,其反应原理如图所示:
(1)若第I步反应生成1molH2,放出热量QkJ,则第Ⅱ步反应的热化学方程式为
(2)一定温度范围内,在两种不同催化剂a、b存在时,甲醇制氢反应的速率常数(k)与温度(T)存在如图变化关系(已知:活化能越大,相应的速率常数越小)。

(3)已知上述制氢过程中存在副反应:
 。将n(CH3OH);n(H2O):n(N2)=1:1:3的混合气体充入某恒温、恒容的密闭容器中(已知:N2不参与反应),初始压强为100kPa,发生甲醇制氢反应和副反应,达平衡时容器内的压强为132kPa,CO2分压为12kPa。
。将n(CH3OH);n(H2O):n(N2)=1:1:3的混合气体充入某恒温、恒容的密闭容器中(已知:N2不参与反应),初始压强为100kPa,发生甲醇制氢反应和副反应,达平衡时容器内的压强为132kPa,CO2分压为12kPa。①H2O的平衡转化率为
②用分压表示甲醇制氢反应的平衡常数

 (列出计算式即可)。
(列出计算式即可)。③若初始时容器中未通入N2,n(CH3OH);n(H2O)=1:1,初始压强仍为100kPa,则H2O的平衡转化率
(4)甲醇在三种催化剂(i、ii、iii)上的电氧化过程同时存在反应①(
 )和反应②(CH3OH→HCOOH)两种电极反应,各自决速步的活化能如下表。
)和反应②(CH3OH→HCOOH)两种电极反应,各自决速步的活化能如下表。| 反应序号 | 催化剂i决速步活化能/eV | 催化剂ii决速步活化能/eV | 催化剂iii决速步活化能/eV |
| 反应① | 0.58 | 0.04 | 0.35 |
| 反应② | 0.02 | 0.56 | 0.32 |
您最近一年使用:0次
23-24高三下·陕西西安·阶段练习
5 . SrCO3可用于生产纳米材料,常温下,以天青石矿(主要成分为SrSO4,含少量CaCO3、MgCO3、ZnCO3、Al2O3、Fe2O3及FeO等杂质)为原料制备SrCO3的流程如下: 、
、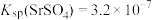 。
。
②该工艺条件下,有关金属离子开始沉淀和完全沉淀以及部分离子的氢氧化物开始溶解的pH见下表:
(1)“盐浸”时,为了提高锶的浸取率可以采取的措施是_______ (写一条即可),采用适当浓度Na2CO3溶液盐浸的目的是_______ (用离子方程式表示)。
(2)“酸浸”时加入H2O2的目的是_______ (用离子方程式表示)。
(3)“第一次调pH”时,需要调pH的范围是_______ ,当Al3+刚好完全沉淀时,溶液中Fe3+的浓度为_______ mol·L-1。
(4)“第三次调pH至12.5”后,需对反应液在95℃水浴中加热,并趁热过滤出“滤渣3”,趁热过滤的目的是_______ 。
(5)“沉锶”时,主要反应的离子方程式为_______ 。
(6)“系列操作”包括_______ (填操作名称)。

 、
、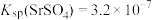 。
。②该工艺条件下,有关金属离子开始沉淀和完全沉淀以及部分离子的氢氧化物开始溶解的pH见下表:
| 金属离子 | Fe3+ | Al3+ | Zn2+ | Mg2+ |
| 开始沉淀的pH(c=1×10-2mol·L-1) | 2.1 | 4.2 | 6.0 | 10.4 |
| 完全沉淀的pH(c=1×10-5mol·L-1) | 4.1 | 5.2 | 8.0 | 12.4 |
| 氢氧化物沉淀开始溶解的pH | - | 7.8 | 10.05 | - |
(1)“盐浸”时,为了提高锶的浸取率可以采取的措施是
(2)“酸浸”时加入H2O2的目的是
(3)“第一次调pH”时,需要调pH的范围是
(4)“第三次调pH至12.5”后,需对反应液在95℃水浴中加热,并趁热过滤出“滤渣3”,趁热过滤的目的是
(5)“沉锶”时,主要反应的离子方程式为
(6)“系列操作”包括
您最近一年使用:0次
23-24高三下·陕西西安·阶段练习
解题方法
6 . 常温下,用0.1000mol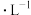 NaOH溶液滴定50.00mL0.1000mol
NaOH溶液滴定50.00mL0.1000mol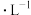
 溶液,滴定曲线如图所示。下列说法错误的是
溶液,滴定曲线如图所示。下列说法错误的是
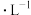 NaOH溶液滴定50.00mL0.1000mol
NaOH溶液滴定50.00mL0.1000mol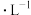
 溶液,滴定曲线如图所示。下列说法错误的是
溶液,滴定曲线如图所示。下列说法错误的是
| A.b点的产物为NaH2PO4,指示滴定至c点时,可使用酚酞作指示剂 |
B.b点溶液中由水电离出的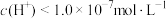 |
C.当V(NaOH)=25.00mL时,溶液中: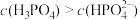 |
D.c点溶液中: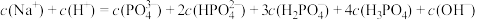 |
您最近一年使用:0次
23-24高三下·陕西西安·阶段练习
解题方法
7 . 氨气是一种无碳能源,是燃料电池研究的重点。如图是两种不同介质条件下氨燃料电池的工作原理示意图。下列说法正确的是

| A.两种条件下M电极的电势均高于N电极 |
B.两种条件下电池的负极反应式均为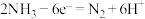 |
| C.若将该电池用于金属表面镀银,则M电极连接镀件 |
| D.当有6mol电子发生转移时,理论上消耗氨气的体积为44.8L |
您最近一年使用:0次
解题方法
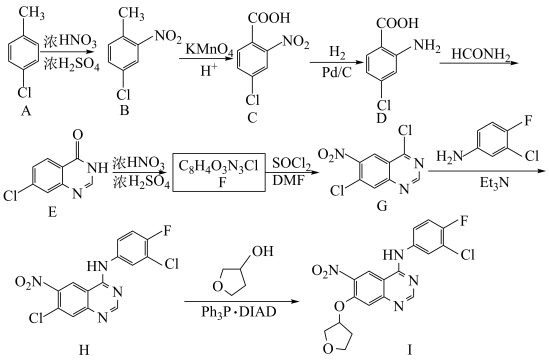
8 . 化合物I是制备抗肿瘤药物阿法替尼的重要中间体,化合物I的一种合成路线如图。
已知:RCH=NH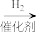 RCH2NH2
RCH2NH2
回答下列问题:
(1)C中含氧官能团的名称是_______ 。
(2)A的化学名称为_______ 。
(3)F的结构简式为_______ ,H→I的反应类型为_______ 。
(4)G→H的化学方程式为_______ 。
(5) 有多种同分异构体,符合下列条件的有
有多种同分异构体,符合下列条件的有_______ 种(不考虑立体异构),其中核磁共振氢谱有3组峰,其峰面积比为6:1:1的结构简式为_______ (写出一种)。
a.能发生银镜反应 b.不含醚键

已知:RCH=NH
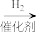 RCH2NH2
RCH2NH2回答下列问题:
(1)C中含氧官能团的名称是
(2)A的化学名称为
(3)F的结构简式为
(4)G→H的化学方程式为
(5)
 有多种同分异构体,符合下列条件的有
有多种同分异构体,符合下列条件的有a.能发生银镜反应 b.不含醚键
您最近一年使用:0次
解题方法
9 . 已知:
①H2O(g)=H2(g)+ O2(g) △H=+241.8kJ/mol
O2(g) △H=+241.8kJ/mol
②C(s)+ O2(g)=CO(g) △H=-110.5kJ/mol
O2(g)=CO(g) △H=-110.5kJ/mol
③C(s)+O2(g)=CO2(g) △H=-393.5kJ/mol
请填写下列空白。
(1)上述反应中属于吸热反应的是_______ (填序号)。
(2)表示C的燃烧热的热化学方程式为_______ (填序号)。
(3)写出CO燃烧的热化学方程式:_______ 。
(4)已知:H2(g)+Cl2(g)=2HCl(g) △H=-184.6kJ/mol,则HCl(g)= H2(g)+
H2(g)+ Cl2(g)的△H=
Cl2(g)的△H=_______ 。
(5)2008年北京奥运会“祥云”火炬的燃料是丙烷(C3H8),1996年亚特兰大奧运会火炬的燃料是丙烯(C3H6)。丙烷脱氢可得到丙烯。已知:
①C3H8(g)=CH4(g)+C2H2(g)+H2(g) △H1=+255.7kJ/mol
②C3H6(g)=CH4(g)+C2H2(g) △H2=+131.5kJ/mol
计算C3H8(g)=C3H6(g)+H2(g)的△H=_______ 。
①H2O(g)=H2(g)+
 O2(g) △H=+241.8kJ/mol
O2(g) △H=+241.8kJ/mol②C(s)+
 O2(g)=CO(g) △H=-110.5kJ/mol
O2(g)=CO(g) △H=-110.5kJ/mol③C(s)+O2(g)=CO2(g) △H=-393.5kJ/mol
请填写下列空白。
(1)上述反应中属于吸热反应的是
(2)表示C的燃烧热的热化学方程式为
(3)写出CO燃烧的热化学方程式:
(4)已知:H2(g)+Cl2(g)=2HCl(g) △H=-184.6kJ/mol,则HCl(g)=
 H2(g)+
H2(g)+ Cl2(g)的△H=
Cl2(g)的△H=(5)2008年北京奥运会“祥云”火炬的燃料是丙烷(C3H8),1996年亚特兰大奧运会火炬的燃料是丙烯(C3H6)。丙烷脱氢可得到丙烯。已知:
①C3H8(g)=CH4(g)+C2H2(g)+H2(g) △H1=+255.7kJ/mol
②C3H6(g)=CH4(g)+C2H2(g) △H2=+131.5kJ/mol
计算C3H8(g)=C3H6(g)+H2(g)的△H=
您最近一年使用:0次
解题方法
10 . I.氮及其化合物与人类生产、生活息息相关。回答下列问题:
(1)固氮酶有铁蛋白和钒铁蛋白两种,它们不仅能够催化N2还原成NH3,还能将环境底物乙炔催化还原成乙烯。
①V2+基态时核外电子排布式为_______ 。
②C、N、O三种元素第一电离能从大到小的顺序是_______ 。
③下列说法正确的有_______ 。
A.C2H2、C2H4都是非极性分子 B.碳负离子 呈三角锥形
呈三角锥形
C.NO+电子式为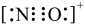 D.NH3沸点比N2高,主要是因为前者是极性分子
D.NH3沸点比N2高,主要是因为前者是极性分子
(2)NaN3可用于汽车安全气囊。写出两种与 互为等电子体的分子或离子
互为等电子体的分子或离子_______ 。
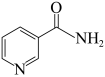
(3)烟酰胺是一种含氮有机物,结构简式如图所示,烟酰胺分子中氮原子的杂化轨道类型有_______ ,1mol该分子中含σ键的数目为_______ 。
Ⅱ.氯化钠是生活中的常用调味品,也是结构化学中研究离子晶体时常用的代表物,其晶胞结构如图所示。

(4)已知在氯化钠晶体中Na+的半径为a pm,Cl-的半径为b pm,它们在晶体中是紧密接触的,则在氯化钠晶体中的空间利用率为_______ (用含a、b的式子表示)。
(5)纳米材料的表面原子占总原子数的比例很大,这是它有许多特殊性质的原因。假设某氯化钠颗粒形状为立方体,边长为氯化钠晶胞的10倍,则该氯化钠颗粒中表面原子占总原子数的百分比为_______ 。
(1)固氮酶有铁蛋白和钒铁蛋白两种,它们不仅能够催化N2还原成NH3,还能将环境底物乙炔催化还原成乙烯。
①V2+基态时核外电子排布式为
②C、N、O三种元素第一电离能从大到小的顺序是
③下列说法正确的有
A.C2H2、C2H4都是非极性分子 B.碳负离子
 呈三角锥形
呈三角锥形C.NO+电子式为
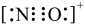 D.NH3沸点比N2高,主要是因为前者是极性分子
D.NH3沸点比N2高,主要是因为前者是极性分子(2)NaN3可用于汽车安全气囊。写出两种与
 互为等电子体的分子或离子
互为等电子体的分子或离子(3)烟酰胺是一种含氮有机物,结构简式如图所示,烟酰胺分子中氮原子的杂化轨道类型有

Ⅱ.氯化钠是生活中的常用调味品,也是结构化学中研究离子晶体时常用的代表物,其晶胞结构如图所示。

(4)已知在氯化钠晶体中Na+的半径为a pm,Cl-的半径为b pm,它们在晶体中是紧密接触的,则在氯化钠晶体中的空间利用率为
(5)纳米材料的表面原子占总原子数的比例很大,这是它有许多特殊性质的原因。假设某氯化钠颗粒形状为立方体,边长为氯化钠晶胞的10倍,则该氯化钠颗粒中表面原子占总原子数的百分比为
您最近一年使用:0次



