1 . 下列设备工作时,将化学能转化为电能的是
|
|
|
|
| A.硅太阳能电池 | B.锂离子电池 | C.太阳能集热器 | D.燃气灶 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 下列反应过程中的能量变化情况符合图像的是
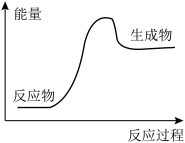
| A.乙醇的燃烧 | B.Ba(OH)2·8H2O与NH4Cl反应 |
| C.镁和盐酸的反应 | D.酸和碱的中和反应 |
您最近一年使用:0次
3 . 完成下列填空。
(1)某学习小组依据氧化还原反应原理: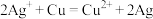 设计成的原电池如图所示。
设计成的原电池如图所示。___________ ;
②负极的电极材料为___________ ;(填化学式)
③正极发生的电极反应___________ ;
④若银电极增重5.4g,外电路转移电子的物质的量___________ mol。
(2)温度一定,在一个2L的恒容密闭容器中,A、B、C三种气体物质的浓度随时间的变化曲线如图所示。根据图中数据,试填写下列空白:___________ 。从开始到平衡时C的反应速率为___________ ,A的转化率为___________ 。
②下列叙述能说明该反应已达到化学平衡状态的是___________ (填序号)。
A.A与C的浓度相等
B.相同时间内消耗3nmolA,同时生成3nmolA
C.相同时间内消耗3nmolA,同时消耗nmolB
D.混合气体的总质量不随时间的变化而变化
E.B的体积分数不再发生变化
F.混合气体的密度不再发生变化
G.混合气体的压强不再发生变化
(1)某学习小组依据氧化还原反应原理:
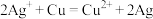 设计成的原电池如图所示。
设计成的原电池如图所示。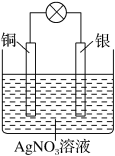
②负极的电极材料为
③正极发生的电极反应
④若银电极增重5.4g,外电路转移电子的物质的量
(2)温度一定,在一个2L的恒容密闭容器中,A、B、C三种气体物质的浓度随时间的变化曲线如图所示。根据图中数据,试填写下列空白:
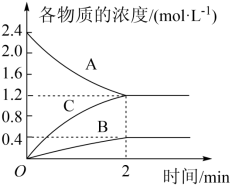
②下列叙述能说明该反应已达到化学平衡状态的是
A.A与C的浓度相等
B.相同时间内消耗3nmolA,同时生成3nmolA
C.相同时间内消耗3nmolA,同时消耗nmolB
D.混合气体的总质量不随时间的变化而变化
E.B的体积分数不再发生变化
F.混合气体的密度不再发生变化
G.混合气体的压强不再发生变化
您最近一年使用:0次
4 . “天津狗不理包子”是天津特色小吃之一,制作“狗不理包子”的主要原料如下:
①猪肉 ②面粉 ③油 ④食盐 ⑤少许味精 ⑥水
下列说法正确的是
(1)富含蛋白质的是①,因此所有蛋白质都不溶于水
(2)富含淀粉的是②,淀粉、纤维素、天然橡胶都是天然有机高分子
(3)通常情况下,油是指植物油,可以使酸性高锰酸钾溶液褪色
(4)水分子内只含极性共价键
(5)人体必需的基本营养物质中不包括:⑤⑥
①猪肉 ②面粉 ③油 ④食盐 ⑤少许味精 ⑥水
下列说法正确的是
(1)富含蛋白质的是①,因此所有蛋白质都不溶于水
(2)富含淀粉的是②,淀粉、纤维素、天然橡胶都是天然有机高分子
(3)通常情况下,油是指植物油,可以使酸性高锰酸钾溶液褪色
(4)水分子内只含极性共价键
(5)人体必需的基本营养物质中不包括:⑤⑥
| A.(2)(3)(4) | B.(1)(2)(3) | C.(3)(4)(5) | D.全部 |
您最近一年使用:0次
5 . 实验室可用干燥的氯气与亚氯酸钠 固体反应来制备
固体反应来制备 ,装置如图所示,已知
,装置如图所示,已知 常温下为黄绿色气体,熔点-56℃,沸点11℃,极易溶于水且不与水反应,高浓度的
常温下为黄绿色气体,熔点-56℃,沸点11℃,极易溶于水且不与水反应,高浓度的 受热时易爆炸,下列说法不正确的是
受热时易爆炸,下列说法不正确的是
 固体反应来制备
固体反应来制备 ,装置如图所示,已知
,装置如图所示,已知 常温下为黄绿色气体,熔点-56℃,沸点11℃,极易溶于水且不与水反应,高浓度的
常温下为黄绿色气体,熔点-56℃,沸点11℃,极易溶于水且不与水反应,高浓度的 受热时易爆炸,下列说法不正确的是
受热时易爆炸,下列说法不正确的是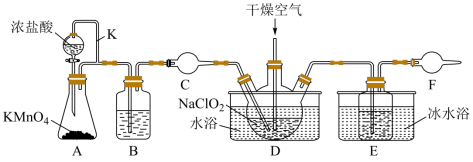
| A.导气管K的作用是平衡气压,保证液体顺利流下 |
| B.C和F中可选用同一种物质 |
C.D中通入一定量的干燥空气,目的主要是防止生成的 浓度过高,发生爆炸 浓度过高,发生爆炸 |
D.D中发生的化学反应中氧化剂与还原剂的物质的量之比为 |
您最近一年使用:0次
6 . 含氮化合物在工农业有着重要的用途。
(1)氨气的发生装置可以选择上图中的A,反应的化学方程式为____________ 。
(2)预收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:a→_________ (按气流方向,用小写字母表示)。
(3)请写出氨气的检验方法:________________ 。
Ⅱ. 经一系列反应可以得到
经一系列反应可以得到 。
。
(4)①中, 和
和 在催化剂作用下反应,其化学方程式是
在催化剂作用下反应,其化学方程式是____________ 。
(5)NO的检验方法是:______________ 。
Ⅲ.研究、 、CO等大气污染气体的处理具有重要现实意义。
、CO等大气污染气体的处理具有重要现实意义。
(6)选择性催化还原技术(SCR)可使NOx与 直接反应,实现无害转化。当NO与
直接反应,实现无害转化。当NO与 的物质的量之比为2∶1时,写出发生反应的化学方程式:
的物质的量之比为2∶1时,写出发生反应的化学方程式:___________ 。
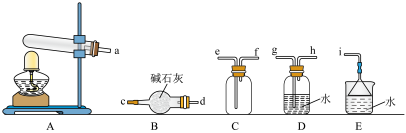
(1)氨气的发生装置可以选择上图中的A,反应的化学方程式为
(2)预收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:a→
(3)请写出氨气的检验方法:
Ⅱ.
 经一系列反应可以得到
经一系列反应可以得到 。
。
(4)①中,
 和
和 在催化剂作用下反应,其化学方程式是
在催化剂作用下反应,其化学方程式是(5)NO的检验方法是:
Ⅲ.研究、
 、CO等大气污染气体的处理具有重要现实意义。
、CO等大气污染气体的处理具有重要现实意义。(6)选择性催化还原技术(SCR)可使NOx与
 直接反应,实现无害转化。当NO与
直接反应,实现无害转化。当NO与 的物质的量之比为2∶1时,写出发生反应的化学方程式:
的物质的量之比为2∶1时,写出发生反应的化学方程式:
您最近一年使用:0次
7 . 下列有关氮及其化合物的说法正确的是
| A.二氧化氮溶于水时,二氧化氮是氧化剂,水是还原剂 |
| B.氨遇到浓盐酸、浓硫酸、浓硝酸都会发生反应,产生白烟 |
| C.久置的浓硝酸颜色略显黄色,那是由于浓硝酸的不稳定性 |
| D.铵盐都不稳定,受热分解都生成NH3 |
您最近一年使用:0次
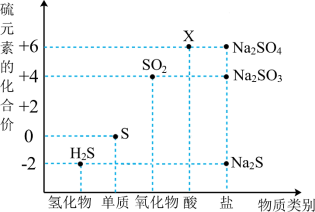
8 . 利用元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系:___________ (填化学式)。
(2)X的浓溶液与铜在一定条件下可以发生反应,该反应的化学反应方程式为___________ ,体现了X的_________ 性质。
(3)收集了一些含有S元素的酸雨,放置一段时间后,pH变小,小攀认为可能是因为酸雨中的亚硫酸被氧化为了___________ 。
(4)配平下列反应:_______
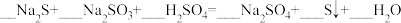 。
。
(5)如图是验证二氧化硫性质的实验装置。___________ (填序号,下同);B中___________ ;C中___________ 。D装置的作用是___________ 。
(2)X的浓溶液与铜在一定条件下可以发生反应,该反应的化学反应方程式为
(3)收集了一些含有S元素的酸雨,放置一段时间后,pH变小,小攀认为可能是因为酸雨中的亚硫酸被氧化为了
(4)配平下列反应:
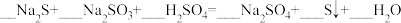 。
。(5)如图是验证二氧化硫性质的实验装置。

您最近一年使用:0次
9 . 无机非金属材料与人类社会的发展与进步息息相关,硅元素更是无机非金属材料的主角,地壳质量的90%以上是二氧化硅和硅酸盐。回答下列问题:
(1)硅元素在元素周期中的位置____________ 。
(2)硅酸盐材料是传统无机非金属材料,下列产品属于硅酸盐的是_________ (填序号)。
①玻璃;②陶瓷;③石英玻璃;④硅芯片;⑤光导纤维;⑥水泥;⑦砖瓦
(3)盛装碱液的试剂瓶用橡胶塞而不用玻璃塞的原因是请用离子方程式来解释原因__________ 。
(4)实验室制取硅酸的方法是向硅酸钠溶液中加入稀盐酸,化学方程式为__________ 。
(5)制备陶瓷和普通水泥都需要以黏土为原料,黏土的主要成分是铝硅酸盐。某种黏土的主要成分为Al2Si2O5(OH)4,将其表示为氧化物的形式为aAl2O3·bSiO2·cH2O,则a:b:c=___________ 。
(1)硅元素在元素周期中的位置
(2)硅酸盐材料是传统无机非金属材料,下列产品属于硅酸盐的是
①玻璃;②陶瓷;③石英玻璃;④硅芯片;⑤光导纤维;⑥水泥;⑦砖瓦
(3)盛装碱液的试剂瓶用橡胶塞而不用玻璃塞的原因是请用离子方程式来解释原因
(4)实验室制取硅酸的方法是向硅酸钠溶液中加入稀盐酸,化学方程式为
(5)制备陶瓷和普通水泥都需要以黏土为原料,黏土的主要成分是铝硅酸盐。某种黏土的主要成分为Al2Si2O5(OH)4,将其表示为氧化物的形式为aAl2O3·bSiO2·cH2O,则a:b:c=
您最近一年使用:0次
10 . 将足量的SO2通入BaCl2溶液中,无明显实验现象,但当通入某种气体后可看到沉淀生成,这种试剂不可能 是
| A.H2S | B.NH3 | C.CO2 | D.NO2 |
您最近一年使用:0次







