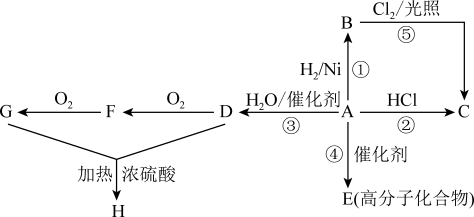
1 . 某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂。
(1)写出A、B、D、E的结构简式:A___________ ,B___________ ,D___________ ,F___________ 。
(2)A能发生聚合反应,其产物为E,E的结构简式为___________ 。
(3)写出②反应的化学反应方程式以及反应类型:②___________ ;反应类型___________ 。
(4)D可以在铜或者银的催化下,逐步氧化,请写出D氧化为F的化学反应方程式以及反应类型:D→F___________ ;反应类型___________ 。
(5)写出D和G生成H的化学反应方程式:D+G→H___________ 。
(6)反应②⑤均可制氯乙烷,反应___________ 最好(填反应序号),原因是___________ 。
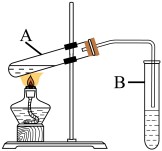
(7)反应D+G→H的实验装置如图所示,试管B中在反应前加入的是___________ 。
(1)写出A、B、D、E的结构简式:A
(2)A能发生聚合反应,其产物为E,E的结构简式为
(3)写出②反应的化学反应方程式以及反应类型:②
(4)D可以在铜或者银的催化下,逐步氧化,请写出D氧化为F的化学反应方程式以及反应类型:D→F
(5)写出D和G生成H的化学反应方程式:D+G→H
(6)反应②⑤均可制氯乙烷,反应
(7)反应D+G→H的实验装置如图所示,试管B中在反应前加入的是
您最近一年使用:0次
2 . 某有机物的结构简式如图所示,则下列说法中不正确的是
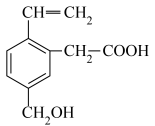
A.该有机物既能与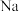 反应,还能与 反应,还能与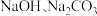 反应 反应 |
| B.该有机物中有3种官能团 |
| C.该有机物在一定条件下能发生加成、加聚、取代、氧化等反应 |
D. 该有机物和足量金属钠反应生成 该有机物和足量金属钠反应生成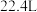 气体 气体 |
您最近一年使用:0次
名校
3 . 下列根据实验方案设计及现象得出结论错误的是
| 选项 | 实验设计及现象 | 结论 |
| A | 往碘的 溶液中加入等体积浓KI溶液,振荡。溶液分层,下层紫红色变浅粉红色,上层呈棕黄色 溶液中加入等体积浓KI溶液,振荡。溶液分层,下层紫红色变浅粉红色,上层呈棕黄色 | 碘在浓KI溶液中溶解能力大于在 中溶解能力 中溶解能力 |
| B | 有机物A加入NaOH乙醇溶液中,充分加热:冷却后,取混合液加足量硝酸酸化,滴加硝酸银溶液,未产生白色沉淀 | 有机物A不可能是氯代烃 |
| C | 向 溶液中,先加NaOH溶液调节 溶液中,先加NaOH溶液调节 ,有红褐色沉淀生成,再加入足量的KSCN溶液,沉淀不溶解 ,有红褐色沉淀生成,再加入足量的KSCN溶液,沉淀不溶解 | 在 时, 时, 结合 结合 的能力比 的能力比 强 强 |
| D | 常温下,用pH计分别测定浓度均为 的KCl溶液和 的KCl溶液和 溶液的pH,测得pH均为7.0 溶液的pH,测得pH均为7.0 | 但两溶液中水的电离程度不相同 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 .  、
、 是新型磁性材料的成分,设
是新型磁性材料的成分,设 为阿伏加德罗常数的值,依据其中有关元素回答问题:
为阿伏加德罗常数的值,依据其中有关元素回答问题:
(1)钕(Nd)属于镧系元素,则其在元素周期表中处于___________ 区, 的价电子排布图为
的价电子排布图为___________ 。
(2) 的立体构型为
的立体构型为___________ ;F原子核外有___________ 种不同空间运动状态的电子。
(3) 是一种还原剂,B原子的杂化方式为
是一种还原剂,B原子的杂化方式为___________ 。该物质中是否存在配位键___________ (填“是”或“否”)。
(4) 的钙钛矿型晶胞结构如图所示,其中Co填充在F形成的正八面体中心。
的钙钛矿型晶胞结构如图所示,其中Co填充在F形成的正八面体中心。___________ 。
②该晶体密度为 ,则K和Co之间的最短距离为
,则K和Co之间的最短距离为___________ pm。
(5) 的制备:称取研细的
的制备:称取研细的 和
和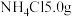 于烧杯中溶解;将溶液转入三颈烧瓶,分液漏斗中分别装有25mL浓氨水、5mL30%的
于烧杯中溶解;将溶液转入三颈烧瓶,分液漏斗中分别装有25mL浓氨水、5mL30%的 溶液,控制反应温度为60℃,打开分液漏斗,反应一段时间后,得
溶液,控制反应温度为60℃,打开分液漏斗,反应一段时间后,得 溶液。写出该反应的离子方程式
溶液。写出该反应的离子方程式___________ 。若上述实验过程中得到 ,则其中所含的
,则其中所含的 键数目为
键数目为___________ 。
(6)已知某温度下 的电离平衡常数:
的电离平衡常数: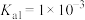 、
、 ,
,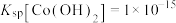 、
、 。写出该温度时向
。写出该温度时向 碳酸钠溶液中逐滴加入
碳酸钠溶液中逐滴加入 溶液,生成沉淀的离子方程式:
溶液,生成沉淀的离子方程式:___________ 。
 、
、 是新型磁性材料的成分,设
是新型磁性材料的成分,设 为阿伏加德罗常数的值,依据其中有关元素回答问题:
为阿伏加德罗常数的值,依据其中有关元素回答问题:(1)钕(Nd)属于镧系元素,则其在元素周期表中处于
 的价电子排布图为
的价电子排布图为(2)
 的立体构型为
的立体构型为(3)
 是一种还原剂,B原子的杂化方式为
是一种还原剂,B原子的杂化方式为(4)
 的钙钛矿型晶胞结构如图所示,其中Co填充在F形成的正八面体中心。
的钙钛矿型晶胞结构如图所示,其中Co填充在F形成的正八面体中心。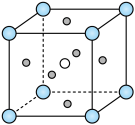
②该晶体密度为
 ,则K和Co之间的最短距离为
,则K和Co之间的最短距离为(5)
 的制备:称取研细的
的制备:称取研细的 和
和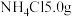 于烧杯中溶解;将溶液转入三颈烧瓶,分液漏斗中分别装有25mL浓氨水、5mL30%的
于烧杯中溶解;将溶液转入三颈烧瓶,分液漏斗中分别装有25mL浓氨水、5mL30%的 溶液,控制反应温度为60℃,打开分液漏斗,反应一段时间后,得
溶液,控制反应温度为60℃,打开分液漏斗,反应一段时间后,得 溶液。写出该反应的离子方程式
溶液。写出该反应的离子方程式 ,则其中所含的
,则其中所含的 键数目为
键数目为(6)已知某温度下
 的电离平衡常数:
的电离平衡常数: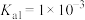 、
、 ,
,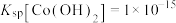 、
、 。写出该温度时向
。写出该温度时向 碳酸钠溶液中逐滴加入
碳酸钠溶液中逐滴加入 溶液,生成沉淀的离子方程式:
溶液,生成沉淀的离子方程式:
您最近一年使用:0次
5 . 有效去除大气中的 是环境保护的重要课题。
是环境保护的重要课题。
(1)用水吸收 的相关热化学方程式如下:
的相关热化学方程式如下:
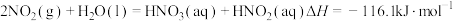
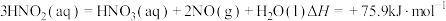
反应 的
的
___________  。
。
(2)用稀硝酸吸收 ,得到
,得到 和
和 的混合溶液,电解该混合溶液可获得较浓的硝酸,写出电解时阳极的电极反应式:
的混合溶液,电解该混合溶液可获得较浓的硝酸,写出电解时阳极的电极反应式:___________ 。( 是弱酸)
是弱酸)
(3)用酸性 水溶液吸收
水溶液吸收 ,吸收过程中存在
,吸收过程中存在 与
与 生成
生成 和
和 的反应,写出该反应的化学方程式:
的反应,写出该反应的化学方程式:___________ 。
(4)在有氧条件下,新型催化剂 能催化
能催化 与
与 反应生成
反应生成 。
。
① 与
与 生成
生成 的反应中,当生成
的反应中,当生成 时,转移的电子数为
时,转移的电子数为___________  。
。
②将一定比例的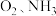 和
和 的混合气体,匀速通入装有催化剂
的混合气体,匀速通入装有催化剂 的反应器中反应(装置见图):
的反应器中反应(装置见图): 的去除率随反应温度的变化曲线如图所示,在
的去除率随反应温度的变化曲线如图所示,在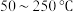 范围内随着温度的升高,
范围内随着温度的升高, 的去除率先迅速上升后缓慢上升的主要原因是
的去除率先迅速上升后缓慢上升的主要原因是___________ 。 (氯的化合价为
(氯的化合价为 价),其原理是
价),其原理是
 接电源的
接电源的___________ (填“正”或“负”)极。
②阳极反应式是___________ 。
 是环境保护的重要课题。
是环境保护的重要课题。(1)用水吸收
 的相关热化学方程式如下:
的相关热化学方程式如下: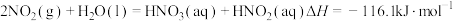
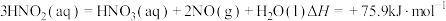
反应
 的
的
 。
。(2)用稀硝酸吸收
 ,得到
,得到 和
和 的混合溶液,电解该混合溶液可获得较浓的硝酸,写出电解时阳极的电极反应式:
的混合溶液,电解该混合溶液可获得较浓的硝酸,写出电解时阳极的电极反应式: 是弱酸)
是弱酸)(3)用酸性
 水溶液吸收
水溶液吸收 ,吸收过程中存在
,吸收过程中存在 与
与 生成
生成 和
和 的反应,写出该反应的化学方程式:
的反应,写出该反应的化学方程式:(4)在有氧条件下,新型催化剂
 能催化
能催化 与
与 反应生成
反应生成 。
。①
 与
与 生成
生成 的反应中,当生成
的反应中,当生成 时,转移的电子数为
时,转移的电子数为 。
。②将一定比例的
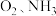 和
和 的混合气体,匀速通入装有催化剂
的混合气体,匀速通入装有催化剂 的反应器中反应(装置见图):
的反应器中反应(装置见图):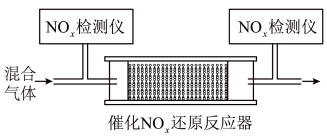
 的去除率随反应温度的变化曲线如图所示,在
的去除率随反应温度的变化曲线如图所示,在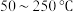 范围内随着温度的升高,
范围内随着温度的升高, 的去除率先迅速上升后缓慢上升的主要原因是
的去除率先迅速上升后缓慢上升的主要原因是
 (氯的化合价为
(氯的化合价为 价),其原理是
价),其原理是
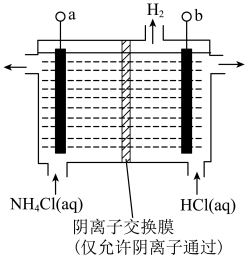
 接电源的
接电源的②阳极反应式是
您最近一年使用:0次
6 . 实验小组制备高铁酸钾 并探究其性质。资料:
并探究其性质。资料: 为紫色固体,微溶于
为紫色固体,微溶于 溶液;具有强氧化性,在酸性或中性溶液中快速产生
溶液;具有强氧化性,在酸性或中性溶液中快速产生 ,在碱性溶液中较稳定。
,在碱性溶液中较稳定。
(1)制备 (夹持装置略)
(夹持装置略) 中反应的化学方程式是
中反应的化学方程式是 ___________ (锰被还原为 )。
)。
②将除杂装置 补充完整并标明所用试剂。
补充完整并标明所用试剂。___________
③ 中得到紫色固体和溶液。
中得到紫色固体和溶液。 中
中 发生的反应有
发生的反应有 ,另外还有
,另外还有___________ (离子方程式)。
(2)探究 的性质
的性质
①取 中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液
中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液 ,经检验气体中含有
,经检验气体中含有 。为证明是否
。为证明是否 氧化了
氧化了 而产生
而产生 ,设计以下方案:
,设计以下方案:
i.由方案 中溶液变红可知
中溶液变红可知 中含有
中含有___________ 离子,但该离子的产生不能判断一定是 将
将 氧化,还可能由
氧化,还可能由___________ 产生(用离子方程式表示)。
ii.方案 可证明
可证明 氧化了
氧化了 。用
。用 溶液洗涤的目的是
溶液洗涤的目的是___________ 。
②根据 的制备实验得出:氧化性
的制备实验得出:氧化性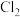
___________ 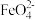 (填“
(填“ ”或“
”或“ ”),而方案
”),而方案 实验表明,
实验表明, 和
和 的氧化性强弱关系相反,原因是
的氧化性强弱关系相反,原因是___________ 。
③资料表明,酸性溶液中的氧化性
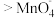 ,验证实验如下:将溶液
,验证实验如下:将溶液 滴入
滴入 和足量
和足量 的混合溶液中,振荡后溶液呈浅紫色,该现象能证明氧化性
的混合溶液中,振荡后溶液呈浅紫色,该现象能证明氧化性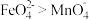 ,请说明理由:
,请说明理由:___________ 。
 并探究其性质。资料:
并探究其性质。资料: 为紫色固体,微溶于
为紫色固体,微溶于 溶液;具有强氧化性,在酸性或中性溶液中快速产生
溶液;具有强氧化性,在酸性或中性溶液中快速产生 ,在碱性溶液中较稳定。
,在碱性溶液中较稳定。(1)制备
 (夹持装置略)
(夹持装置略)
 中反应的化学方程式是
中反应的化学方程式是  )。
)。②将除杂装置
 补充完整并标明所用试剂。
补充完整并标明所用试剂。③
 中得到紫色固体和溶液。
中得到紫色固体和溶液。 中
中 发生的反应有
发生的反应有 ,另外还有
,另外还有(2)探究
 的性质
的性质①取
 中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液
中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液 ,经检验气体中含有
,经检验气体中含有 。为证明是否
。为证明是否 氧化了
氧化了 而产生
而产生 ,设计以下方案:
,设计以下方案:方案 | 取少量 ,滴加 ,滴加 溶液至过量,溶液呈红色。 溶液至过量,溶液呈红色。 |
方案 | 用 溶液充分洗涤C中所得固体,再用 溶液充分洗涤C中所得固体,再用 溶液将 溶液将 溶出,得到紫色溶液b。取少量 溶出,得到紫色溶液b。取少量 ,滴加盐酸,有 ,滴加盐酸,有 产生。 产生。 |
 中溶液变红可知
中溶液变红可知 中含有
中含有 将
将 氧化,还可能由
氧化,还可能由ii.方案
 可证明
可证明 氧化了
氧化了 。用
。用 溶液洗涤的目的是
溶液洗涤的目的是②根据
 的制备实验得出:氧化性
的制备实验得出:氧化性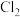
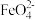 (填“
(填“ ”或“
”或“ ”),而方案
”),而方案 实验表明,
实验表明, 和
和 的氧化性强弱关系相反,原因是
的氧化性强弱关系相反,原因是③资料表明,酸性溶液中的氧化性

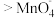 ,验证实验如下:将溶液
,验证实验如下:将溶液 滴入
滴入 和足量
和足量 的混合溶液中,振荡后溶液呈浅紫色,该现象能证明氧化性
的混合溶液中,振荡后溶液呈浅紫色,该现象能证明氧化性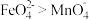 ,请说明理由:
,请说明理由:
您最近一年使用:0次
名校
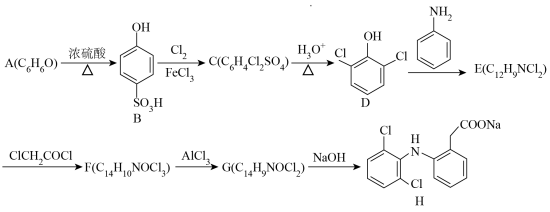
7 . 一种非甾体抗炎药物(H)的合成路线如下(部分反应条件省略):
(1)D的化学名称为___________ (用系统命名法命名);其中官能团的名称为___________ 。
(2)设计A→B和C→D两步反应的目的是___________ 。
(3)D→E的反应类型为___________ ;E→F的化学反应方程式为___________ 。
(4)C的结构简式为___________ 。
(5)符合下列条件G的同分异构体共有___________ 种,结构简式为___________ (任写出一种)。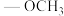 、―CN;
、―CN;
③含有四种化学环境的氢。
(6)已知: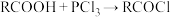 。综合上述信息,写出以
。综合上述信息,写出以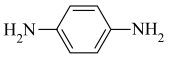 和
和 为主要原料制备
为主要原料制备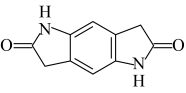 的合成路线
的合成路线___________ 。
已知:I.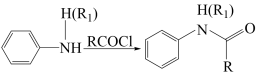
Ⅱ.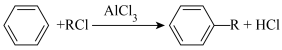
(1)D的化学名称为
(2)设计A→B和C→D两步反应的目的是
(3)D→E的反应类型为
(4)C的结构简式为
(5)符合下列条件G的同分异构体共有
①除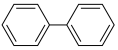 结构外,不含其他环状结构;
结构外,不含其他环状结构;
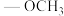 、―CN;
、―CN;③含有四种化学环境的氢。
(6)已知:
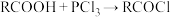 。综合上述信息,写出以
。综合上述信息,写出以 和
和 为主要原料制备
为主要原料制备 的合成路线
的合成路线
您最近一年使用:0次
名校
8 . 25℃时, 水溶液中
水溶液中 、
、 、
、 的分布分数
的分布分数 与pH的关系如下图。例如
与pH的关系如下图。例如 。向0.5L浓度为0.1mol/L的氨水中通入
。向0.5L浓度为0.1mol/L的氨水中通入 气体。已知该温度下,
气体。已知该温度下, 的
的 ,下列说法正确的是
,下列说法正确的是
 水溶液中
水溶液中 、
、 、
、 的分布分数
的分布分数 与pH的关系如下图。例如
与pH的关系如下图。例如 。向0.5L浓度为0.1mol/L的氨水中通入
。向0.5L浓度为0.1mol/L的氨水中通入 气体。已知该温度下,
气体。已知该温度下, 的
的 ,下列说法正确的是
,下列说法正确的是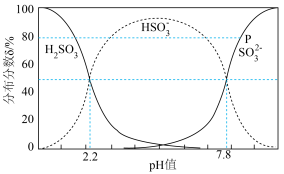
A.通入0.05mol 时, 时,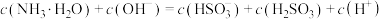 |
B.当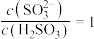 时, 时,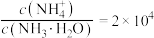 |
C.当 时, 时,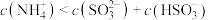 |
D. 的 的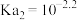 |
您最近一年使用:0次
名校
解题方法
9 .  (三草酸合铁酸钾)为亮绿色晶体,可用于晒制蓝图。回答下列问题:
(三草酸合铁酸钾)为亮绿色晶体,可用于晒制蓝图。回答下列问题:
(1)晒制蓝图时,用 作感光剂,以
作感光剂,以 溶液为显色剂。其光解反应的化学方程式为
溶液为显色剂。其光解反应的化学方程式为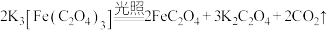 ;显色反应中生成的蓝色物质的化学式为
;显色反应中生成的蓝色物质的化学式为___________ 。
(2)某小组为探究三草酸合铁酸钾的热分解产物,按下图所示装置进行实验。___________ 。
②实验中观察到装置B、F中澄清石灰水均变浑浊,装置E中固体变为红色,由此判断热分解产物中一定含有___________ 。
③为防止倒吸,停止实验时应进行的操作是___________ 。
④样品完全分解后,装置A中的残留物含有FeO和 ,检验
,检验 存在的方法是取少许固体粉末于试管中,加稀硫酸溶解,
存在的方法是取少许固体粉末于试管中,加稀硫酸溶解,___________ (补全试剂和现象),证明残留物中含有 。
。
(3)测定三草酸合铁酸钾中铁的含量。
①称量mg样品于锥形瓶中,溶解后加稀 酸化,用
酸化,用 溶液滴定至终点。该操作的目的是
溶液滴定至终点。该操作的目的是___________ ,滴定终点的现象是___________ 。
②向上述溶液中加入适量还原剂将 完全还原为
完全还原为 ,加入稀
,加入稀 酸化后,用
酸化后,用 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液VmL。该晶体中铁元素的质量分数的表达式为
溶液VmL。该晶体中铁元素的质量分数的表达式为___________ 。若滴定前滴定管尖嘴内有气泡,终点读数时滴定管尖嘴内无气泡,会使测定结果___________ (填“偏大””“偏小”或“无影响”)。
③常温下,已知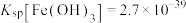 ,若将
,若将 与
与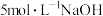 溶液等体积混合,静置,则上层清液中
溶液等体积混合,静置,则上层清液中 的浓度为
的浓度为___________  。
。
 (三草酸合铁酸钾)为亮绿色晶体,可用于晒制蓝图。回答下列问题:
(三草酸合铁酸钾)为亮绿色晶体,可用于晒制蓝图。回答下列问题:(1)晒制蓝图时,用
 作感光剂,以
作感光剂,以 溶液为显色剂。其光解反应的化学方程式为
溶液为显色剂。其光解反应的化学方程式为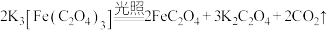 ;显色反应中生成的蓝色物质的化学式为
;显色反应中生成的蓝色物质的化学式为(2)某小组为探究三草酸合铁酸钾的热分解产物,按下图所示装置进行实验。
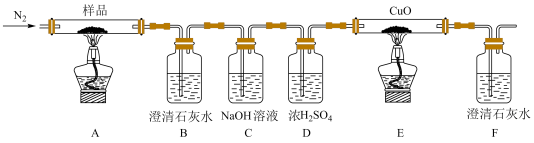
②实验中观察到装置B、F中澄清石灰水均变浑浊,装置E中固体变为红色,由此判断热分解产物中一定含有
③为防止倒吸,停止实验时应进行的操作是
④样品完全分解后,装置A中的残留物含有FeO和
 ,检验
,检验 存在的方法是取少许固体粉末于试管中,加稀硫酸溶解,
存在的方法是取少许固体粉末于试管中,加稀硫酸溶解, 。
。(3)测定三草酸合铁酸钾中铁的含量。
①称量mg样品于锥形瓶中,溶解后加稀
 酸化,用
酸化,用 溶液滴定至终点。该操作的目的是
溶液滴定至终点。该操作的目的是②向上述溶液中加入适量还原剂将
 完全还原为
完全还原为 ,加入稀
,加入稀 酸化后,用
酸化后,用 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液VmL。该晶体中铁元素的质量分数的表达式为
溶液VmL。该晶体中铁元素的质量分数的表达式为③常温下,已知
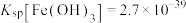 ,若将
,若将 与
与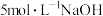 溶液等体积混合,静置,则上层清液中
溶液等体积混合,静置,则上层清液中 的浓度为
的浓度为 。
。
您最近一年使用:0次
名校
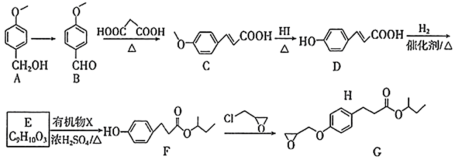
10 . 化合物G是一种医药中间体,以芳香化合物A为原料制备G的一种合成路线如下:
(1)A生成B所需的试剂和条件为___________ 。
(2)B与新制的氢氧化铜悬浊液反应的化学方程式:___________ 。
(3)D中含氧官能团的名称为___________ ,1molD可与含___________ 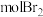 的水溶液发生反应。
的水溶液发生反应。
(4)有机物X的名称为___________ 。
(5)由F生成G的反应类型为___________ ;一个G分子中手性碳原子(连有四个不同原子或基团的碳原子)的数目为___________ 。
(6)芳香族化合物H是D的同分异构体,同时满足下列条件的H的结构有___________ 种(不含立体异构),任写出其中一种同分异物体的结构简式:___________ 。
①分子中有五个碳原子在一条直线上;
②能与NaOH溶液反应,且1molH消耗3molNaOH;
③苯环上的一氯代物只有一种。
(7)参照上述合成路线和信息,以乙二醛( )和丙二醛(
)和丙二醛(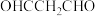 )为原料(无机试剂任选),设计制备
)为原料(无机试剂任选),设计制备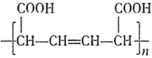 的合成路线:
的合成路线:___________ 。
已知: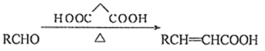
(1)A生成B所需的试剂和条件为
(2)B与新制的氢氧化铜悬浊液反应的化学方程式:
(3)D中含氧官能团的名称为
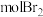 的水溶液发生反应。
的水溶液发生反应。(4)有机物X的名称为
(5)由F生成G的反应类型为
(6)芳香族化合物H是D的同分异构体,同时满足下列条件的H的结构有
①分子中有五个碳原子在一条直线上;
②能与NaOH溶液反应,且1molH消耗3molNaOH;
③苯环上的一氯代物只有一种。
(7)参照上述合成路线和信息,以乙二醛(
 )和丙二醛(
)和丙二醛(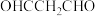 )为原料(无机试剂任选),设计制备
)为原料(无机试剂任选),设计制备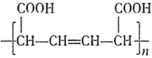 的合成路线:
的合成路线:
您最近一年使用:0次



