1 .  可用于制备除虫剂、发光材料等。某课题小组拟用硫酸钙和焦炭在高温条件下反应制备硫化钙并检验气体产物。回答下列问题:
可用于制备除虫剂、发光材料等。某课题小组拟用硫酸钙和焦炭在高温条件下反应制备硫化钙并检验气体产物。回答下列问题:
(1)甲同学设计如图所示的实验装置检验气体产物。___________ 。
②装置D中能证明产物中有 的实验现象为
的实验现象为___________ ,D中发生反应的化学方程式为___________ 。
(2)乙同学提出,根据氧化还原反应原理,装置A中的气体产物可能还有 、
、 ,为了验证具体的气体产物,请结合上述装置并选择下列仪器设计实验方案(有些仪器可重复使用)。
,为了验证具体的气体产物,请结合上述装置并选择下列仪器设计实验方案(有些仪器可重复使用)。___________ (填字母)。
A、F、___________、___________、I、H、I、M
②能证明有 生成的实验现象是
生成的实验现象是___________ 。
③若 中混有
中混有 ,除上述试剂外,还可以将气体通入饱和
,除上述试剂外,还可以将气体通入饱和___________ (填化学式)溶液中,以除去 。
。
(3)经实验检验反应的气体产物有 、
、 、
、 且气体体积之比为
且气体体积之比为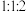 ,写出装置A中发生反应的化学方程式:
,写出装置A中发生反应的化学方程式:___________ 。
(4)利用重量法测定固体产物中各成分的质量之比。将少量固体产物溶于足量的饱和碳酸钠溶液中,再进行过滤、洗涤、干燥等操作,需要测定的物理量有固体产物的质量和生成___________ 沉淀的质量(填化学式)。[已知 与
与 反应生成
反应生成 和
和 ]
]
 可用于制备除虫剂、发光材料等。某课题小组拟用硫酸钙和焦炭在高温条件下反应制备硫化钙并检验气体产物。回答下列问题:
可用于制备除虫剂、发光材料等。某课题小组拟用硫酸钙和焦炭在高温条件下反应制备硫化钙并检验气体产物。回答下列问题:(1)甲同学设计如图所示的实验装置检验气体产物。
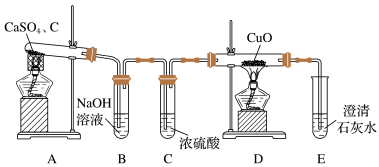
②装置D中能证明产物中有
 的实验现象为
的实验现象为(2)乙同学提出,根据氧化还原反应原理,装置A中的气体产物可能还有
 、
、 ,为了验证具体的气体产物,请结合上述装置并选择下列仪器设计实验方案(有些仪器可重复使用)。
,为了验证具体的气体产物,请结合上述装置并选择下列仪器设计实验方案(有些仪器可重复使用)。 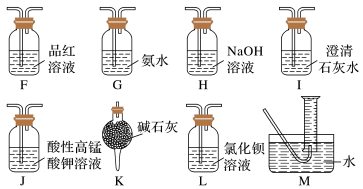
A、F、___________、___________、I、H、I、M
②能证明有
 生成的实验现象是
生成的实验现象是③若
 中混有
中混有 ,除上述试剂外,还可以将气体通入饱和
,除上述试剂外,还可以将气体通入饱和 。
。(3)经实验检验反应的气体产物有
 、
、 、
、 且气体体积之比为
且气体体积之比为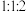 ,写出装置A中发生反应的化学方程式:
,写出装置A中发生反应的化学方程式:(4)利用重量法测定固体产物中各成分的质量之比。将少量固体产物溶于足量的饱和碳酸钠溶液中,再进行过滤、洗涤、干燥等操作,需要测定的物理量有固体产物的质量和生成
 与
与 反应生成
反应生成 和
和 ]
]
您最近一年使用:0次
名校
解题方法
2 . 甲醇是重要的化工原料,利用合成气(CO、 、
、 )在催化剂的作用下合成甲醇。在体积为1L的恒容密闭容器中,充入1.0 mol
)在催化剂的作用下合成甲醇。在体积为1L的恒容密闭容器中,充入1.0 mol  和3.0 mol
和3.0 mol  ,在一定条件下发生反应:
,在一定条件下发生反应: ,测得
,测得 和
和 的物质的量随时间的变化如图所示。回答下列问题:
的物质的量随时间的变化如图所示。回答下列问题:___________ mol⋅L ⋅min
⋅min ,此时v(正)
,此时v(正)___________ v(逆)(填“>”“<”或“=”)。
②下列措施能增大反应速率的是___________ (填字母)。
A.升高温度 B.降低压强 C.减小 的浓度 D.加入合适的催化剂
的浓度 D.加入合适的催化剂
(2)反应达到平衡时, 的转化率为
的转化率为___________ , 的体积分数为
的体积分数为___________ 。
(3)下列描述中能说明上述反应达到平衡状态的是___________(填字母)。
(4)化石燃料燃烧产生的 是主要的温室气体之一,使用电化学方法能够对
是主要的温室气体之一,使用电化学方法能够对 进行吸收。利用活泼金属与
进行吸收。利用活泼金属与 的反应,能够构建金属
的反应,能够构建金属 电池。其中一种
电池。其中一种 电池的模型如下图所示(图中
电池的模型如下图所示(图中 是固体):
是固体):___________ (填“正”或“负”)极,正极电极反应式为___________ 。
②该电池中每转移2 mol电子,能够吸收___________ mol  。
。
 、
、 )在催化剂的作用下合成甲醇。在体积为1L的恒容密闭容器中,充入1.0 mol
)在催化剂的作用下合成甲醇。在体积为1L的恒容密闭容器中,充入1.0 mol  和3.0 mol
和3.0 mol  ,在一定条件下发生反应:
,在一定条件下发生反应: ,测得
,测得 和
和 的物质的量随时间的变化如图所示。回答下列问题:
的物质的量随时间的变化如图所示。回答下列问题: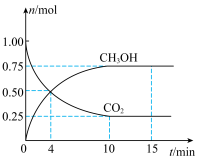
 ⋅min
⋅min ,此时v(正)
,此时v(正)②下列措施能增大反应速率的是
A.升高温度 B.降低压强 C.减小
 的浓度 D.加入合适的催化剂
的浓度 D.加入合适的催化剂(2)反应达到平衡时,
 的转化率为
的转化率为 的体积分数为
的体积分数为(3)下列描述中能说明上述反应达到平衡状态的是___________(填字母)。
A. 、 、 、 、 、 、 四种物质的浓度相等 四种物质的浓度相等 |
| B.混合气体的密度不随时间的变化而变化 |
| C.混合气体的总压强不随时间的变化而变化 |
D.单位时间内消耗3 mol  的同时生成1 mol 的同时生成1 mol  |
(4)化石燃料燃烧产生的
 是主要的温室气体之一,使用电化学方法能够对
是主要的温室气体之一,使用电化学方法能够对 进行吸收。利用活泼金属与
进行吸收。利用活泼金属与 的反应,能够构建金属
的反应,能够构建金属 电池。其中一种
电池。其中一种 电池的模型如下图所示(图中
电池的模型如下图所示(图中 是固体):
是固体):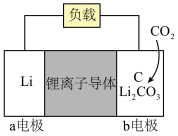
②该电池中每转移2 mol电子,能够吸收
 。
。
您最近一年使用:0次
7日内更新
|
77次组卷
|
3卷引用:山西省名校联考2023-2024学年高一下学期5月月考化学试题
3 . 有机物A的分子式为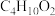 ,不含醚键,含氧官能团能被连续催化氧化为
,不含醚键,含氧官能团能被连续催化氧化为 。已知:同一个碳原子上连2个羟基不稳定。A可能的结构有(不考虑立体异构)
。已知:同一个碳原子上连2个羟基不稳定。A可能的结构有(不考虑立体异构)
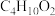 ,不含醚键,含氧官能团能被连续催化氧化为
,不含醚键,含氧官能团能被连续催化氧化为 。已知:同一个碳原子上连2个羟基不稳定。A可能的结构有(不考虑立体异构)
。已知:同一个碳原子上连2个羟基不稳定。A可能的结构有(不考虑立体异构)| A.7种 | B.5种 | C.4种 | D.3种 |
您最近一年使用:0次
4 . 利用氢气作为能源的前提是安全有效地解决储存氢气的问题。化学家已研究出多种储存氢气的方法。回答下列问题:
(1)某金属R的储氢材料可以通过化学反应将氢吸附和排放,已知R为短周期金属元素,其部分电离能数据如表所示:
该金属元素R是___________ (填元素符号),其位于元素周期表___________ 区。
(2)NH3BH3(氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。
氨硼烷(NH3BH3)中N、B都达到稳定结构,NH3BH3存在配位键,提供空轨道的是___________ (填元素符号),用化学键表示出(NH3BH3)分子的结构式:___________ 。
(3)有储氢功能的铜银合金晶体具有立方堆积结构,晶胞中Cu原子位于面心,Ag原子位于顶点,氢原子可进到由Cu原子与Ag原子构成的全部四面体空隙中。该晶体储氢后的化学式为___________ 。
(4)过渡金属Q与镧(La)形成的合金是一种储氢材料,其中基态Q原子的价层电子排布式为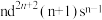 ,该合金的晶胞结构和z轴方向的投影图如图所示:
,该合金的晶胞结构和z轴方向的投影图如图所示:___________ ,该合金的密度为___________ g·cm-3(用含a,c的代数式表示,NA为阿伏加德罗常数的值)。
(1)某金属R的储氢材料可以通过化学反应将氢吸附和排放,已知R为短周期金属元素,其部分电离能数据如表所示:
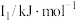 | 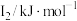 |  |  |  |
| 578 | 1817 | 2745 | 11577 | 14842 |
(2)NH3BH3(氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。
氨硼烷(NH3BH3)中N、B都达到稳定结构,NH3BH3存在配位键,提供空轨道的是
(3)有储氢功能的铜银合金晶体具有立方堆积结构,晶胞中Cu原子位于面心,Ag原子位于顶点,氢原子可进到由Cu原子与Ag原子构成的全部四面体空隙中。该晶体储氢后的化学式为
(4)过渡金属Q与镧(La)形成的合金是一种储氢材料,其中基态Q原子的价层电子排布式为
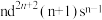 ,该合金的晶胞结构和z轴方向的投影图如图所示:
,该合金的晶胞结构和z轴方向的投影图如图所示:
您最近一年使用:0次
7日内更新
|
35次组卷
|
2卷引用:山西省部分学校2023-2024学年高二下学期五月份联化学试题
5 . 碱酸混合锌-硝酸根电池具有电压高、放电功率大等优点,其工作原理如图所示,工作时, 在双极膜(允许
在双极膜(允许 和
和 穿梭)界内解离成
穿梭)界内解离成 和
和 。下列说法正确的是
。下列说法正确的是
 在双极膜(允许
在双极膜(允许 和
和 穿梭)界内解离成
穿梭)界内解离成 和
和 。下列说法正确的是
。下列说法正确的是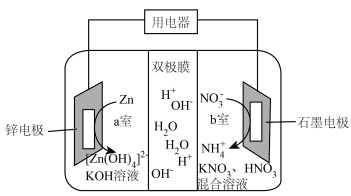
A.放电时,双极膜内的 会移向b室 会移向b室 |
B.放电时,锌电极的电极反应式为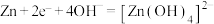 |
C.放电时,总反应为 |
| D.放电一段时间后,a室溶液pH会增大 |
您最近一年使用:0次
名校
6 . 设 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是
 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是A.标准状况下,0.5 mol  的体积为11.2 L 的体积为11.2 L |
B.1 mol  与1 mol 与1 mol  在光照下充分反应生成的 在光照下充分反应生成的 分子数目为 分子数目为 |
C.一定条件下,密闭容器中1 mol  与足量 与足量 充分反应时转移 充分反应时转移 个电子 个电子 |
D.标准状况下,22.4 L 中含有 中含有 键的数目为 键的数目为 |
您最近一年使用:0次
7日内更新
|
97次组卷
|
3卷引用:山西省名校联考2023-2024学年高一下学期5月月考化学试题
名校
解题方法
7 . 燃料电池能量转化效率高,供电量易于调节,具有广阔的应用前景。以 溶液为电解质溶液的某甲烷—空气燃料电池装置如图所示,下列说法错误的是
溶液为电解质溶液的某甲烷—空气燃料电池装置如图所示,下列说法错误的是
 溶液为电解质溶液的某甲烷—空气燃料电池装置如图所示,下列说法错误的是
溶液为电解质溶液的某甲烷—空气燃料电池装置如图所示,下列说法错误的是
| A.a极为电池的负极 | B.b极通入的气体为空气 |
C. 向b极方向移动 向b极方向移动 | D. 发生反应,转移 发生反应,转移 电子 电子 |
您最近一年使用:0次
名校
解题方法
8 . 硫的氧化物和氨的氧化物造成的环境问题日益受到关注。下列说法正确的是
A.硫在足量 中燃烧会生成 中燃烧会生成 |
B.在燃煤中加入 ,可以减少 ,可以减少 对环境的污染 对环境的污染 |
C. 能使酸性 能使酸性 溶液褪色,说明 溶液褪色,说明 具有漂白性 具有漂白性 |
D.汽车尾气中的主要大气污染物为 , , 和 和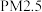 |
您最近一年使用:0次
解题方法
9 . 下列实验操作及现象能得出相应结论的是
| 选项 | 实验提作 | 现象 | 始论 |
| A | 在试管中加入少量淀粉和适量稀碳酸,加热一段时间,待溶液冷却后,加入新制氢氧化铜,加热 | 未观察到砖红色沉淀生成 | 淀粉未发生水解 |
| B | 向装有 和 和 的试管中分别滴加盐酸 的试管中分别滴加盐酸 | 装 的试管中产生黄绿色气体,装 的试管中产生黄绿色气体,装 的试管中无明显现象 的试管中无明显现象 | 氧化性: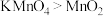 |
| C | 向蛋白质溶液中加入浓NaOH溶液 | 出现浑浊 | 蛋白质在NaOH溶液中发生了水解,生成了氨基酸 |
| D | 往75%的医用酒精中加入一小粒Na | 钠表面有大量气泡产生 | 钠能与 反应产生 反应产生 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
10 . 二氧化碳催化加氢制甲醇的反应为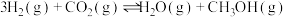 ,已知该反应为放热反应,在恒容密闭容器中充入
,已知该反应为放热反应,在恒容密闭容器中充入 和
和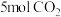 进行反应,下列说法正确的是
进行反应,下列说法正确的是
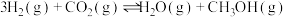 ,已知该反应为放热反应,在恒容密闭容器中充入
,已知该反应为放热反应,在恒容密闭容器中充入 和
和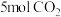 进行反应,下列说法正确的是
进行反应,下列说法正确的是A.反应过程中,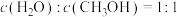 |
| B.气体密度不变可说明反应已达到平衡状态 |
| C.断键吸收的总能量大于形成化学键放出的总能量 |
D.反应达到平衡时 的转化率可能为 的转化率可能为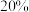 |
您最近一年使用:0次



