名校
解题方法
1 . 氮化锂是一种快离子导体,其电导率比其他无机锂盐都高,用于制造性能优越的全固态电池。某兴趣小组利用下列装置制备少量氮化锂,请回答下列问题: 和
和 ,约
,约 时
时 与
与 反应生成
反应生成 。
。
②氮化锂遇水剧烈反应,在空气中加热能剧烈燃烧。
(1)装置A的名称为___________ ;装置C的作用为___________ 。
(2)装置D中加入药品之前需要进行的操作是___________ 。
(3)按照气流的方向,装置的连接顺序为d接__,__接__,__接__,__接c;________ (填接口小写字母)。
(4)装置E中发生反应的化学方程式为___________ 。
(5)装置F的作用为___________ 。
(6) 的电子式为
的电子式为_______________ ;
实验测得装置B反应前后的质量如表所示:
则生成氮化锂的质量为_______________ g。

 和
和 ,约
,约 时
时 与
与 反应生成
反应生成 。
。②氮化锂遇水剧烈反应,在空气中加热能剧烈燃烧。
(1)装置A的名称为
(2)装置D中加入药品之前需要进行的操作是
(3)按照气流的方向,装置的连接顺序为d接__,__接__,__接__,__接c;
(4)装置E中发生反应的化学方程式为
(5)装置F的作用为
(6)
 的电子式为
的电子式为实验测得装置B反应前后的质量如表所示:
| 反应前 | 反应后 | |
| 装置B的质量/g | 19.2 | 28.3 |
您最近一年使用:0次
名校
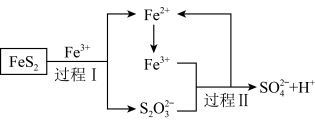
2 . 硫铁矿(含 )是一种重要的化学矿物原料,也是工业制硫酸的主要原料,其煅烧过程及产物存在如下转化关系:
)是一种重要的化学矿物原料,也是工业制硫酸的主要原料,其煅烧过程及产物存在如下转化关系:
(1)硫铁矿 中
中 元素的化合价为
元素的化合价为_______________ 。
(2)为了使反应Ⅰ燃烧得更充分,可以采用的措施是_______________ 。(任写一条)
(3)将 通入新制碘水中,发现溶液褪色,发生反应的离子方程式为
通入新制碘水中,发现溶液褪色,发生反应的离子方程式为_______________ 。
(4)下列关于 的说法不正确的是_______________。
的说法不正确的是_______________。
(5)工业上为了防止污染,可以利用氧化亚铁硫杆菌(T.f)对硫铁矿进行催化脱硫,该过程如图所示: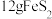 ,转移的电子的物质的量为
,转移的电子的物质的量为_______________ 。
②脱硫过程中产生的 在酸性溶液中会形成淡黄色沉淀并产生刺激性气味的气体,写出其离子方程式
在酸性溶液中会形成淡黄色沉淀并产生刺激性气味的气体,写出其离子方程式_______________ 。
③在 和
和 的混合液中,可用于检验
的混合液中,可用于检验 的试剂是
的试剂是_______________ 。
a.酸性高锰酸钾溶液 b.硫氰化钾溶液
c.先加入硫氰化钾溶液,再加入过氧化氢 d.氢氧化钠溶液
 )是一种重要的化学矿物原料,也是工业制硫酸的主要原料,其煅烧过程及产物存在如下转化关系:
)是一种重要的化学矿物原料,也是工业制硫酸的主要原料,其煅烧过程及产物存在如下转化关系:
(1)硫铁矿
 中
中 元素的化合价为
元素的化合价为(2)为了使反应Ⅰ燃烧得更充分,可以采用的措施是
(3)将
 通入新制碘水中,发现溶液褪色,发生反应的离子方程式为
通入新制碘水中,发现溶液褪色,发生反应的离子方程式为(4)下列关于
 的说法不正确的是_______________。
的说法不正确的是_______________。| A.浓硫酸有强氧化性,稀硫酸没有氧化性 |
| B.常温下,浓硫酸与铁不反应,故可用铁罐车储运浓硫酸 |
C.浓硫酸具有吸水性,可用于干燥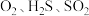 等气体 等气体 |
| D.蔗糖中滴入浓硫酸,可观察到蔗糖由白变黑、体积膨胀并有刺激性气味气体产生,该过程中浓硫酸体现了脱水性和强氧化性 |
(5)工业上为了防止污染,可以利用氧化亚铁硫杆菌(T.f)对硫铁矿进行催化脱硫,该过程如图所示:
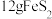 ,转移的电子的物质的量为
,转移的电子的物质的量为②脱硫过程中产生的
 在酸性溶液中会形成淡黄色沉淀并产生刺激性气味的气体,写出其离子方程式
在酸性溶液中会形成淡黄色沉淀并产生刺激性气味的气体,写出其离子方程式③在
 和
和 的混合液中,可用于检验
的混合液中,可用于检验 的试剂是
的试剂是a.酸性高锰酸钾溶液 b.硫氰化钾溶液
c.先加入硫氰化钾溶液,再加入过氧化氢 d.氢氧化钠溶液
您最近一年使用:0次
名校
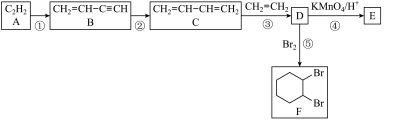
3 . 乙炔是一种重要的化工原料中间体,可以合成众多的化工产品。根据下列流程图,回答问题
(1)写出实验室制备A化学方程式_______ ;为除去 中的杂质,需将气体通入装有
中的杂质,需将气体通入装有_______ (填化学式)溶液的洗气瓶。
(2)化合物 能发生加聚反应,写出其中按1,4加聚反应的化学方程式
能发生加聚反应,写出其中按1,4加聚反应的化学方程式_______ 。
(3)③的反应类型为_______ 反应。
(4) 的结构简式为
的结构简式为_______ ,F的同分异构体中除 外含六元环的还有
外含六元环的还有_______ 种。
(5)已知有一样品 为
为 ,在足量
,在足量 中充分燃烧,将生成的混合气体依次通过无水
中充分燃烧,将生成的混合气体依次通过无水 和碱石灰,分别增重
和碱石灰,分别增重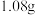 和
和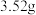 。质谱测得该有机物的相对分子量为118,其分子式为
。质谱测得该有机物的相对分子量为118,其分子式为_______ 。
(6)有机物 是一种重要的有机合成中间体,用于制造塑料、涂料和黏合剂等。由元素分析可知,有机物
是一种重要的有机合成中间体,用于制造塑料、涂料和黏合剂等。由元素分析可知,有机物 的分子式为
的分子式为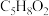 ,经红外光谱测定,有机物
,经红外光谱测定,有机物 中含有醛基;有机物
中含有醛基;有机物 的核磁共振氢谱图上有2组吸收峰,峰面积之比为
的核磁共振氢谱图上有2组吸收峰,峰面积之比为 。由此,可以推断有机物
。由此,可以推断有机物 的结构简式为
的结构简式为_______ 。
已知:①

(1)写出实验室制备A化学方程式
 中的杂质,需将气体通入装有
中的杂质,需将气体通入装有(2)化合物
 能发生加聚反应,写出其中按1,4加聚反应的化学方程式
能发生加聚反应,写出其中按1,4加聚反应的化学方程式(3)③的反应类型为
(4)
 的结构简式为
的结构简式为 外含六元环的还有
外含六元环的还有(5)已知有一样品
 为
为 ,在足量
,在足量 中充分燃烧,将生成的混合气体依次通过无水
中充分燃烧,将生成的混合气体依次通过无水 和碱石灰,分别增重
和碱石灰,分别增重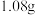 和
和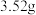 。质谱测得该有机物的相对分子量为118,其分子式为
。质谱测得该有机物的相对分子量为118,其分子式为(6)有机物
 是一种重要的有机合成中间体,用于制造塑料、涂料和黏合剂等。由元素分析可知,有机物
是一种重要的有机合成中间体,用于制造塑料、涂料和黏合剂等。由元素分析可知,有机物 的分子式为
的分子式为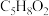 ,经红外光谱测定,有机物
,经红外光谱测定,有机物 中含有醛基;有机物
中含有醛基;有机物 的核磁共振氢谱图上有2组吸收峰,峰面积之比为
的核磁共振氢谱图上有2组吸收峰,峰面积之比为 。由此,可以推断有机物
。由此,可以推断有机物 的结构简式为
的结构简式为
您最近一年使用:0次
名校
4 . 短周期主族元素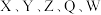 的原子序数依次增大,其中
的原子序数依次增大,其中 基态原子最外层
基态原子最外层 轨道有两个未成对电子,
轨道有两个未成对电子, 的电负性为
的电负性为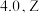 与
与 同主族且五种元素可形成如图所示的阴离子,下列说法正确的是
同主族且五种元素可形成如图所示的阴离子,下列说法正确的是
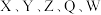 的原子序数依次增大,其中
的原子序数依次增大,其中 基态原子最外层
基态原子最外层 轨道有两个未成对电子,
轨道有两个未成对电子, 的电负性为
的电负性为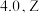 与
与 同主族且五种元素可形成如图所示的阴离子,下列说法正确的是
同主族且五种元素可形成如图所示的阴离子,下列说法正确的是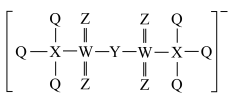
A. 可形成多种化合物且均为非极性分子 可形成多种化合物且均为非极性分子 |
B.第一电离能: |
C.相同条件下 的简单氢化物比 的简单氢化物比 的简单氢化物稳定,是因为 的简单氢化物稳定,是因为 的简单氢化物存在氢键 的简单氢化物存在氢键 |
D.简单原子半径: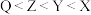 |
您最近一年使用:0次
名校
5 . 一种硼镁化合物具有超导性能,晶体结构属于立方晶系,其晶体结构、晶胞沿c轴的投影图如下所示,下列说法错误的是
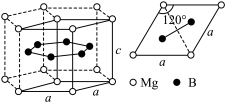
A.晶胞中含有1个 | B.该物质化学式为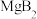 |
C.距离 最近的 最近的 有12个 有12个 | D. 与 与 最近距离为 最近距离为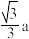 |
您最近一年使用:0次
名校
6 . 饮用水中 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为
还原为 ,反应的离子方程式为:
,反应的离子方程式为: (未配平)。设
(未配平)。设 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是
 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为
还原为 ,反应的离子方程式为:
,反应的离子方程式为: (未配平)。设
(未配平)。设 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是A.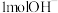 含有的电子数为 含有的电子数为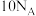 |
B.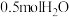 中含有氧氢键的数目为 中含有氧氢键的数目为 |
C.标准状况下,每生成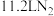 反应转移的电子数目为 反应转移的电子数目为 |
D.消耗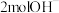 时,溶液中增加的 时,溶液中增加的 数目为 数目为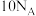 |
您最近一年使用:0次
解题方法
7 . 《自然》报道了我国科学家利用催化剂通过化学链合成氨。回答下列问题:
(1)NH3可用于制备NaN3、NH₄NO₃,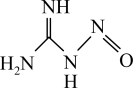 (亚硝基胍)等含氮化合物,基态N的核外电子排布为
(亚硝基胍)等含氮化合物,基态N的核外电子排布为___________ ; NH₄NO₃中 NH 中中心原子的杂化轨道类型为
中中心原子的杂化轨道类型为___________ NO 的空间结构为
的空间结构为___________ ; 亚硝基胍分子中σ键与π键的数目比为___________ 。
(2)N、P位于同一主族,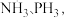 分子结构如图所示:
分子结构如图所示:___________ ,
②NH₃比PH₃的沸点高, 其主要原因是___________ 。
③磷化镓的晶胞结构如下图所示,A点坐标为(0,0,0),B点坐标为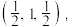 则C点坐标为
则C点坐标为___________ ;
(1)NH3可用于制备NaN3、NH₄NO₃,
 (亚硝基胍)等含氮化合物,基态N的核外电子排布为
(亚硝基胍)等含氮化合物,基态N的核外电子排布为 中中心原子的杂化轨道类型为
中中心原子的杂化轨道类型为 的空间结构为
的空间结构为(2)N、P位于同一主族,
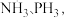 分子结构如图所示:
分子结构如图所示:
②NH₃比PH₃的沸点高, 其主要原因是
③磷化镓的晶胞结构如下图所示,A点坐标为(0,0,0),B点坐标为
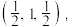 则C点坐标为
则C点坐标为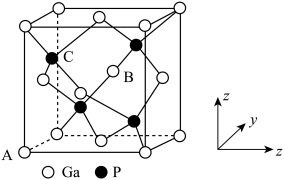
您最近一年使用:0次
解题方法
8 . 磷化硼(BP)是一种超硬耐磨涂层材料,其结构与金刚石类似,晶胞结构如图所示,设晶胞参数为 apm,下列说法不正确的是


| A.基态磷原子的核外电子运动状态有 15种 |
B.P与B原子的最近距离为 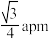 |
| C.与P原子最近的等距离的P原子有 12个 |
D.该晶体的密度为 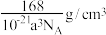 |
您最近一年使用:0次
9 . 氮和硒(Se)都是重要元素,在医药、催化、材料等领域有广泛应用,回答下列问题:
(1)乙烷硒啉是一种抗癌新药,其结构式如图:___________ ,价层有___________ 种不同能量的电子
②比较 、
、 、
、 三种氢化物:沸点由高到低依次为
三种氢化物:沸点由高到低依次为___________ ,稳定性由强到弱依次为___________ 。
③比较键角大小:气态 分子
分子___________ 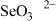 离子(填“>”“<”或“=”),原因是
离子(填“>”“<”或“=”),原因是
___________ 。
(2)① 是有机合成中常用的还原剂,其阴离子
是有机合成中常用的还原剂,其阴离子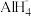 空间结构为
空间结构为___________ , 中存在的化学键
中存在的化学键___________ (填标号)。
A.离子键 B. 键 C.极性键 D.氢键
键 C.极性键 D.氢键
② 中阴离子的空间结构为
中阴离子的空间结构为___________ ;
(1)乙烷硒啉是一种抗癌新药,其结构式如图:
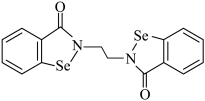
②比较
 、
、 、
、 三种氢化物:沸点由高到低依次为
三种氢化物:沸点由高到低依次为③比较键角大小:气态
 分子
分子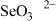 离子(填“>”“<”或“=”),原因是
离子(填“>”“<”或“=”),原因是(2)①
 是有机合成中常用的还原剂,其阴离子
是有机合成中常用的还原剂,其阴离子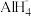 空间结构为
空间结构为 中存在的化学键
中存在的化学键A.离子键 B.
 键 C.极性键 D.氢键
键 C.极性键 D.氢键②
 中阴离子的空间结构为
中阴离子的空间结构为③1mol 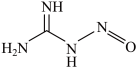 中含
中含 键
键
您最近一年使用:0次
10 . 电解硫酸钠溶液制取电池正极材料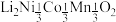 的前驱体
的前驱体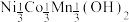 ,其工作原理如图所示。下列说法
,其工作原理如图所示。下列说法错误 的是
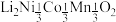 的前驱体
的前驱体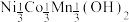 ,其工作原理如图所示。下列说法
,其工作原理如图所示。下列说法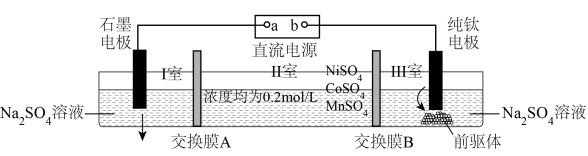
| A.交换膜B是阳离子交换膜 |
| B.通电一段时间后,I室溶液的pH降低 |
C.b是直流电源的负极,纯钛电极的反应为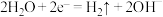 |
D.当产生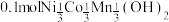 时,纯钛电极上至少产生标准状况下1.12L气体 时,纯钛电极上至少产生标准状况下1.12L气体 |
您最近一年使用:0次



