解题方法
1 . 表列出了①~⑨九种元素在周期表中的位置:
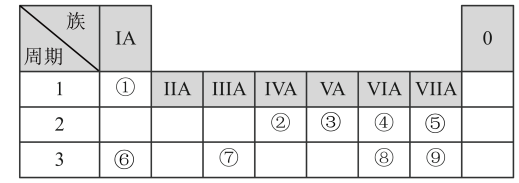
(1)①~⑨九种元素中原子半径最大的是_____ (填元素符号)。
(2)元素③的原子结构示意图为_____ ;元素①与⑨组成的化合物的电子式:_____ ;由⑤、⑥两种元素组成的化合物的化学键类型为_____ (“离子键”或“共价键”)。
(3)元素③、④的简单氢化物的稳定性较弱的是_____ (填化学式);元素⑧、⑨的最高价氧化物对应的水化物中,酸性较强的是_____ (填化学式)。
(4)元素①与②所形成的最简单有机物的空间结构是_____ ,该物质与⑨的单质在光照下发生反应,该反应的产物是_____ (填“纯净物”或“混合物”)。元素①与②所形成的最简单烯烃为M,写出M与元素⑨的单质在一定条件下反应的化学方程式:_____ ,该反应类型为_____ 。
(5)元素⑧的单质在空气中燃烧生成_____ 色固体,此固体与二氧化碳反应的化学方程式为_____ 。

(1)①~⑨九种元素中原子半径最大的是
(2)元素③的原子结构示意图为
(3)元素③、④的简单氢化物的稳定性较弱的是
(4)元素①与②所形成的最简单有机物的空间结构是
(5)元素⑧的单质在空气中燃烧生成
您最近一年使用:0次
解题方法
2 . 下列操作能达到目的的是
| 选项 | 操作 | 目的 |
| A | 向10 mL0.1 mol·L-1草酸溶液中先滴加1 mL0.1 mol·L-1KMnO4溶液,再滴加1 mL 0.2 mol·L-1KMnO4溶液 | 探究浓度对反应速率的影响 |
| B | 分别用pH计测定0.1 mol·L-1的HOCH2COOH溶液在25 °C、45 °C时的pH(浓度变化不考虑) | 探究温度对电离平衡的影响 |
| C | 将铁、铜片插入浓硝酸(常温)构成原电池,并连接电流计 | 验证原电池中较活泼金属为负极 |
| D | 向物质的量浓度均为1 mol·L-1的Na2CO3和Na2SO4混合液中加入等体积的过量AgNO3溶液 | 探究 Ag2CO3和Ag2SO4溶度积的大小 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-07-15更新
|
949次组卷
|
4卷引用:天津市2023届普通高中学业水平等级性考试模拟化学试题
名校
解题方法
3 . 下列实验方案中,不能测定出 和
和 的混合物中
的混合物中 质量分数的是
质量分数的是
 和
和 的混合物中
的混合物中 质量分数的是
质量分数的是A.取ag混合物与足量 溶液充分反应,过滤、洗涤、干燥,得到bg固体 溶液充分反应,过滤、洗涤、干燥,得到bg固体 |
| B.取ag混合物充分加热,质量减少bg |
| C.取ag混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得到bg固体 |
| D.取ag混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,质量增加bg |
您最近一年使用:0次
2022-07-12更新
|
1080次组卷
|
8卷引用:天津市和平区2021-2022学年高一下学期高中学业水平合格性模拟考试化学试题
天津市和平区2021-2022学年高一下学期高中学业水平合格性模拟考试化学试题重庆第二外国语学校2021-2022学年高一上学期期末考试化学试题重庆市主城区六校2021-2022学年高一上学期期末联考化学试题(已下线)卷03 阿伏伽德罗常数有关计算-【小题小卷】冲刺2022年高考化学小题限时集训(全国卷专用)河南省濮阳市2021-2022学年高一下学期学业质量检测(期末)化学试卷黑龙江省双鸭山市第一中学2022-2023学年高三上学期开学考试化学试题黑龙江省哈尔滨市第九中学校2022-2023学年高一上学期11月月考化学试题四川省内江市资中县第二中学2022-2023学年高二上学期期中考试化学试题
名校
解题方法
4 . 下列说法不正确 的是
| A.棉短绒中的纤维素可在铜氨溶液中溶解,将形成的溶液压入酸中可得到质量更高的纤维 |
| B.用纸层析法分离Fe3+和Cu2+,将滤纸上的试样点完全浸入展开剂可提高分离效果 |
| C.实验室制备阿司匹林过程中加入饱和NaHCO3溶液的主要目的是除去水杨酸 |
| D.将CoCl2•6H2O晶体溶于95%乙醇,逐滴滴加蒸馏水,溶液颜色由蓝色逐渐转变为粉红色 |
您最近一年使用:0次
2022-06-25更新
|
1101次组卷
|
3卷引用:天津市2023届普通高中学业水平等级性考试模拟化学试题
5 . 下图表示各物质之间的转化关系。已知:常温下B、D、F、G、I、J是气体,F、G是空气中的主要成分,D是一种碱性气体;A中阴、阳离子个数比是 ,E是一种黑色氧化物,H是紫红色金属单质(部分生成物和反应条件省略)
,E是一种黑色氧化物,H是紫红色金属单质(部分生成物和反应条件省略)

请按要求回答下列问题:
(1)A物质是_______ ;X物质是_______ ;K物质是_______ (均写化学式)。
(2)反应③的化学方程式是_______ 。
(3)反应①中产生标准状况下1.12L气体F,则转移的电子数目是_______ 。
(4)反应②的化学反应方程式为_______ ;作氧化剂的是_______ 。
(5)某小组同学用如图所示装置制取氨,并探究其性质。

①大试管中发生的反应的化学方程式是_______ 。
②请将方框中的收集装置补充完整_______ ,解释采用这种收集方法的原因是_______ 。
③甲同学用如图所示的装置进行尾气处理,乙同学认为不合理,其理由是:_______ 。

 ,E是一种黑色氧化物,H是紫红色金属单质(部分生成物和反应条件省略)
,E是一种黑色氧化物,H是紫红色金属单质(部分生成物和反应条件省略)
请按要求回答下列问题:
(1)A物质是
(2)反应③的化学方程式是
(3)反应①中产生标准状况下1.12L气体F,则转移的电子数目是
(4)反应②的化学反应方程式为
(5)某小组同学用如图所示装置制取氨,并探究其性质。

①大试管中发生的反应的化学方程式是
②请将方框中的收集装置补充完整
③甲同学用如图所示的装置进行尾气处理,乙同学认为不合理,其理由是:

您最近一年使用:0次
解题方法
6 . 乙酸硅[ (CH3COO)4Si,熔点:110°C,沸点:148°C]是白色至米色晶体。某校同学设计实验先制备SiCl4(熔点:-70℃,沸点:57.6℃,极易水解),再由SiCl4与乙酸酐[(CH3CO)2O(熔点:-73℃,沸点:140℃反应制备乙酸硅。回答下列问题:
(1)制备SiCl4装置(部分夹持仪器已省路)如下:
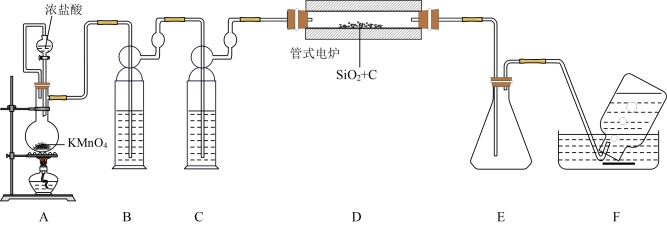
①A中制取Cl2反应的离子方程式为_______ 。
②B中盛放的试剂是_______ 。
③F中收集到的气体是CO,制备SiCl4的化学方程式为_______ 。
④上述设计的装置有一处明显不妥,改进的方法是_______ 。
(2)制备(CH3COO)4Si的反应装置如图所示。将一定量的SiCl4放入仪器a中,在电磁搅拌下,由滴液漏斗滴入过量的乙酸酐,关闭活塞。SiCl4和(CH3CO)2O的反应为放热反应,反应后反应混合物带色,并开始析出(CH3COO)4Si晶体。
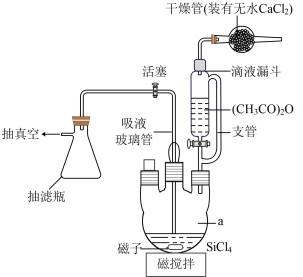
①仪器a的名称为_______ ;图中支管的作用是_______ 。
②写出生成(CH3COO)4Si的化学方程式:_______ (生成物有两种)。
③完成反应后,将反应混合液放置数日,再用干冰-丙酮浴冷却后,将导管伸入液面以下,_______ (结合装置图填写操作),获得(CH3COO)4Si晶体粗品,若得到较纯 (CH3COO)4Si,则下一步操作为_______ 。
(1)制备SiCl4装置(部分夹持仪器已省路)如下:

①A中制取Cl2反应的离子方程式为
②B中盛放的试剂是
③F中收集到的气体是CO,制备SiCl4的化学方程式为
④上述设计的装置有一处明显不妥,改进的方法是
(2)制备(CH3COO)4Si的反应装置如图所示。将一定量的SiCl4放入仪器a中,在电磁搅拌下,由滴液漏斗滴入过量的乙酸酐,关闭活塞。SiCl4和(CH3CO)2O的反应为放热反应,反应后反应混合物带色,并开始析出(CH3COO)4Si晶体。

①仪器a的名称为
②写出生成(CH3COO)4Si的化学方程式:
③完成反应后,将反应混合液放置数日,再用干冰-丙酮浴冷却后,将导管伸入液面以下,
您最近一年使用:0次
2022-06-10更新
|
593次组卷
|
2卷引用:天津市2023届普通高中学业水平等级性考试模拟化学试题
7 . 设NA为阿伏加德罗常数的值。下列说法 正确的是
| A.44.8 L丙烯和44.8 L丙烷中含有的碳原子数均为6NA |
| B.将1mol明矾完全溶于水,所得溶液中阴离子总数小于2NA |
| C.12.8g铜完全溶于未知浓度的硝酸中,转移的电子数为0.4NA |
D.1 mol苯乙烯(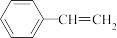 )与足量H2在催化剂和加热条件下反应,形成C- H键的数目最多为2 NA )与足量H2在催化剂和加热条件下反应,形成C- H键的数目最多为2 NA |
您最近一年使用:0次
2022-06-09更新
|
867次组卷
|
2卷引用:天津市2023届普通高中学业水平等级性考试模拟化学试题
名校
解题方法
8 . 如图为某烃的键线式结构,下列说法错误的是
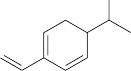
| A.该烃与环己二烯相差5个“CH2”基团 |
| B.一定条件下,能发生加聚反应 |
| C.苯环上只有一个取代基的同分异构体共有8种 |
| D.该烃和Br2按物质的量之比1:1加成时,所得产物共有5种 |
您最近一年使用:0次
2022-05-11更新
|
2711次组卷
|
9卷引用:天津市2023届普通高中学业水平等级性考试模拟化学试题
天津市2023届普通高中学业水平等级性考试模拟化学试题安徽师范大学附属中学2021-2022学年高二下学期期中考试化学试题重庆市缙云教育联盟2022-2023学年高三上学期8月质量检测化学试题(已下线)第33讲 烃和卤代烃(讲)-2023年高考化学一轮复习讲练测(全国通用)黑龙江省齐齐哈尔三立高中2022-2023学年高一下学期期初考试化学试题甘肃省张掖市高台县第一中学2022-2023学年高二下学期7月月考化学试题吉林省长春市第五中学2022-2023学年高一下学期期末考试化学试题内蒙古呼伦贝尔市满洲里市第一中学2022-2023学年高二下学期期末考试化学试题福建省泉州市永春第一中学2023-2024学年高二下学期4月期中考试化学试题
解题方法
9 . 研究氮和碳的化合物对工业生产和防治污染有重要意义,回答下列问题:
(1)利用 的还原性可以消除氮氧化物的污染,其中除去
的还原性可以消除氮氧化物的污染,其中除去 的主要反应如下:
的主要反应如下: 。某研究小组将
。某研究小组将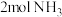 、
、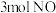 和一定量的
和一定量的 充入
充入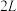 密闭容器中,在
密闭容器中,在 催化剂表面发生上述反应,
催化剂表面发生上述反应, 的转化率随温度变化的情况如图所示:
的转化率随温度变化的情况如图所示:

①温度从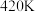 升高到
升高到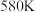 用时
用时 ,则此时段内
,则此时段内 的平均反应速率
的平均反应速率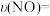
_______ ;
②在有氧条件下,温度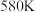 之后
之后 生成
生成 的转化率降低的原因可能是
的转化率降低的原因可能是_______ 。
(2)研究表明,氮氧化物( )和二氧化硫都与大气中雾霾的形成有关。已知:
)和二氧化硫都与大气中雾霾的形成有关。已知: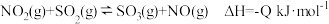 ,一定温度下,向2L恒容密闭容器中充入
,一定温度下,向2L恒容密闭容器中充入 和
和 各
各 ,
, 达到平衡,此时容器中
达到平衡,此时容器中 和
和 的浓度之比为1∶3,则
的浓度之比为1∶3,则 的平衡转化率是
的平衡转化率是_____ ;若在该温度下,向2L恒容密闭容器中充入 、
、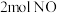 ,则达平衡时吸收的热量=
,则达平衡时吸收的热量=_____  。
。
(3)研究人员开发了一种新型的硼、氮共掺杂的多孔石墨烯材料作为正极催化剂的锂-二氧化碳二次电池,实现了碳酸锂在电池中的高度可逆分解其装置示意图如图所示。

放电时,正极反应式为_____ 。
(4)砷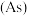 是第四周期ⅤA族元素,其化合物,有着广泛的用途。
是第四周期ⅤA族元素,其化合物,有着广泛的用途。 时,将
时,将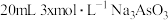 、
、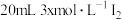 和
和 溶液混合,发生反应:
溶液混合,发生反应: 。溶液中
。溶液中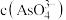 与反应时间(t)的关系如图所示。
与反应时间(t)的关系如图所示。

①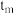 时v逆)
时v逆)_______ 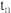 时v(逆),(填“大于”“小于”或“等于”)
时v(逆),(填“大于”“小于”或“等于”)
②若平衡时溶液的 ,则该反应的平衡常数K为
,则该反应的平衡常数K为_______ 。(用x、y表示)
(1)利用
 的还原性可以消除氮氧化物的污染,其中除去
的还原性可以消除氮氧化物的污染,其中除去 的主要反应如下:
的主要反应如下: 。某研究小组将
。某研究小组将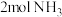 、
、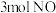 和一定量的
和一定量的 充入
充入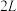 密闭容器中,在
密闭容器中,在 催化剂表面发生上述反应,
催化剂表面发生上述反应, 的转化率随温度变化的情况如图所示:
的转化率随温度变化的情况如图所示:
①温度从
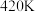 升高到
升高到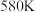 用时
用时 ,则此时段内
,则此时段内 的平均反应速率
的平均反应速率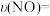
②在有氧条件下,温度
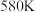 之后
之后 生成
生成 的转化率降低的原因可能是
的转化率降低的原因可能是(2)研究表明,氮氧化物(
 )和二氧化硫都与大气中雾霾的形成有关。已知:
)和二氧化硫都与大气中雾霾的形成有关。已知: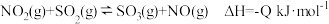 ,一定温度下,向2L恒容密闭容器中充入
,一定温度下,向2L恒容密闭容器中充入 和
和 各
各 ,
, 达到平衡,此时容器中
达到平衡,此时容器中 和
和 的浓度之比为1∶3,则
的浓度之比为1∶3,则 的平衡转化率是
的平衡转化率是 、
、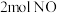 ,则达平衡时吸收的热量=
,则达平衡时吸收的热量= 。
。(3)研究人员开发了一种新型的硼、氮共掺杂的多孔石墨烯材料作为正极催化剂的锂-二氧化碳二次电池,实现了碳酸锂在电池中的高度可逆分解其装置示意图如图所示。

放电时,正极反应式为
(4)砷
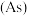 是第四周期ⅤA族元素,其化合物,有着广泛的用途。
是第四周期ⅤA族元素,其化合物,有着广泛的用途。 时,将
时,将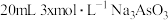 、
、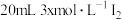 和
和 溶液混合,发生反应:
溶液混合,发生反应: 。溶液中
。溶液中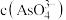 与反应时间(t)的关系如图所示。
与反应时间(t)的关系如图所示。
①
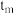 时v逆)
时v逆)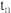 时v(逆),(填“大于”“小于”或“等于”)
时v(逆),(填“大于”“小于”或“等于”)②若平衡时溶液的
 ,则该反应的平衡常数K为
,则该反应的平衡常数K为
您最近一年使用:0次
2021-03-24更新
|
269次组卷
|
2卷引用:天津市2023届普通高中学业水平等级性考试模拟化学试题
10 . 近期,天津大学张兵教授等人通过将二氧化碳电还原反应与辛胺氧化反应耦合,实现了两电极体系中甲酸和辛腈的高选择性合成.反应体系示意图如图所示:

下列说法正确的是

下列说法正确的是
| A.电极b与电源负极相连 |
| B.转移1mol电子可消耗11.2LCO2(标况下) |
| C.Al与Ga是相邻的同主族元素,其原子序数相差8 |
| D.该反应装置能有效利用CO2,从而减弱因CO2导致的酸雨问题 |
您最近一年使用:0次
2021-01-09更新
|
351次组卷
|
2卷引用:天津市2023届普通高中学业水平等级性考试模拟化学试题



