实验室研究从医用废感光胶片中回收银的方法。
(1)银的浸出 溶液与
溶液与 溶液直接混合能发生氧化还原反应:
溶液直接混合能发生氧化还原反应:
ii. 。
。
① 溶液将胶片上的单质银转化为
溶液将胶片上的单质银转化为 ,其离子方程式是
,其离子方程式是___________ 。
② 溶液能溶解
溶液能溶解 并得到含
并得到含 的浸出液。结合平衡移动原理解释
的浸出液。结合平衡移动原理解释 溶解的原因:
溶解的原因:___________ 。
Ⅱ.一步法:用水溶解 和乙二胺四乙酸二钠(用
和乙二胺四乙酸二钠(用 表示)的混合固体,调节
表示)的混合固体,调节 形成
形成 溶液,再加入一定量
溶液,再加入一定量 ,配成浸取液。将废感光胶片浸入浸取液中,发生反应:
,配成浸取液。将废感光胶片浸入浸取液中,发生反应:
 。
。
③从物质氧化性或还原性的角度分析加入 的作用:
的作用:___________ 。
(2)银的还原
调节(1)所得浸出液 ,向其中加入
,向其中加入 溶液(B的化合价为
溶液(B的化合价为 )至不再产生黑色沉淀,过滤得到粗银:滤液中的
)至不再产生黑色沉淀,过滤得到粗银:滤液中的 可以循环使用。补全离子方程式:
可以循环使用。补全离子方程式:___________ 。

(3)银浸出率的测定
称取 洗净干燥的原胶片,灼烧灰化后用
洗净干燥的原胶片,灼烧灰化后用 溶解,过滤。滤液用
溶解,过滤。滤液用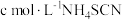 标准溶液滴定至终点,消耗标准溶液
标准溶液滴定至终点,消耗标准溶液 。另取
。另取 洗净干燥的浸取后胶片,用同样方法处理,滴定,消耗
洗净干燥的浸取后胶片,用同样方法处理,滴定,消耗 标准溶液
标准溶液 。(已知:
。(已知: )
)
银的浸出率
___________ (列出计算表达式)。
(1)银的浸出
I、两步法:
 溶液与
溶液与 溶液直接混合能发生氧化还原反应:
溶液直接混合能发生氧化还原反应:ii.
 。
。①
 溶液将胶片上的单质银转化为
溶液将胶片上的单质银转化为 ,其离子方程式是
,其离子方程式是②
 溶液能溶解
溶液能溶解 并得到含
并得到含 的浸出液。结合平衡移动原理解释
的浸出液。结合平衡移动原理解释 溶解的原因:
溶解的原因:Ⅱ.一步法:用水溶解
 和乙二胺四乙酸二钠(用
和乙二胺四乙酸二钠(用 表示)的混合固体,调节
表示)的混合固体,调节 形成
形成 溶液,再加入一定量
溶液,再加入一定量 ,配成浸取液。将废感光胶片浸入浸取液中,发生反应:
,配成浸取液。将废感光胶片浸入浸取液中,发生反应: 。
。③从物质氧化性或还原性的角度分析加入
 的作用:
的作用:(2)银的还原
调节(1)所得浸出液
 ,向其中加入
,向其中加入 溶液(B的化合价为
溶液(B的化合价为 )至不再产生黑色沉淀,过滤得到粗银:滤液中的
)至不再产生黑色沉淀,过滤得到粗银:滤液中的 可以循环使用。补全离子方程式:
可以循环使用。补全离子方程式:
(3)银浸出率的测定
称取
 洗净干燥的原胶片,灼烧灰化后用
洗净干燥的原胶片,灼烧灰化后用 溶解,过滤。滤液用
溶解,过滤。滤液用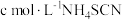 标准溶液滴定至终点,消耗标准溶液
标准溶液滴定至终点,消耗标准溶液 。另取
。另取 洗净干燥的浸取后胶片,用同样方法处理,滴定,消耗
洗净干燥的浸取后胶片,用同样方法处理,滴定,消耗 标准溶液
标准溶液 。(已知:
。(已知: )
)银的浸出率

更新时间:2024-05-07 17:13:03
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
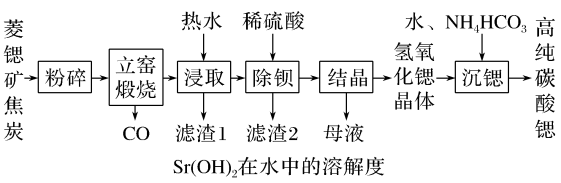
【推荐1】碳酸锶(SrCO3)是一种重要的工业原料,广泛用于生产锶铁氧体磁性材料。一种以菱锶矿(含80~90%SrCO3,少量MgCO3、CaCO3、BaCO3等)制备高纯碳酸锶的工艺流程如图:
(1)元素Sr在元素周期表的位置_______ 。
(2)菱锶矿、焦炭混合粉碎的目的是_______ 。
(3)“立窑煅烧”中SrCO3与焦炭反应生成两种氧化物,则该反应的化学方程式为_______ 。
(4)“浸取”中用热水浸取而不用冷水的原因是_______ 。
(5)“沉锶”中反应的化学方程式为_______ 。
(6)锶铁氧体是由锶和铁的氧化物组成的复合磁性材料。某种锶铁氧体(xSrO·yFe2O3)中Sr与Fe的质量比为0.13,则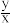 为
为_______ (取整数)。

| 温度/℃ | 10 | 20 | 30 | 40 | 60 | 80 | 90 | 100 |
| 溶解度/(g/100g) | 1.25 | 1.77 | 2.64 | 3.95 | 8.42 | 20.2 | 44.5 | 91.2 |
(2)菱锶矿、焦炭混合粉碎的目的是
(3)“立窑煅烧”中SrCO3与焦炭反应生成两种氧化物,则该反应的化学方程式为
(4)“浸取”中用热水浸取而不用冷水的原因是
(5)“沉锶”中反应的化学方程式为
(6)锶铁氧体是由锶和铁的氧化物组成的复合磁性材料。某种锶铁氧体(xSrO·yFe2O3)中Sr与Fe的质量比为0.13,则
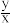 为
为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】氧钒(IV)碱式碳酸铵晶体化学式为:(NH4)5[(VO)6(CO3)4(OH)9]·10H2O,实验室以V2O5为原料制备该晶体的流程如图:
V2O5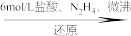 VOCl2溶液
VOCl2溶液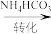 氧钒(IV)碱式碳酸铵晶体
氧钒(IV)碱式碳酸铵晶体
(1)N2H4的电子式是_______ 。若“还原”后其它产物均绿色环保,写出该反应的化学方程式_______  。
。
(2)“转化”可在如图装置中进行。(已知VO2+能被O2氧化)
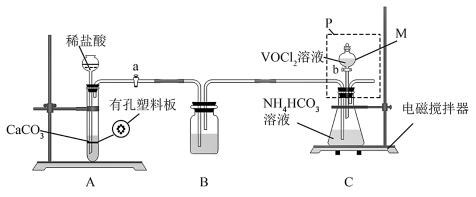
①仪器M的名称是_______ 。使A中制气反应停止的操作是_______ 。
②装置C中将VOCl2转化并得到产品,实验操作顺序为:打开活塞a→_______ →_______ →_______ .(填标号)。
I.取下P(如图),锥形瓶口塞上橡胶塞
II.将锥形瓶置于干燥器中,静置后过滤
III.打开活塞b,加入VOCl2溶液,持续搅拌一段时间,使反应完全
③得到紫红色晶体,抽滤,并用饱和NH4HCO3溶液洗涤3次,用无水乙醇洗涤2次,再用乙醚洗涤2次,抽干称重。用饱和NH4HCO3溶液洗涤除去的阴离子主要是_______ (填离子符号),用乙醚洗涤的目的是_______ 。
④称量mg产品于锥形瓶中,先将产品中钒元素转化为VO ,消除其它干扰,再用cmol·L-1(NH4)2Fe(SO4)2标准溶液滴定至终点,消耗标准溶液的体积为VmL(已知滴定反应为VO
,消除其它干扰,再用cmol·L-1(NH4)2Fe(SO4)2标准溶液滴定至终点,消耗标准溶液的体积为VmL(已知滴定反应为VO +Fe2++2H+=VO2++Fe3++H2O).则产品中钒的质量分数为
+Fe2++2H+=VO2++Fe3++H2O).则产品中钒的质量分数为_______ (以VO2+的量进行计算,列出计算式)。
V2O5
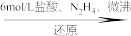 VOCl2溶液
VOCl2溶液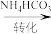 氧钒(IV)碱式碳酸铵晶体
氧钒(IV)碱式碳酸铵晶体(1)N2H4的电子式是
 。
。(2)“转化”可在如图装置中进行。(已知VO2+能被O2氧化)

①仪器M的名称是
②装置C中将VOCl2转化并得到产品,实验操作顺序为:打开活塞a→
I.取下P(如图),锥形瓶口塞上橡胶塞
II.将锥形瓶置于干燥器中,静置后过滤
III.打开活塞b,加入VOCl2溶液,持续搅拌一段时间,使反应完全
③得到紫红色晶体,抽滤,并用饱和NH4HCO3溶液洗涤3次,用无水乙醇洗涤2次,再用乙醚洗涤2次,抽干称重。用饱和NH4HCO3溶液洗涤除去的阴离子主要是
④称量mg产品于锥形瓶中,先将产品中钒元素转化为VO
 ,消除其它干扰,再用cmol·L-1(NH4)2Fe(SO4)2标准溶液滴定至终点,消耗标准溶液的体积为VmL(已知滴定反应为VO
,消除其它干扰,再用cmol·L-1(NH4)2Fe(SO4)2标准溶液滴定至终点,消耗标准溶液的体积为VmL(已知滴定反应为VO +Fe2++2H+=VO2++Fe3++H2O).则产品中钒的质量分数为
+Fe2++2H+=VO2++Fe3++H2O).则产品中钒的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】实验室用浓盐酸和 制
制 ,并以干燥的
,并以干燥的 为原料制备
为原料制备 ,装置如下图所示。回答下列问题:
,装置如下图所示。回答下列问题:
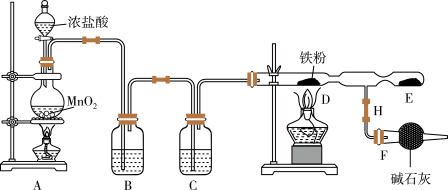
已知: 固体易升华,易吸收水分而潮解变质。请回答下列问题:
固体易升华,易吸收水分而潮解变质。请回答下列问题:
(1)连接好仪器后首先应进行的操作是_______ ;图中盛放碱石灰的仪器是_______ 。
(2)写出装置A中发生的离子方程式_______ 。
(3)装置B中盛放的试剂是_______ 。F装置所起的作用是_______ 。
(4)实验时,先点燃_______ 处的酒精灯,再点燃_______ 处酒精灯,D处发生的现象是_______ 。
(5)已知 与浓盐酸在常温下反应就可制取氯气:_______
与浓盐酸在常温下反应就可制取氯气:_______ _______
_______ (浓)= _______
(浓)= _______ _______
_______ _______
_______ _______
_______
①配平上述化学方程式,并用单线桥标出电子转移的情况。_________
②当生成标准状况下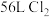 时对应转移的电子数为
时对应转移的电子数为_______ 。
 制
制 ,并以干燥的
,并以干燥的 为原料制备
为原料制备 ,装置如下图所示。回答下列问题:
,装置如下图所示。回答下列问题:
已知:
 固体易升华,易吸收水分而潮解变质。请回答下列问题:
固体易升华,易吸收水分而潮解变质。请回答下列问题:(1)连接好仪器后首先应进行的操作是
(2)写出装置A中发生的离子方程式
(3)装置B中盛放的试剂是
(4)实验时,先点燃
(5)已知
 与浓盐酸在常温下反应就可制取氯气:_______
与浓盐酸在常温下反应就可制取氯气:_______ _______
_______ (浓)= _______
(浓)= _______ _______
_______ _______
_______ _______
_______
①配平上述化学方程式,并用单线桥标出电子转移的情况。
②当生成标准状况下
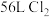 时对应转移的电子数为
时对应转移的电子数为
您最近一年使用:0次
【推荐1】已知氢氧化钙和钨酸钙(CaWO4)都是微溶电解质,两者的溶解度均随温度升高而减小。在钨冶炼工艺中,将氢氧化钙加入钨酸钠碱性溶液中得到钨酸钙,发生反应Ⅰ: (aq)+Ca(OH)2(s)
(aq)+Ca(OH)2(s) CaWO4(s)+2OH-(aq)
CaWO4(s)+2OH-(aq)
(1)如图为不同温度下Ca(OH)2、CaWO4 的沉淀溶解平衡曲线。

①计算T1时,Ksp(CaWO4)=________ 。
②T1________ T2(填“>”“=”或“<”)。
(2)反应Ⅰ的平衡常数K理论值如表:
①该反应平衡常数K的表达式为________ 。
②该反应的ΔH________ 0(“>”“=”或“<”)。
③由于溶液中离子间的相互作用,实验测得的平衡常数与理论值相距甚远。50℃时,向一定体积的钨酸钠碱性溶液[c(Na2WO4)=c(NaOH)=0.5 mol·L-1]中,加入过量Ca(OH)2,反应达到平衡后 的沉淀率为60%,此时
的沉淀率为60%,此时 的平衡浓度为
的平衡浓度为________ mol·L-1,实验测得的平衡常数为________ (保留小数点后两位)。
(3)制取钨酸钙时,适时向反应混合液中添加适量盐酸,其作用是________ 。
 (aq)+Ca(OH)2(s)
(aq)+Ca(OH)2(s) CaWO4(s)+2OH-(aq)
CaWO4(s)+2OH-(aq)(1)如图为不同温度下Ca(OH)2、CaWO4 的沉淀溶解平衡曲线。

①计算T1时,Ksp(CaWO4)=
②T1
(2)反应Ⅰ的平衡常数K理论值如表:
| 温度/℃ | 25 | 50 | 90 | 100 |
| K | 79.96 | 208.06 | 222.88 | 258.05 |
①该反应平衡常数K的表达式为
②该反应的ΔH
③由于溶液中离子间的相互作用,实验测得的平衡常数与理论值相距甚远。50℃时,向一定体积的钨酸钠碱性溶液[c(Na2WO4)=c(NaOH)=0.5 mol·L-1]中,加入过量Ca(OH)2,反应达到平衡后
 的沉淀率为60%,此时
的沉淀率为60%,此时 的平衡浓度为
的平衡浓度为(3)制取钨酸钙时,适时向反应混合液中添加适量盐酸,其作用是
您最近一年使用:0次
【推荐2】2019年诺贝尔化学奖颁给了为锂电池发展作出突出贡献的三位科学家。某废旧锂电池正极主要由LiFePO4、铝箔、炭黑等组成,Fe、Li、P具有极高的回收价值,具体流程如下:

(1)过程ⅰ生成NaAlO2溶液的离子方程式是________ 。
(2)过程ⅱ中HCl/H2O2的作用是_________ 。
(3)浸出液X的主要成分为Li+、Fe3+、 等。过程ⅲ控制碳酸钠溶液浓度20%、温度85℃、反应时间3h条件下,探究pH对磷酸铁沉淀的影响,如下图所示。
等。过程ⅲ控制碳酸钠溶液浓度20%、温度85℃、反应时间3h条件下,探究pH对磷酸铁沉淀的影响,如下图所示。
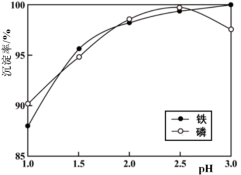
①综合考虑铁和磷沉淀率,最佳pH为_________ 。
②当pH>2.5后,随pH增加,磷沉淀率出现了减小的趋势,解释其原因_________ 。
(4)LiFePO4可以通过(NH4)2Fe(SO4)2、H3PO4与LiOH溶液发生共沉淀反应制取,共沉淀反应的化学方程式为__________ 。

(1)过程ⅰ生成NaAlO2溶液的离子方程式是
(2)过程ⅱ中HCl/H2O2的作用是
(3)浸出液X的主要成分为Li+、Fe3+、
 等。过程ⅲ控制碳酸钠溶液浓度20%、温度85℃、反应时间3h条件下,探究pH对磷酸铁沉淀的影响,如下图所示。
等。过程ⅲ控制碳酸钠溶液浓度20%、温度85℃、反应时间3h条件下,探究pH对磷酸铁沉淀的影响,如下图所示。
①综合考虑铁和磷沉淀率,最佳pH为
②当pH>2.5后,随pH增加,磷沉淀率出现了减小的趋势,解释其原因
(4)LiFePO4可以通过(NH4)2Fe(SO4)2、H3PO4与LiOH溶液发生共沉淀反应制取,共沉淀反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】电解金属锰阳极渣(主要成分 ,杂质为Pb,Fe、Cu元素的化合物)和黄铁矿(
,杂质为Pb,Fe、Cu元素的化合物)和黄铁矿( )为原料可制备
)为原料可制备 ,其流程如图所示:
,其流程如图所示:
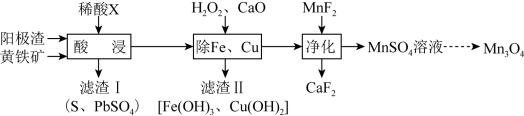
已知: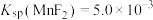 ,
, ,回答下列问题:
,回答下列问题:
(1)“酸浸”时,所用的稀酸X是___________ 。
(2)“除Fe、Cu”过程中加入 溶液时,发生反应的离子方程式为
溶液时,发生反应的离子方程式为___________ 。加入氧化钙的目的是除去铁和铜元素,用化学平衡移动原理解释除去铁元素的原理___________ 。
(3)“净化”过程反应的离子方程式为___________ ,若“净化”过程中 的浓度为2mol/L,则此时
的浓度为2mol/L,则此时 的浓度为
的浓度为___________ mol/L。
(4)“酸浸”过程中, 、
、 的质量浓度、Mn浸出率与时间的关系如图1所示。20~80min内,浸出Mn元素的主要离子方程式为
的质量浓度、Mn浸出率与时间的关系如图1所示。20~80min内,浸出Mn元素的主要离子方程式为___________ 。

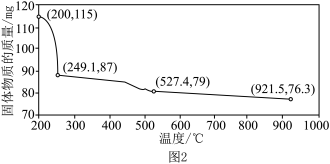
(5)碳酸锰在空气中加热可以生成相应的氧化物,称取115mg碳酸锰(摩尔质量115g/mol)加热,固体物质的质量随温度的变化如图2所示。527.4℃时, 生成相应固体物质的化学方程式为
生成相应固体物质的化学方程式为________ 。
 ,杂质为Pb,Fe、Cu元素的化合物)和黄铁矿(
,杂质为Pb,Fe、Cu元素的化合物)和黄铁矿( )为原料可制备
)为原料可制备 ,其流程如图所示:
,其流程如图所示:
已知:
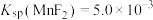 ,
, ,回答下列问题:
,回答下列问题:(1)“酸浸”时,所用的稀酸X是
(2)“除Fe、Cu”过程中加入
 溶液时,发生反应的离子方程式为
溶液时,发生反应的离子方程式为(3)“净化”过程反应的离子方程式为
 的浓度为2mol/L,则此时
的浓度为2mol/L,则此时 的浓度为
的浓度为(4)“酸浸”过程中,
 、
、 的质量浓度、Mn浸出率与时间的关系如图1所示。20~80min内,浸出Mn元素的主要离子方程式为
的质量浓度、Mn浸出率与时间的关系如图1所示。20~80min内,浸出Mn元素的主要离子方程式为
(5)碳酸锰在空气中加热可以生成相应的氧化物,称取115mg碳酸锰(摩尔质量115g/mol)加热,固体物质的质量随温度的变化如图2所示。527.4℃时,
 生成相应固体物质的化学方程式为
生成相应固体物质的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】工业上利用碳酸锰矿(主要成分为MnCO3,还含有Fe、Mg、Ca的碳酸盐、Cu、Ni、Al的氧化物及少量不溶杂质)制备硫酸锰,其工艺流程如下:

请回答下列问题:
(1)“酸浸”中MnCO3溶解的离子方程式为___________ 。为提高“酸浸”速率,下列措施不可行的是___________ (选填序号)。
A.升温 B.采用高压氧酸浸 C.使用98%的浓硫酸 D.将矿石粉碎成小块
(2)“除铝铁”步骤中加入MnO2发生反应的离子方程式为___________ 。
(3)加入氨水调节pH与铝铁去除率、锰损失率的关系如图所示,则应调节的pH范围为___________ (选填序号)。

A.1~2 B.2~3 C.3~4 D.4~5
已知在此条件下Mn2+不会产生沉淀,推测锰元素损失的可能原因是___________ 。
(4)“除铜镍”步骤可以加入硫化铵将Cu、Ni元素除去,其缺点是___________ 。造成锰元素损失,产率下降。实际生产采用SDD代替。
(5)“结晶分离”步骤所得滤渣主要成分是___________ 。
(6)为确定所得硫酸锰中含有的结晶水,称取纯化后的硫酸锰晶体8.45g,加热至完全脱去结晶水,固体减重0.9g,则该硫酸锰晶体的化学式为___________ 。

请回答下列问题:
(1)“酸浸”中MnCO3溶解的离子方程式为
A.升温 B.采用高压氧酸浸 C.使用98%的浓硫酸 D.将矿石粉碎成小块
(2)“除铝铁”步骤中加入MnO2发生反应的离子方程式为
(3)加入氨水调节pH与铝铁去除率、锰损失率的关系如图所示,则应调节的pH范围为

A.1~2 B.2~3 C.3~4 D.4~5
已知在此条件下Mn2+不会产生沉淀,推测锰元素损失的可能原因是
(4)“除铜镍”步骤可以加入硫化铵将Cu、Ni元素除去,其缺点是
(5)“结晶分离”步骤所得滤渣主要成分是
(6)为确定所得硫酸锰中含有的结晶水,称取纯化后的硫酸锰晶体8.45g,加热至完全脱去结晶水,固体减重0.9g,则该硫酸锰晶体的化学式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】某兴趣小组利用废旧电池的铜帽(铜锌总含量约99%)制备了CuSO4·5H2O样品,制备流程如下:
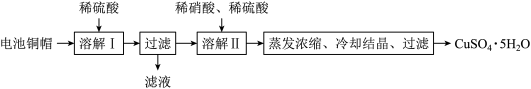
(1)“溶解Ⅱ”过程中,发生反应的离子方程式为___ 。
(2)“溶解Ⅱ”过程中应控制反应温度,温度不能过高的原因是___ 。
(3)为测定所得CuSO4·5H2O样品的纯度,兴趣小组进行了如下实验:称取2.540g样品,配制成250mL溶液,取25.00mL溶液于锥形瓶中,加入过量KI并充分振荡后,滴加几滴淀粉溶液,再滴入0.0400mol·L-1的Na2S2O3溶液至刚好完全反应,恰好完全反应时消耗Na2S2O3溶液的体积为25.00 mL。实验过程中发生的反应如下:2Cu2++4I-=2CuI↓+I2、2S2O32-+I2=S4O62-+2I-
①配制250mL溶液所需的玻璃仪器除烧杯、胶头滴管外还有___ 。
②计算出样品中CuSO4·5H2O的质量分数。___ (写出计算过程)

(1)“溶解Ⅱ”过程中,发生反应的离子方程式为
(2)“溶解Ⅱ”过程中应控制反应温度,温度不能过高的原因是
(3)为测定所得CuSO4·5H2O样品的纯度,兴趣小组进行了如下实验:称取2.540g样品,配制成250mL溶液,取25.00mL溶液于锥形瓶中,加入过量KI并充分振荡后,滴加几滴淀粉溶液,再滴入0.0400mol·L-1的Na2S2O3溶液至刚好完全反应,恰好完全反应时消耗Na2S2O3溶液的体积为25.00 mL。实验过程中发生的反应如下:2Cu2++4I-=2CuI↓+I2、2S2O32-+I2=S4O62-+2I-
①配制250mL溶液所需的玻璃仪器除烧杯、胶头滴管外还有
②计算出样品中CuSO4·5H2O的质量分数。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】硫代硫酸钠(Na2S2O3)具有较强的还原性,还能与中强酸反应,在精细化工领域应用广泛.将SO2通入按一定比例配制成的Na2S和Na2CO3的混合溶液中,可制得Na2S2O3•5H2O(大苏打).

(1)实验室用Na2SO3和硫酸制备SO2,可选用的气体发生装置是_____ (选填编号);检查该装置气密性的操作是:关闭止水夹,再_______________ 。
(2)在Na2S和Na2CO3的混合溶液中不断通入SO2气体的过程中,发现:
①浅黄色沉淀先逐渐增多,反应的化学方程式为________________ (生成的盐为正盐);
②浅黄色沉淀保持一段时间不变,有无色无嗅的气体产生,则反应的化学方程式为__________________ (生成的盐为正盐);
③浅黄色沉淀逐渐减少(这时有Na2S2O3生成);
④继续通入SO2,浅黄色沉淀又会逐渐增多,反应的化学方程式为_______________ (生成的盐为酸式盐)。
(3)制备Na2S2O3时,为了使反应物利用率最大化,Na2S和Na2CO3的物质的量之比应为_________ ;通过反应顺序,可比较出:温度相同时,同物质的量浓度的Na2S溶液和Na2CO3溶液pH更大的是_________ 。
(4)硫代硫酸钠的纯度可用滴定法进行测定,原理是:2S2O32﹣+I3﹣=S4O62﹣+3I﹣.
①为保证不变质,配制硫代硫酸钠溶液须用新煮沸并冷却的蒸馏水,其理由是___________ 。
②取2.500g含杂质的Na2S2O3•5H2O晶体配成50mL溶液,每次取10.00mL用0.0500mol/L KI3溶液滴定(以淀粉为指示剂),实验数据如下(第3次初读数为0.00,终点读数如图e;杂质不参加反应):
到达滴定终点的现象是_______________ ;Na2S2O3•5H2O(式量248)的质量分数是(保留4位小数)__________ 。

(1)实验室用Na2SO3和硫酸制备SO2,可选用的气体发生装置是
(2)在Na2S和Na2CO3的混合溶液中不断通入SO2气体的过程中,发现:
①浅黄色沉淀先逐渐增多,反应的化学方程式为
②浅黄色沉淀保持一段时间不变,有无色无嗅的气体产生,则反应的化学方程式为
③浅黄色沉淀逐渐减少(这时有Na2S2O3生成);
④继续通入SO2,浅黄色沉淀又会逐渐增多,反应的化学方程式为
(3)制备Na2S2O3时,为了使反应物利用率最大化,Na2S和Na2CO3的物质的量之比应为
(4)硫代硫酸钠的纯度可用滴定法进行测定,原理是:2S2O32﹣+I3﹣=S4O62﹣+3I﹣.
①为保证不变质,配制硫代硫酸钠溶液须用新煮沸并冷却的蒸馏水,其理由是
②取2.500g含杂质的Na2S2O3•5H2O晶体配成50mL溶液,每次取10.00mL用0.0500mol/L KI3溶液滴定(以淀粉为指示剂),实验数据如下(第3次初读数为0.00,终点读数如图e;杂质不参加反应):
| 编号 | 1 | 2 | 3 |
| 消耗KI3溶液的体积/mL | 19.98 | 20.02 |
到达滴定终点的现象是
您最近一年使用:0次



