氧钒(IV)碱式碳酸铵晶体化学式为:(NH4)5[(VO)6(CO3)4(OH)9]·10H2O,实验室以V2O5为原料制备该晶体的流程如图:
V2O5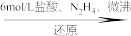 VOCl2溶液
VOCl2溶液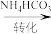 氧钒(IV)碱式碳酸铵晶体
氧钒(IV)碱式碳酸铵晶体
(1)N2H4的电子式是_______ 。若“还原”后其它产物均绿色环保,写出该反应的化学方程式_______  。
。
(2)“转化”可在如图装置中进行。(已知VO2+能被O2氧化)
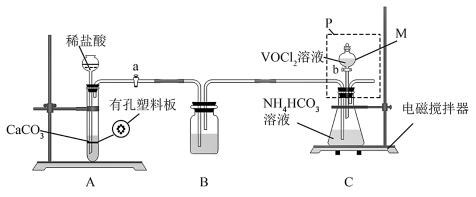
①仪器M的名称是_______ 。使A中制气反应停止的操作是_______ 。
②装置C中将VOCl2转化并得到产品,实验操作顺序为:打开活塞a→_______ →_______ →_______ .(填标号)。
I.取下P(如图),锥形瓶口塞上橡胶塞
II.将锥形瓶置于干燥器中,静置后过滤
III.打开活塞b,加入VOCl2溶液,持续搅拌一段时间,使反应完全
③得到紫红色晶体,抽滤,并用饱和NH4HCO3溶液洗涤3次,用无水乙醇洗涤2次,再用乙醚洗涤2次,抽干称重。用饱和NH4HCO3溶液洗涤除去的阴离子主要是_______ (填离子符号),用乙醚洗涤的目的是_______ 。
④称量mg产品于锥形瓶中,先将产品中钒元素转化为VO ,消除其它干扰,再用cmol·L-1(NH4)2Fe(SO4)2标准溶液滴定至终点,消耗标准溶液的体积为VmL(已知滴定反应为VO
,消除其它干扰,再用cmol·L-1(NH4)2Fe(SO4)2标准溶液滴定至终点,消耗标准溶液的体积为VmL(已知滴定反应为VO +Fe2++2H+=VO2++Fe3++H2O).则产品中钒的质量分数为
+Fe2++2H+=VO2++Fe3++H2O).则产品中钒的质量分数为_______ (以VO2+的量进行计算,列出计算式)。
V2O5
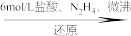 VOCl2溶液
VOCl2溶液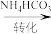 氧钒(IV)碱式碳酸铵晶体
氧钒(IV)碱式碳酸铵晶体(1)N2H4的电子式是
 。
。(2)“转化”可在如图装置中进行。(已知VO2+能被O2氧化)

①仪器M的名称是
②装置C中将VOCl2转化并得到产品,实验操作顺序为:打开活塞a→
I.取下P(如图),锥形瓶口塞上橡胶塞
II.将锥形瓶置于干燥器中,静置后过滤
III.打开活塞b,加入VOCl2溶液,持续搅拌一段时间,使反应完全
③得到紫红色晶体,抽滤,并用饱和NH4HCO3溶液洗涤3次,用无水乙醇洗涤2次,再用乙醚洗涤2次,抽干称重。用饱和NH4HCO3溶液洗涤除去的阴离子主要是
④称量mg产品于锥形瓶中,先将产品中钒元素转化为VO
 ,消除其它干扰,再用cmol·L-1(NH4)2Fe(SO4)2标准溶液滴定至终点,消耗标准溶液的体积为VmL(已知滴定反应为VO
,消除其它干扰,再用cmol·L-1(NH4)2Fe(SO4)2标准溶液滴定至终点,消耗标准溶液的体积为VmL(已知滴定反应为VO +Fe2++2H+=VO2++Fe3++H2O).则产品中钒的质量分数为
+Fe2++2H+=VO2++Fe3++H2O).则产品中钒的质量分数为
更新时间:2021/03/12 14:47:38
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
【推荐1】废旧电路板主要含有塑料。Fe、Cu、SnO2、PbO2等,研究人员一种从处理废旧电路板中回收金属锡(Sn)的流程如下。

已知:Sn和Pb位于周期表第IVA族;SnO2,PbO2可与强碱共热反应生成易溶盐和水。
(1)“焙烧”的主要目的是___________ 。
(2)“滤渣”中含有的金属元素有___________ (填元素符号)。
(3)SnO2与NaOH溶液反应的离子方程式为___________ 。
(4)加入Na2S可与"滤液a”中的Na2PbO3反应以达到除铅的目的,写出相关的化学方程式_____ ;可循环利用的物质的化学式为_______ 。
(5)理论上过量的焦炭与SnO2在高温下恰好反应时二者的质量比为___________ 。
(6)测定粗锡中Sn的纯度:在强酸性环境中将1.0g的粗锡样品溶解(此时Sn全部转化成Sn2+),迅速加入过量NH4Fe(SO4)2溶液,以二苯胺磺酸钠为指示剂,用0.1mol·L-1K2Cr2O7标准溶液滴定至终点。平行测定三次消耗的K2Cr2O7溶液的体积平均为25.00mL,计算Sn的纯度。
已知:由Sn2++2Fe3+=Sn4++2Fe2+、 +6Fe2++14H+=2Cr2++6Fe3++7H2O
+6Fe2++14H+=2Cr2++6Fe3++7H2O
①溶解粗锡时不宜选用浓盐酸,理由是___________ ;
②粗锡样品中Sn的纯度为___________ 。

已知:Sn和Pb位于周期表第IVA族;SnO2,PbO2可与强碱共热反应生成易溶盐和水。
(1)“焙烧”的主要目的是
(2)“滤渣”中含有的金属元素有
(3)SnO2与NaOH溶液反应的离子方程式为
(4)加入Na2S可与"滤液a”中的Na2PbO3反应以达到除铅的目的,写出相关的化学方程式
(5)理论上过量的焦炭与SnO2在高温下恰好反应时二者的质量比为
(6)测定粗锡中Sn的纯度:在强酸性环境中将1.0g的粗锡样品溶解(此时Sn全部转化成Sn2+),迅速加入过量NH4Fe(SO4)2溶液,以二苯胺磺酸钠为指示剂,用0.1mol·L-1K2Cr2O7标准溶液滴定至终点。平行测定三次消耗的K2Cr2O7溶液的体积平均为25.00mL,计算Sn的纯度。
已知:由Sn2++2Fe3+=Sn4++2Fe2+、
 +6Fe2++14H+=2Cr2++6Fe3++7H2O
+6Fe2++14H+=2Cr2++6Fe3++7H2O①溶解粗锡时不宜选用浓盐酸,理由是
②粗锡样品中Sn的纯度为
您最近一年使用:0次
【推荐2】用辉铜矿(主要成分为Cu2S,含少量Fe2O3、SiO2,等杂质)制备难溶于水的碱式碳酸铜的流程如下:
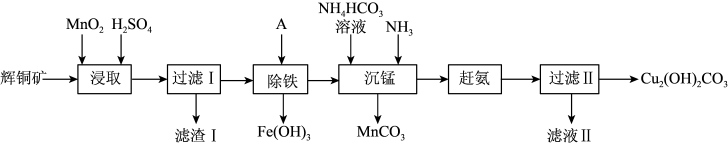
(1)下列措施无法加快浸取速率的是___________ 。(填字母)
A.延长浸取时间
B.将辉铜矿粉碎
C.充分搅拌
D.适当增大硫酸浓度
(2)滤渣I中的主要成分是MnO2、S、SiO2,请写出“浸取”反应中生成S的离子方程式:___________ 。
(3)研究发现,若先除铁再浸取,浸取速率明显变慢,可能的原因是___________ 。
(4)“除铁”的方法是通过调节溶液pH,使Fe3+转化为Fe(OH)3,则加入的试剂A最好是___________ 。
A.CO2 B.CuO C.氨水 D.HCl
(5)“沉锰”(除Mn2+)过程中有关反应的离子方程式为___________ 。
(6)滤液Ⅱ所含溶质主要是___________ (填化学式)。
(7)该流程中可循环使用的物质是___________ (填化学式)。

(1)下列措施无法加快浸取速率的是
A.延长浸取时间
B.将辉铜矿粉碎
C.充分搅拌
D.适当增大硫酸浓度
(2)滤渣I中的主要成分是MnO2、S、SiO2,请写出“浸取”反应中生成S的离子方程式:
(3)研究发现,若先除铁再浸取,浸取速率明显变慢,可能的原因是
(4)“除铁”的方法是通过调节溶液pH,使Fe3+转化为Fe(OH)3,则加入的试剂A最好是
A.CO2 B.CuO C.氨水 D.HCl
(5)“沉锰”(除Mn2+)过程中有关反应的离子方程式为
(6)滤液Ⅱ所含溶质主要是
(7)该流程中可循环使用的物质是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】钪是一种稀土金属元素,在国防、航天、核能等领域具有重要应用。工业上利用固体废料“赤泥”(含 、
、 、
、 、
、 、
、 等)回收
等)回收 的工艺流程如图。
的工艺流程如图。 难溶于盐酸;
难溶于盐酸;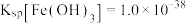 。
。
回答下列问题:
(1)为提高“酸浸”速率,对“赤泥”的处理方式为___________ ;滤渣I的主要成分是___________ (填化学式)。
(2)“氧化”时加入足量 的目的是
的目的是___________ ;氧化后溶液中 浓度为
浓度为 ,常温下“调
,常温下“调 ”时,若控制
”时,若控制 ,则
,则 的去除率为
的去除率为___________ 。(忽略调 前后溶液的体积变化)。
前后溶液的体积变化)。
(3)已知 时,
时,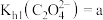 ,
,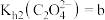 ,
,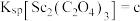 。“沉钪”时,发生反应:
。“沉钪”时,发生反应: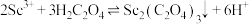 ,该反应的平衡常数
,该反应的平衡常数
___________ (用含 、
、 、
、 的代数式表示)。
的代数式表示)。
 、
、 、
、 、
、 、
、 等)回收
等)回收 的工艺流程如图。
的工艺流程如图。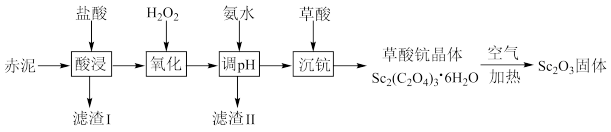
 难溶于盐酸;
难溶于盐酸;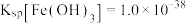 。
。回答下列问题:
(1)为提高“酸浸”速率,对“赤泥”的处理方式为
(2)“氧化”时加入足量
 的目的是
的目的是 浓度为
浓度为 ,常温下“调
,常温下“调 ”时,若控制
”时,若控制 ,则
,则 的去除率为
的去除率为 前后溶液的体积变化)。
前后溶液的体积变化)。(3)已知
 时,
时,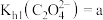 ,
,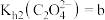 ,
,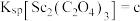 。“沉钪”时,发生反应:
。“沉钪”时,发生反应: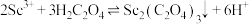 ,该反应的平衡常数
,该反应的平衡常数
 、
、 、
、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】三氯化铬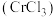 在工业上主要用作媒染剂和催化剂,根据所学知识回答下列问题。
在工业上主要用作媒染剂和催化剂,根据所学知识回答下列问题。
实验室以工业铬酸钠 为原料制备氯化铬晶体
为原料制备氯化铬晶体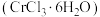 ,其装置如图所示。
,其装置如图所示。
①仪器 的冷凝水从
的冷凝水从_____ (填“上口”或“下口”)进水。
②将 工业铬酸钠、
工业铬酸钠、 甲醇、
甲醇、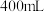 水依次加入仪器
水依次加入仪器 中。升温至
中。升温至 时,打开仪器a活塞缓慢滴加足量盐酸,保持温度在
时,打开仪器a活塞缓慢滴加足量盐酸,保持温度在 反应
反应 ,反应生成
,反应生成 ,再经过一系列步骤可得
,再经过一系列步骤可得 晶体。写出酸性条件下,甲醇与铬酸钠反应的离子方程式:
晶体。写出酸性条件下,甲醇与铬酸钠反应的离子方程式:_____ 。
(2)测定氯化铬晶体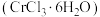 的质量分数
的质量分数
ⅰ.称取样品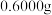 ,加水溶解并配成
,加水溶解并配成 的溶液。
的溶液。
ⅱ.移取 样品溶液于带塞的锥形瓶中,加入少量
样品溶液于带塞的锥形瓶中,加入少量 溶液,再加入过量的
溶液,再加入过量的 溶液,使
溶液,使 转化为
转化为 ;加热煮沸一段时间,加入过量的硫酸酸化,将
;加热煮沸一段时间,加入过量的硫酸酸化,将 转化为
转化为 。
。
ⅲ.用新配制的 的
的 标准溶液滴定步骤ⅱ所得溶液至终点。重复滴定3次,平均消耗
标准溶液滴定步骤ⅱ所得溶液至终点。重复滴定3次,平均消耗 溶液
溶液 (已知
(已知 被
被 还原为
还原为 )。
)。
①滴定前装有标准溶液的滴定管排气泡时,应选择下图中的_____ (填标号,下同)。 滴定管进行实验,当滴定管中的液面在刻度“10”处时,管内液体的体积
滴定管进行实验,当滴定管中的液面在刻度“10”处时,管内液体的体积_____ 。
A. B.
B. C.
C.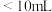 D.
D.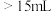
③步骤ⅱ中“加热煮沸一段时间”的目的是_____ 。
④计算 的质量分数:
的质量分数:_____ (结果保留3位有效数字)。
⑤在上述实验中,下列操作(其他操作正确)会造成测定结果偏低的有_____ (填标号)。
A.滴定管使用前,水洗后未用标准溶液润洗
B.锥形瓶水洗后未干燥
C.滴定终点读数时俯视读数
D.滴定前滴定管尖嘴部分有气泡,滴定后消失
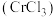 在工业上主要用作媒染剂和催化剂,根据所学知识回答下列问题。
在工业上主要用作媒染剂和催化剂,根据所学知识回答下列问题。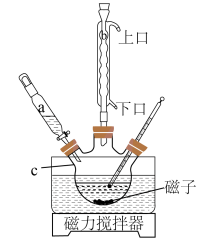

实验室以工业铬酸钠
 为原料制备氯化铬晶体
为原料制备氯化铬晶体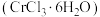 ,其装置如图所示。
,其装置如图所示。①仪器
 的冷凝水从
的冷凝水从②将
 工业铬酸钠、
工业铬酸钠、 甲醇、
甲醇、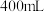 水依次加入仪器
水依次加入仪器 中。升温至
中。升温至 时,打开仪器a活塞缓慢滴加足量盐酸,保持温度在
时,打开仪器a活塞缓慢滴加足量盐酸,保持温度在 反应
反应 ,反应生成
,反应生成 ,再经过一系列步骤可得
,再经过一系列步骤可得 晶体。写出酸性条件下,甲醇与铬酸钠反应的离子方程式:
晶体。写出酸性条件下,甲醇与铬酸钠反应的离子方程式:(2)测定氯化铬晶体
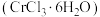 的质量分数
的质量分数ⅰ.称取样品
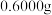 ,加水溶解并配成
,加水溶解并配成 的溶液。
的溶液。ⅱ.移取
 样品溶液于带塞的锥形瓶中,加入少量
样品溶液于带塞的锥形瓶中,加入少量 溶液,再加入过量的
溶液,再加入过量的 溶液,使
溶液,使 转化为
转化为 ;加热煮沸一段时间,加入过量的硫酸酸化,将
;加热煮沸一段时间,加入过量的硫酸酸化,将 转化为
转化为 。
。ⅲ.用新配制的
 的
的 标准溶液滴定步骤ⅱ所得溶液至终点。重复滴定3次,平均消耗
标准溶液滴定步骤ⅱ所得溶液至终点。重复滴定3次,平均消耗 溶液
溶液 (已知
(已知 被
被 还原为
还原为 )。
)。①滴定前装有标准溶液的滴定管排气泡时,应选择下图中的
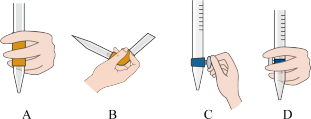
 滴定管进行实验,当滴定管中的液面在刻度“10”处时,管内液体的体积
滴定管进行实验,当滴定管中的液面在刻度“10”处时,管内液体的体积A.
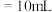 B.
B.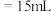 C.
C.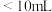 D.
D.
③步骤ⅱ中“加热煮沸一段时间”的目的是
④计算
 的质量分数:
的质量分数:⑤在上述实验中,下列操作(其他操作正确)会造成测定结果偏低的有
A.滴定管使用前,水洗后未用标准溶液润洗
B.锥形瓶水洗后未干燥
C.滴定终点读数时俯视读数
D.滴定前滴定管尖嘴部分有气泡,滴定后消失
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】实验室测定中和热的步骤如下(如图):
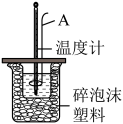
第一步:量取40.0 mL 0.25 mol/L H2SO4溶液倒入小烧杯中,测量温度;
第二步:量取40.0 mL 0.55 mol/L NaOH溶液,测量温度;
第三步:将NaOH溶液倒入小烧杯中,混合均匀后测量混合液温度。
请回答:
(1)图中仪器A的名称是____________ 。
(2)NaOH溶液稍过量的原因____________ .
(3)加入NaOH溶液的正确操作是____________ (填字母)。
A.沿玻璃棒缓慢加入 B.分三次均匀加入
C.一次迅速加入 D.用滴定管小心滴加
(4)上述实验测得的结果与理论上的57.3 kJ/mol有偏差,其原因可能是____________ 。
a.NaOH溶液倒入盛有硫酸的小烧杯中后未及时将盖板盖好
b.实验装置保温、隔热效果不好
c.用温度计测定NaOH溶液起始温度后又直接测定H2SO4溶液的温度
d.使用温度计搅拌混合液体
(5)若将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,放出的热量_____ (填“小于”、“等于”或“大于”)57.3 kJ,原因是__________________________________ 。
(6)已知某温度下:CH3COOH(aq)+OH-(aq)=CH3COO﹣(aq)+H2O(l) △H=﹣12.1 kJ•mol﹣1;H+(aq)+OH﹣(aq)= H2O(l) △H=﹣55.6 kJ•mol﹣1。则CH3COOH在水溶液中电离的△H=________________ 。

第一步:量取40.0 mL 0.25 mol/L H2SO4溶液倒入小烧杯中,测量温度;
第二步:量取40.0 mL 0.55 mol/L NaOH溶液,测量温度;
第三步:将NaOH溶液倒入小烧杯中,混合均匀后测量混合液温度。
请回答:
(1)图中仪器A的名称是
(2)NaOH溶液稍过量的原因
(3)加入NaOH溶液的正确操作是
A.沿玻璃棒缓慢加入 B.分三次均匀加入
C.一次迅速加入 D.用滴定管小心滴加
(4)上述实验测得的结果与理论上的57.3 kJ/mol有偏差,其原因可能是
a.NaOH溶液倒入盛有硫酸的小烧杯中后未及时将盖板盖好
b.实验装置保温、隔热效果不好
c.用温度计测定NaOH溶液起始温度后又直接测定H2SO4溶液的温度
d.使用温度计搅拌混合液体
(5)若将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,放出的热量
(6)已知某温度下:CH3COOH(aq)+OH-(aq)=CH3COO﹣(aq)+H2O(l) △H=﹣12.1 kJ•mol﹣1;H+(aq)+OH﹣(aq)= H2O(l) △H=﹣55.6 kJ•mol﹣1。则CH3COOH在水溶液中电离的△H=
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某课题组正在研究与 相关的课题,包括钢材酸洗废液中除去
相关的课题,包括钢材酸洗废液中除去 原理以及含较高浓度
原理以及含较高浓度 的工业废水中
的工业废水中 资源化利用,过程如下:
资源化利用,过程如下:
(1)配制模拟酸洗废液
配制 的
的 和
和 混合溶液,向其中加入计算量的
混合溶液,向其中加入计算量的 ,得到
,得到 含铬量为
含铬量为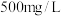 的模拟酸洗废液。
的模拟酸洗废液。 转化为
转化为 的离子方程式为
的离子方程式为_______ 。
(2)研究除 原理
原理
如图-1所示,向三颈瓶中加入5g铁粉,在搅拌下加入模拟酸洗废液 ,40℃下加热
,40℃下加热 ,产生不溶物,过滤。
,产生不溶物,过滤。
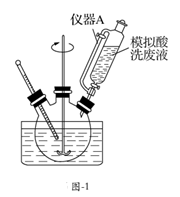
①基态 的核外电子排布式为
的核外电子排布式为_______ 。
②采用40℃水浴加热的优点为_______ 。
(3)除 原理推测如下:
原理推测如下:
①加入铁粉与溶液中的 反应,溶液中的
反应,溶液中的 和
和 含量升高;随着溶液pH升高,
含量升高;随着溶液pH升高, 更易与
更易与 结合生成
结合生成 ;
; 进一步氧化生成
进一步氧化生成 胶体;
胶体; 一方面因
一方面因 和
和 胶体具有较好的吸附性被除去,
胶体具有较好的吸附性被除去, 被除去的另一重要原因是
被除去的另一重要原因是_______ 。
研究废水中较高浓度 的资源化应用——制备
的资源化应用——制备
已知:Cr(Ⅲ)的存在形态的物质的量分数随溶液pH的分布如图-2所示。
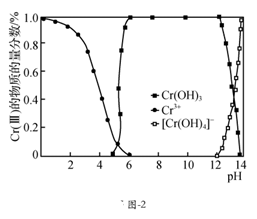
②先从含高浓度 的工业废水中分离、提纯,得到
的工业废水中分离、提纯,得到 溶液,再由
溶液,再由 溶液制得
溶液制得 。请补充完整由
。请补充完整由 溶液制得
溶液制得 的实验方案:取分离、提纯得到的
的实验方案:取分离、提纯得到的 溶液,
溶液,_______ ,低温烘干,得到高纯 晶体。
晶体。
[实验中须使用 的试剂: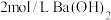 溶液、
溶液、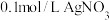 溶液、
溶液、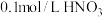 溶液、蒸馏水]
溶液、蒸馏水]
③测定 样品纯度。准确称取
样品纯度。准确称取 样品,溶于过量硫酸并配成
样品,溶于过量硫酸并配成 溶液。取
溶液。取 溶液,用足量
溶液,用足量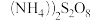 溶液将
溶液将 氧化为
氧化为 ,煮沸除去过量的
,煮沸除去过量的 ,冷却至室温。再加入过量KI溶液,以淀粉溶液为指示剂,用
,冷却至室温。再加入过量KI溶液,以淀粉溶液为指示剂,用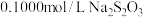 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 溶液
溶液 。
。
已知反应: ;
;
计算 样品的纯度
样品的纯度_______ (写出计算过程,结果保留四位有效数字)。
 相关的课题,包括钢材酸洗废液中除去
相关的课题,包括钢材酸洗废液中除去 原理以及含较高浓度
原理以及含较高浓度 的工业废水中
的工业废水中 资源化利用,过程如下:
资源化利用,过程如下:(1)配制模拟酸洗废液
配制
 的
的 和
和 混合溶液,向其中加入计算量的
混合溶液,向其中加入计算量的 ,得到
,得到 含铬量为
含铬量为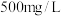 的模拟酸洗废液。
的模拟酸洗废液。 转化为
转化为 的离子方程式为
的离子方程式为(2)研究除
 原理
原理如图-1所示,向三颈瓶中加入5g铁粉,在搅拌下加入模拟酸洗废液
 ,40℃下加热
,40℃下加热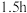 ,产生不溶物,过滤。
,产生不溶物,过滤。
①基态
 的核外电子排布式为
的核外电子排布式为②采用40℃水浴加热的优点为
(3)除
 原理推测如下:
原理推测如下:①加入铁粉与溶液中的
 反应,溶液中的
反应,溶液中的 和
和 含量升高;随着溶液pH升高,
含量升高;随着溶液pH升高, 更易与
更易与 结合生成
结合生成 ;
; 进一步氧化生成
进一步氧化生成 胶体;
胶体; 一方面因
一方面因 和
和 胶体具有较好的吸附性被除去,
胶体具有较好的吸附性被除去, 被除去的另一重要原因是
被除去的另一重要原因是研究废水中较高浓度
 的资源化应用——制备
的资源化应用——制备
已知:Cr(Ⅲ)的存在形态的物质的量分数随溶液pH的分布如图-2所示。

②先从含高浓度
 的工业废水中分离、提纯,得到
的工业废水中分离、提纯,得到 溶液,再由
溶液,再由 溶液制得
溶液制得 。请补充完整由
。请补充完整由 溶液制得
溶液制得 的实验方案:取分离、提纯得到的
的实验方案:取分离、提纯得到的 溶液,
溶液, 晶体。
晶体。[实验中
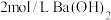 溶液、
溶液、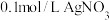 溶液、
溶液、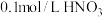 溶液、蒸馏水]
溶液、蒸馏水]③测定
 样品纯度。准确称取
样品纯度。准确称取 样品,溶于过量硫酸并配成
样品,溶于过量硫酸并配成 溶液。取
溶液。取 溶液,用足量
溶液,用足量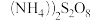 溶液将
溶液将 氧化为
氧化为 ,煮沸除去过量的
,煮沸除去过量的 ,冷却至室温。再加入过量KI溶液,以淀粉溶液为指示剂,用
,冷却至室温。再加入过量KI溶液,以淀粉溶液为指示剂,用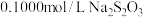 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 溶液
溶液 。
。已知反应:
 ;
;
计算
 样品的纯度
样品的纯度
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某校课外小组为测定某碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数,甲、乙两组同学分别进行了下列相关实验.
方案Ⅰ.甲组同学用质量法,按如下图所示的实验流程进行实验:

(1)实验时,蒸发结晶操作中,除了酒精灯外,还要用到的仪器是_______
(2)有同学认为“加入适量盐酸”不好操控,应改为“过量盐酸”,便于操作且不影响测定的准确性,你认为对或错_______ ,为什么___________________
(3)若实验中测得样品质量为46.4g,固体质量为40.95g,则碳酸钠的质量分数为_______ .(保留3位有效数字)
(4)蒸发结晶过程中若有固体飞溅,测得碳酸钠的质量分数____________ (填偏大 偏小 无影响).
方案Ⅱ:乙组同学的主要实验流程图如下:
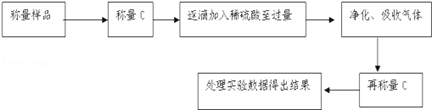
按如下图所示装置进行实验:
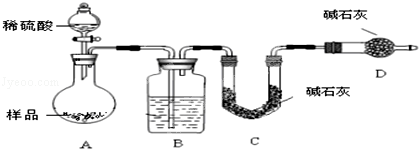
(5)在C中装碱石灰来吸收净化后的气体.D装置的作用是_____________________ .
(6)有的同学认为为了减少实验误差,在反应前后都通入N2,反应后通入N2的目的是______________________________ .
方案Ⅲ:气体分析法
(7)把一定量样品与足量稀硫酸反应后,用如图装置测量产生CO2气体的体积,B溶液最好采用_________ (以下选项中选择)使测量误差较小.

方案Ⅰ.甲组同学用质量法,按如下图所示的实验流程进行实验:

(1)实验时,蒸发结晶操作中,除了酒精灯外,还要用到的仪器是
(2)有同学认为“加入适量盐酸”不好操控,应改为“过量盐酸”,便于操作且不影响测定的准确性,你认为对或错
(3)若实验中测得样品质量为46.4g,固体质量为40.95g,则碳酸钠的质量分数为
(4)蒸发结晶过程中若有固体飞溅,测得碳酸钠的质量分数
方案Ⅱ:乙组同学的主要实验流程图如下:

按如下图所示装置进行实验:

(5)在C中装碱石灰来吸收净化后的气体.D装置的作用是
(6)有的同学认为为了减少实验误差,在反应前后都通入N2,反应后通入N2的目的是
方案Ⅲ:气体分析法
(7)把一定量样品与足量稀硫酸反应后,用如图装置测量产生CO2气体的体积,B溶液最好采用

| A.饱和碳酸钠溶液 | B.饱和碳酸氢钠溶液 |
| C.饱和氢氧化钠溶液 | D.饱和硫酸铜溶液 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ.现有下列10种物质:①液态HCl ②熔融KCl ③Ba(OH)2溶液 ④CO2 ⑤NaHSO4固体 ⑥胆矾 ⑦CaO固体 ⑧NaHCO3固体 ⑨盐酸 ⑩蔗糖。
(1)上述物质中能导电且属于电解质的有___________ 。(填写序号)
(2)物质⑤在熔化状态下电离方程式为:___________ 。
Ⅱ.大多数的化学反应都是在溶剂中进行的,配制溶液是进行化学实验操作的基本技能。
已知某“84消毒液”瓶体部分标签如图所示。
根据上述信息回答下列问题:
(3)计算该“84”消毒液中NaClO的物质的量浓度为______ 。
(4)某实验需用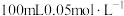 的NaClO消毒液,现用该“84”消毒液配制,需要用10mL量筒量取该“84”消毒液的体积为
的NaClO消毒液,现用该“84”消毒液配制,需要用10mL量筒量取该“84”消毒液的体积为_____ mL。在配制过程中,所需玻璃仪器除量筒、烧杯、玻璃棒外还有______ 。
(5)下列操作可能使配制溶液浓度偏低的是_______(填字母)。
(6)为测定某品牌“84”消毒液的浓度,准确量取10.00mL消毒液于水配成100.00mL水溶液,从中取出25.00mL加入锥形瓶中,并加入过量KI溶液,酸化、充分反应后向溶液中滴加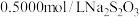 溶液。完全反应时消耗
溶液。完全反应时消耗 溶液38.50mL。反应过程中的相关化学方程式为:
溶液38.50mL。反应过程中的相关化学方程式为: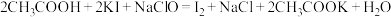 ,
, ;通过计算求出该“84”消毒液中NaClO的物质的量浓度
;通过计算求出该“84”消毒液中NaClO的物质的量浓度______ 。(写出详细计算过程)
(1)上述物质中能导电且属于电解质的有
(2)物质⑤在熔化状态下电离方程式为:
Ⅱ.大多数的化学反应都是在溶剂中进行的,配制溶液是进行化学实验操作的基本技能。
已知某“84消毒液”瓶体部分标签如图所示。
| 商品名称:84消毒液 【有效成分】NaClO 【NaClO摩尔质量】74.5g/mol 【规格】500mL 【质量分数】7.45% 【密度】约为1g/mL |
(3)计算该“84”消毒液中NaClO的物质的量浓度为
(4)某实验需用
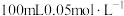 的NaClO消毒液,现用该“84”消毒液配制,需要用10mL量筒量取该“84”消毒液的体积为
的NaClO消毒液,现用该“84”消毒液配制,需要用10mL量筒量取该“84”消毒液的体积为(5)下列操作可能使配制溶液浓度偏低的是_______(填字母)。
| A.量取“84”消毒液时,俯视量筒 |
| B.移液时,未洗涤烧杯内壁和玻璃棒 |
| C.定容摇匀后,发现液面低于刻度线,又加水至刻度线 |
| D.定容时,俯视刻度线 |
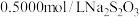 溶液。完全反应时消耗
溶液。完全反应时消耗 溶液38.50mL。反应过程中的相关化学方程式为:
溶液38.50mL。反应过程中的相关化学方程式为: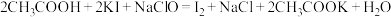 ,
, ;通过计算求出该“84”消毒液中NaClO的物质的量浓度
;通过计算求出该“84”消毒液中NaClO的物质的量浓度
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某研究性实验小组欲验证浓硝酸在与Cu、Ag合金的反应过程中除生成NO2气体外,还会有少量NO生成、并测定Cu、Ag合金中Cu的质量分数。查阅相关资料表明:“常温下,NO2与N2O4混合存在,在低于0℃时几乎只有无色的N2O4液体或晶体存在。”为此,他们设计了如下图所示的装置。
(1)写出A中Cu与HNO3反应可能的化学方程式_____________________________ 。
(2)实验开始前先打开A部分的活塞K1,持续通入一段时间的氮气再关闭K1,其目的是___________ ;装置中B瓶的作用是___________________________________ 。
(3)停止反应后,打开D中的活塞K2并通入O2,若有NO生成,则D中出现的现象是________ 。
(4)为减小实验误差,在A中反应完成和D中出现现象后,还应继续进行的操作是________ 。
(5)实验测得如下数据:实验前,Cu、Ag合金的质量:15.0g,浓HNO3:40mL 13.5 mol·L-1;实验后A溶液:V=40mL c(H+)=1.0 mol·L-1。假设反应中HNO3既无挥发也无分解,则:参加反应的HNO3的物质的量为__________________ mol。
(6)若已知Cu、Ag合金的质量为m g,且溶解完全。请利用A装置中反应后的溶液进行简单的操作,以确定合金中Cu的质量分数,其实验过程为_____________________ 。
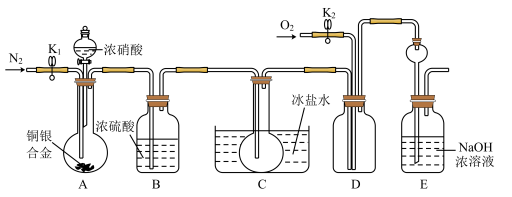
(1)写出A中Cu与HNO3反应可能的化学方程式
(2)实验开始前先打开A部分的活塞K1,持续通入一段时间的氮气再关闭K1,其目的是
(3)停止反应后,打开D中的活塞K2并通入O2,若有NO生成,则D中出现的现象是
(4)为减小实验误差,在A中反应完成和D中出现现象后,还应继续进行的操作是
(5)实验测得如下数据:实验前,Cu、Ag合金的质量:15.0g,浓HNO3:40mL 13.5 mol·L-1;实验后A溶液:V=40mL c(H+)=1.0 mol·L-1。假设反应中HNO3既无挥发也无分解,则:参加反应的HNO3的物质的量为
(6)若已知Cu、Ag合金的质量为m g,且溶解完全。请利用A装置中反应后的溶液进行简单的操作,以确定合金中Cu的质量分数,其实验过程为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】Ⅰ.氨的测定:精确称取w g X,加适量水溶解,注入如图所示的仪器A中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,用 mL
mL 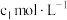 的盐酸标准溶液吸收。蒸氨结束后取下接收瓶,用
的盐酸标准溶液吸收。蒸氨结束后取下接收瓶,用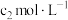 NaOH标准溶液滴定过剩的HCl,到终点时消耗
NaOH标准溶液滴定过剩的HCl,到终点时消耗 mL NaOH溶液。
mL NaOH溶液。
(1)盛装样品液的仪器名称是_______ 。
(2)用NaOH标准溶液滴定过剩的HCl时,应使用_______ 式滴定管,可使用的指示剂为_______ 。
(3)样品中氨的质量分数表达式为(以 计)
计)_______ 。
(4)测定氨前应该对装置进行气密性检验,若气密性不好测定结果将_______ (填“偏高”或“偏低”)。
Ⅱ.醋酸亚铬[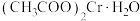 ]为砖红色晶体,难溶于冷水,易溶于酸,在气体分析中用作氧气吸收剂。一般制备方法是先在封闭体系中利用金属锌作还原剂,将三价铬(水溶液为绿色)还原为二价铬(水溶液为亮蓝色);二价铬再与醋酸钠溶液作用即可制得醋酸亚铬。实验装置如图所示,回答下列问题:
]为砖红色晶体,难溶于冷水,易溶于酸,在气体分析中用作氧气吸收剂。一般制备方法是先在封闭体系中利用金属锌作还原剂,将三价铬(水溶液为绿色)还原为二价铬(水溶液为亮蓝色);二价铬再与醋酸钠溶液作用即可制得醋酸亚铬。实验装置如图所示,回答下列问题:_______ 。
(6)将过量锌粒和氯化铬固体置于c中,加入少量蒸馏水,按图连接好装置,打开 、
、 ,关闭
,关闭 。
。
①c中溶液由绿色逐渐变为亮蓝色,该反应的离子方程式为_______ 。
②同时c中有气体产生,该气体的作用是_______ 。
 mL
mL 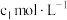 的盐酸标准溶液吸收。蒸氨结束后取下接收瓶,用
的盐酸标准溶液吸收。蒸氨结束后取下接收瓶,用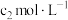 NaOH标准溶液滴定过剩的HCl,到终点时消耗
NaOH标准溶液滴定过剩的HCl,到终点时消耗 mL NaOH溶液。
mL NaOH溶液。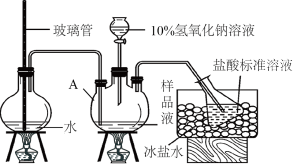
(1)盛装样品液的仪器名称是
(2)用NaOH标准溶液滴定过剩的HCl时,应使用
(3)样品中氨的质量分数表达式为(以
 计)
计)(4)测定氨前应该对装置进行气密性检验,若气密性不好测定结果将
Ⅱ.醋酸亚铬[
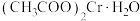 ]为砖红色晶体,难溶于冷水,易溶于酸,在气体分析中用作氧气吸收剂。一般制备方法是先在封闭体系中利用金属锌作还原剂,将三价铬(水溶液为绿色)还原为二价铬(水溶液为亮蓝色);二价铬再与醋酸钠溶液作用即可制得醋酸亚铬。实验装置如图所示,回答下列问题:
]为砖红色晶体,难溶于冷水,易溶于酸,在气体分析中用作氧气吸收剂。一般制备方法是先在封闭体系中利用金属锌作还原剂,将三价铬(水溶液为绿色)还原为二价铬(水溶液为亮蓝色);二价铬再与醋酸钠溶液作用即可制得醋酸亚铬。实验装置如图所示,回答下列问题: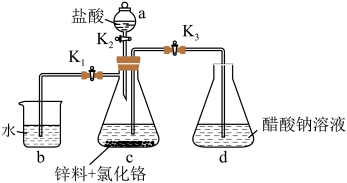
(6)将过量锌粒和氯化铬固体置于c中,加入少量蒸馏水,按图连接好装置,打开
 、
、 ,关闭
,关闭 。
。①c中溶液由绿色逐渐变为亮蓝色,该反应的离子方程式为
②同时c中有气体产生,该气体的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】I、某研究性学习小组为了验证CH4是否具有还原性,设计了如下实验:
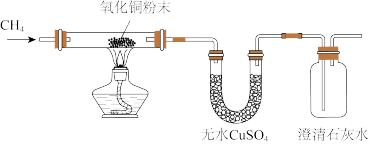
(1)实验过程中观察到无水CuSO4逐渐变蓝,澄清石灰水出现浑浊现象,则CH4与CuO反应的化学方程式为____________ 。
(2)研究小组将CH4通入溴水时,发现溴水逐渐褪色,你认为原因可能是_________________ 。
请设计一个实验方案证明你的结论(用文字表示,不必画实验装置图)__________________ 。
II、
(3)工业上用电石-乙炔生产氯乙烯的反应如下:CaO+3C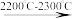 CaC2+CO
CaC2+CO
CaC2+2H2O→CH≡CH↑+Ca(OH)2,CH≡CH+HCl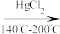 CH2=CHCl
CH2=CHCl
电石-乙炔法的优点是流程简单,产品纯度高,而且不依赖与石油资源。
电石-乙炔法的缺点是:___________ 、___________ 。
(4)乙烷和氯气反应可制得ClCH2CH2Cl,ClCH2CH2Cl加热分解得到氯乙烯和氯化氢。请设计以乙烯和氯气为原料制取氯乙烯的方案(其他原料自选),用化学方程式表示_____________ (不必注明反应条件)。要求:①反应产生的氯化氢必须用于氯乙烯的制备;②不再产生其他废液。

(1)实验过程中观察到无水CuSO4逐渐变蓝,澄清石灰水出现浑浊现象,则CH4与CuO反应的化学方程式为
(2)研究小组将CH4通入溴水时,发现溴水逐渐褪色,你认为原因可能是
请设计一个实验方案证明你的结论(用文字表示,不必画实验装置图)
II、
(3)工业上用电石-乙炔生产氯乙烯的反应如下:CaO+3C
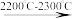 CaC2+CO
CaC2+COCaC2+2H2O→CH≡CH↑+Ca(OH)2,CH≡CH+HCl
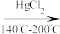 CH2=CHCl
CH2=CHCl电石-乙炔法的优点是流程简单,产品纯度高,而且不依赖与石油资源。
电石-乙炔法的缺点是:
(4)乙烷和氯气反应可制得ClCH2CH2Cl,ClCH2CH2Cl加热分解得到氯乙烯和氯化氢。请设计以乙烯和氯气为原料制取氯乙烯的方案(其他原料自选),用化学方程式表示
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】含氯消毒剂是消毒剂中常用的一类产品。
I.某实验小组用如图装置制备家用消毒液。
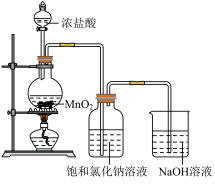
(1)图中盛装浓盐酸的仪器名称是___ ,写出利用上述装置制备消毒液涉及反应的化学方程式,制氯气:___ 、制消毒液:___ 。此方法获得的消毒液的有效成分是___ (填名称)。
(2)洗气瓶中饱和食盐水的作用是___ 。
(3)此消毒液在使用时应注意一些事项,下列说法正确的是___ 。
a.可以用于衣物消毒
b.可以用于瓷砖、大理石地面的消毒
c.可以用于皮肤消毒
d.与洁厕灵(含盐酸)混合使用效果更好
(4)Cl2是一种有毒气体,如果泄漏会造成严重的环境污染。化工厂可用浓氨水来检验Cl2是否泄漏,有关反应的化学方程式为:3Cl2(气)+8NH3(气)=6NH4Cl(固)+N2(气)若反应中消耗Cl21.5mol,则被氧化的NH3在标准状况下的体积为___ L,该过程中电子转移的总数为___ 个。
II.(5)二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。氯酸钠与盐酸在50℃的条件下反应得到二氧化氯和氯气的混合气体。控制50℃的加热方法是___ ,写出该反应的化学方程式___ 。
(6)目前已开发出用电解法制取ClO2的新工艺。
如图所示,用石墨做电极,在一定条件下电解饱和食盐水制取ClO2。写出阳极产生ClO2的电极反应式:___ 。
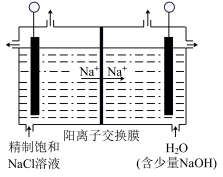
I.某实验小组用如图装置制备家用消毒液。

(1)图中盛装浓盐酸的仪器名称是
(2)洗气瓶中饱和食盐水的作用是
(3)此消毒液在使用时应注意一些事项,下列说法正确的是
a.可以用于衣物消毒
b.可以用于瓷砖、大理石地面的消毒
c.可以用于皮肤消毒
d.与洁厕灵(含盐酸)混合使用效果更好
(4)Cl2是一种有毒气体,如果泄漏会造成严重的环境污染。化工厂可用浓氨水来检验Cl2是否泄漏,有关反应的化学方程式为:3Cl2(气)+8NH3(气)=6NH4Cl(固)+N2(气)若反应中消耗Cl21.5mol,则被氧化的NH3在标准状况下的体积为
II.(5)二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。氯酸钠与盐酸在50℃的条件下反应得到二氧化氯和氯气的混合气体。控制50℃的加热方法是
(6)目前已开发出用电解法制取ClO2的新工艺。
如图所示,用石墨做电极,在一定条件下电解饱和食盐水制取ClO2。写出阳极产生ClO2的电极反应式:

您最近一年使用:0次



