已知氢氧化钙和钨酸钙(CaWO4)都是微溶电解质,两者的溶解度均随温度升高而减小。在钨冶炼工艺中,将氢氧化钙加入钨酸钠碱性溶液中得到钨酸钙,发生反应Ⅰ: (aq)+Ca(OH)2(s)
(aq)+Ca(OH)2(s) CaWO4(s)+2OH-(aq)
CaWO4(s)+2OH-(aq)
(1)如图为不同温度下Ca(OH)2、CaWO4 的沉淀溶解平衡曲线。

①计算T1时,Ksp(CaWO4)=________ 。
②T1________ T2(填“>”“=”或“<”)。
(2)反应Ⅰ的平衡常数K理论值如表:
①该反应平衡常数K的表达式为________ 。
②该反应的ΔH________ 0(“>”“=”或“<”)。
③由于溶液中离子间的相互作用,实验测得的平衡常数与理论值相距甚远。50℃时,向一定体积的钨酸钠碱性溶液[c(Na2WO4)=c(NaOH)=0.5 mol·L-1]中,加入过量Ca(OH)2,反应达到平衡后 的沉淀率为60%,此时
的沉淀率为60%,此时 的平衡浓度为
的平衡浓度为________ mol·L-1,实验测得的平衡常数为________ (保留小数点后两位)。
(3)制取钨酸钙时,适时向反应混合液中添加适量盐酸,其作用是________ 。
 (aq)+Ca(OH)2(s)
(aq)+Ca(OH)2(s) CaWO4(s)+2OH-(aq)
CaWO4(s)+2OH-(aq)(1)如图为不同温度下Ca(OH)2、CaWO4 的沉淀溶解平衡曲线。

①计算T1时,Ksp(CaWO4)=
②T1
(2)反应Ⅰ的平衡常数K理论值如表:
| 温度/℃ | 25 | 50 | 90 | 100 |
| K | 79.96 | 208.06 | 222.88 | 258.05 |
①该反应平衡常数K的表达式为
②该反应的ΔH
③由于溶液中离子间的相互作用,实验测得的平衡常数与理论值相距甚远。50℃时,向一定体积的钨酸钠碱性溶液[c(Na2WO4)=c(NaOH)=0.5 mol·L-1]中,加入过量Ca(OH)2,反应达到平衡后
 的沉淀率为60%,此时
的沉淀率为60%,此时 的平衡浓度为
的平衡浓度为(3)制取钨酸钙时,适时向反应混合液中添加适量盐酸,其作用是
更新时间:2020-10-24 08:18:01
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】废镍催化剂主要含 ,还有少量
,还有少量 及其氧化物、
及其氧化物、 。某研究性学习小组设计如下工艺流程回收镍,制备硫酸镍晶体
。某研究性学习小组设计如下工艺流程回收镍,制备硫酸镍晶体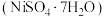 。
。

该小组同学查阅资料知:
①镍的化学性质与铁相似,能与酸缓慢反应;
②溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
(1)除“粉碎”外,请你再写出一条提高废镍催化剂酸浸效率的措施___________ 。
(2)滤渣1的主要成分有___________ 。
(3)“溶液”中加入 目的是
目的是___________ (用离子方程式表示)。
(4)下列物质调溶液 ,最好选用
,最好选用___________ (填字母标号)。
a.氨水 b.稀 c.
c. d.
d.
(5)若调 前
前 和
和 浓度均为
浓度均为 ,则“调
,则“调 ”需控制溶液
”需控制溶液 的范围为
的范围为___________ 。
(6)如图为 ,溶解度随温度变化关系,据图分析操作
,溶解度随温度变化关系,据图分析操作 是
是___________ 。

 ,还有少量
,还有少量 及其氧化物、
及其氧化物、 。某研究性学习小组设计如下工艺流程回收镍,制备硫酸镍晶体
。某研究性学习小组设计如下工艺流程回收镍,制备硫酸镍晶体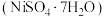 。
。
该小组同学查阅资料知:
①镍的化学性质与铁相似,能与酸缓慢反应;
②溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 |  |  |  |  |
开始沉淀时 的 的 | 7.2 | 3.7 | 2.2 | 7.5 |
沉淀完全时 的 的 | 8.7 | 4.7 | 3.2 | 9.0 |
(1)除“粉碎”外,请你再写出一条提高废镍催化剂酸浸效率的措施
(2)滤渣1的主要成分有
(3)“溶液”中加入
 目的是
目的是(4)下列物质调溶液
 ,最好选用
,最好选用a.氨水 b.稀
 c.
c. d.
d.
(5)若调
 前
前 和
和 浓度均为
浓度均为 ,则“调
,则“调 ”需控制溶液
”需控制溶液 的范围为
的范围为(6)如图为
 ,溶解度随温度变化关系,据图分析操作
,溶解度随温度变化关系,据图分析操作 是
是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】实验室研究从医用废感光胶片中回收银的方法。
(1)银的浸出 溶液与
溶液与 溶液直接混合能发生氧化还原反应:
溶液直接混合能发生氧化还原反应:
ii. 。
。
① 溶液将胶片上的单质银转化为
溶液将胶片上的单质银转化为 ,其离子方程式是
,其离子方程式是___________ 。
② 溶液能溶解
溶液能溶解 并得到含
并得到含 的浸出液。结合平衡移动原理解释
的浸出液。结合平衡移动原理解释 溶解的原因:
溶解的原因:___________ 。
Ⅱ.一步法:用水溶解 和乙二胺四乙酸二钠(用
和乙二胺四乙酸二钠(用 表示)的混合固体,调节
表示)的混合固体,调节 形成
形成 溶液,再加入一定量
溶液,再加入一定量 ,配成浸取液。将废感光胶片浸入浸取液中,发生反应:
,配成浸取液。将废感光胶片浸入浸取液中,发生反应:
 。
。
③从物质氧化性或还原性的角度分析加入 的作用:
的作用:___________ 。
(2)银的还原
调节(1)所得浸出液 ,向其中加入
,向其中加入 溶液(B的化合价为
溶液(B的化合价为 )至不再产生黑色沉淀,过滤得到粗银:滤液中的
)至不再产生黑色沉淀,过滤得到粗银:滤液中的 可以循环使用。补全离子方程式:
可以循环使用。补全离子方程式:___________ 。

(3)银浸出率的测定
称取 洗净干燥的原胶片,灼烧灰化后用
洗净干燥的原胶片,灼烧灰化后用 溶解,过滤。滤液用
溶解,过滤。滤液用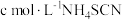 标准溶液滴定至终点,消耗标准溶液
标准溶液滴定至终点,消耗标准溶液 。另取
。另取 洗净干燥的浸取后胶片,用同样方法处理,滴定,消耗
洗净干燥的浸取后胶片,用同样方法处理,滴定,消耗 标准溶液
标准溶液 。(已知:
。(已知: )
)
银的浸出率
___________ (列出计算表达式)。
(1)银的浸出
I、两步法:
 溶液与
溶液与 溶液直接混合能发生氧化还原反应:
溶液直接混合能发生氧化还原反应:ii.
 。
。①
 溶液将胶片上的单质银转化为
溶液将胶片上的单质银转化为 ,其离子方程式是
,其离子方程式是②
 溶液能溶解
溶液能溶解 并得到含
并得到含 的浸出液。结合平衡移动原理解释
的浸出液。结合平衡移动原理解释 溶解的原因:
溶解的原因:Ⅱ.一步法:用水溶解
 和乙二胺四乙酸二钠(用
和乙二胺四乙酸二钠(用 表示)的混合固体,调节
表示)的混合固体,调节 形成
形成 溶液,再加入一定量
溶液,再加入一定量 ,配成浸取液。将废感光胶片浸入浸取液中,发生反应:
,配成浸取液。将废感光胶片浸入浸取液中,发生反应: 。
。③从物质氧化性或还原性的角度分析加入
 的作用:
的作用:(2)银的还原
调节(1)所得浸出液
 ,向其中加入
,向其中加入 溶液(B的化合价为
溶液(B的化合价为 )至不再产生黑色沉淀,过滤得到粗银:滤液中的
)至不再产生黑色沉淀,过滤得到粗银:滤液中的 可以循环使用。补全离子方程式:
可以循环使用。补全离子方程式:
(3)银浸出率的测定
称取
 洗净干燥的原胶片,灼烧灰化后用
洗净干燥的原胶片,灼烧灰化后用 溶解,过滤。滤液用
溶解,过滤。滤液用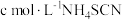 标准溶液滴定至终点,消耗标准溶液
标准溶液滴定至终点,消耗标准溶液 。另取
。另取 洗净干燥的浸取后胶片,用同样方法处理,滴定,消耗
洗净干燥的浸取后胶片,用同样方法处理,滴定,消耗 标准溶液
标准溶液 。(已知:
。(已知: )
)银的浸出率

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】我国科学家用粗氢氧化高钴[Co(OH)3]制备硫酸钴晶体(CoSO4∙7H2O),其工艺流程如下。

已知:ⅰ.还原浸出液中的阳离子有:Co2+、H+、Fe2+和Ca2+等
iⅱ.部分物质的溶度积常数如下(25℃)
ⅲ.CoSO4∙7H2O溶解度随温度升高而明显增大
(1)氢氧化高钴溶于硫酸的化学方程式是_____________ 。
(2)浸出Co2+时,理论上氧化剂和还原剂物质的量之比为_____________ 。
(3)写出“氧化沉铁”的离子方程式_____________ ;
25℃时,浊液中铁离子浓度为_____________ mol/L(此时pH为4)。
(4)结合平衡移动原理解释“氟化沉钙”步骤加入过量NaF的原因_____________ 。
(5)P507萃取后,经反萃取得到硫酸钴溶液,将硫酸钴溶液经_____________ 操作,得到硫酸钴晶体。
(6)用滴定法测定硫酸钴晶体中的钴含量,其原理和操作如下。
在溶液中,用铁氰化钾将Co(Ⅱ)氧化为Co(Ⅲ),过量的铁氰化钾以Co(Ⅱ)标准液返滴定。反应的方程式为: 。
。
已知:铁氰化钾标准液浓度为c mol/L,Co(Ⅱ)标准液质量浓度为ρg/L。
取mg硫酸钴晶体,加水配成200mL溶液,取20mL待测液进行滴定,消耗V1mL铁氰化钾标准液、V2mL Co(Ⅱ)标准液。
计算样品中钴含量ω=_____________ (以钴的质量分数ω计)。

已知:ⅰ.还原浸出液中的阳离子有:Co2+、H+、Fe2+和Ca2+等
iⅱ.部分物质的溶度积常数如下(25℃)
物质 | Ksp |
CaF2 |
|
Fe(OH)3 |
|
(1)氢氧化高钴溶于硫酸的化学方程式是
(2)浸出Co2+时,理论上氧化剂和还原剂物质的量之比为
(3)写出“氧化沉铁”的离子方程式
25℃时,浊液中铁离子浓度为
(4)结合平衡移动原理解释“氟化沉钙”步骤加入过量NaF的原因
(5)P507萃取后,经反萃取得到硫酸钴溶液,将硫酸钴溶液经
(6)用滴定法测定硫酸钴晶体中的钴含量,其原理和操作如下。
在溶液中,用铁氰化钾将Co(Ⅱ)氧化为Co(Ⅲ),过量的铁氰化钾以Co(Ⅱ)标准液返滴定。反应的方程式为:
 。
。已知:铁氰化钾标准液浓度为c mol/L,Co(Ⅱ)标准液质量浓度为ρg/L。
取mg硫酸钴晶体,加水配成200mL溶液,取20mL待测液进行滴定,消耗V1mL铁氰化钾标准液、V2mL Co(Ⅱ)标准液。
计算样品中钴含量ω=
您最近一年使用:0次
【推荐1】工业上以石煤(主要成分为V2O3,含有少量SiO2、P2O5等杂质)为原料制备钒的主要流程如图:
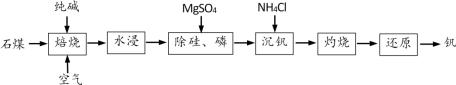
已知:①NH4VO3难溶于水。②Ksp(MgSiO3)=2.4×10-5,Ksp[Mg3(PO4)2]=2.7×10-27。
(1)焙烧:通入空气的条件下,向石煤中加纯碱焙烧,将V2O3转化为NaVO3的化学方程式为___ 。
(2)除硅、磷:
①用MgSO4溶液除硅、磷时,Si、P会形成Mg3(PO4)2、MgSiO3沉淀。若沉淀后溶液中c(PO )=1.0×10-8mol•L-1,则c(SiO
)=1.0×10-8mol•L-1,则c(SiO )=
)=___ mol•L-1。
②如图所示,随着温度升高,除磷率下降,其原因是Mg3(PO4)2溶解度增大、___ ;随着温度升高,除硅率升高,其原因是___ 。

(3)沉钒:此过程反应温度需控制在50℃左右,温度不能过高的原因为___ 。
(4)灼烧:在灼烧NH4VO3的过程中,固体的残留率(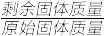 ×100%)随温度变化的曲线如图所示,则A~B段发生反应的方程式为
×100%)随温度变化的曲线如图所示,则A~B段发生反应的方程式为___ 。
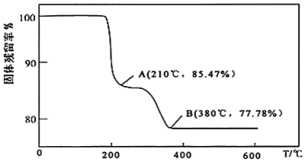

已知:①NH4VO3难溶于水。②Ksp(MgSiO3)=2.4×10-5,Ksp[Mg3(PO4)2]=2.7×10-27。
(1)焙烧:通入空气的条件下,向石煤中加纯碱焙烧,将V2O3转化为NaVO3的化学方程式为
(2)除硅、磷:
①用MgSO4溶液除硅、磷时,Si、P会形成Mg3(PO4)2、MgSiO3沉淀。若沉淀后溶液中c(PO
 )=1.0×10-8mol•L-1,则c(SiO
)=1.0×10-8mol•L-1,则c(SiO )=
)=②如图所示,随着温度升高,除磷率下降,其原因是Mg3(PO4)2溶解度增大、

(3)沉钒:此过程反应温度需控制在50℃左右,温度不能过高的原因为
(4)灼烧:在灼烧NH4VO3的过程中,固体的残留率(
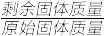 ×100%)随温度变化的曲线如图所示,则A~B段发生反应的方程式为
×100%)随温度变化的曲线如图所示,则A~B段发生反应的方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】钯(Pd)是一种银白色金属,在航天、航空、航海、兵器和核能等高科技领域用途广泛。以硫化镍铜矿(含有 以及少量的
以及少量的 )为原料制备
)为原料制备 和
和 的工艺流程如图:
的工艺流程如图:
II.王水具有强氧化性,能将单质钯转化为 。
。
III. 时,
时,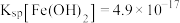 ,
, ,
,
 。
。
试回答下列问题:
(1)在硫化镍铜矿灼烧过程中,部分元素转化为氧化物,在实验室枃烧时,下列仪器中不需要用到的是____________ (填标号);“灼烧”前将矿石粉碎成细颗粒的目的是____________ (填一条即可)。 的利用率,通常“酸浸”时需加热,试分析可能的原因:
的利用率,通常“酸浸”时需加热,试分析可能的原因:____________ (从平衡移动角度作答)和加快浸取速率。
(3)“置换”时加入铁单质除去溶液中的 ,再
,再_______________ (填方法)除去引入的铁元素。
(4)“除硅”过程中发生反应的离子方程式为____________ , 的空间结构为
的空间结构为____________ 。
(5)在制备 的过程中,需加入过量的浓氨水,原因为
的过程中,需加入过量的浓氨水,原因为_________________ 。
(6)“氢气还原”时有 生成,
生成, 溶液中离子浓度大小关系为
溶液中离子浓度大小关系为____________ 。
 以及少量的
以及少量的 )为原料制备
)为原料制备 和
和 的工艺流程如图:
的工艺流程如图:
II.王水具有强氧化性,能将单质钯转化为
 。
。III.
 时,
时,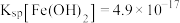 ,
, ,
,
 。
。试回答下列问题:
(1)在硫化镍铜矿灼烧过程中,部分元素转化为氧化物,在实验室枃烧时,下列仪器中不需要用到的是

 的利用率,通常“酸浸”时需加热,试分析可能的原因:
的利用率,通常“酸浸”时需加热,试分析可能的原因:(3)“置换”时加入铁单质除去溶液中的
 ,再
,再(4)“除硅”过程中发生反应的离子方程式为
 的空间结构为
的空间结构为(5)在制备
 的过程中,需加入过量的浓氨水,原因为
的过程中,需加入过量的浓氨水,原因为(6)“氢气还原”时有
 生成,
生成, 溶液中离子浓度大小关系为
溶液中离子浓度大小关系为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】I.常温下, 的
的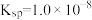 ,饱和溶液中存在平衡:
,饱和溶液中存在平衡: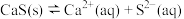 。
。
(1)①该温度下,将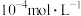 氯化钙溶液与
氯化钙溶液与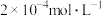 硫化钠溶液等体积混合,能否产生沉淀并说明理由:
硫化钠溶液等体积混合,能否产生沉淀并说明理由:_________ ;温度升高时,
_________ (填“增大”“减小”或“不变”,下同)。
②向 悬浊液中滴加少量浓盐酸,
悬浊液中滴加少量浓盐酸,
______ ,原因是_______ (用文字和离子方程式说明)。
(2)若向 悬浊液中加入
悬浊液中加入 溶液,生成一种黑色固体物质,写出该过程中发生反应的离子方程式:
溶液,生成一种黑色固体物质,写出该过程中发生反应的离子方程式:_________ 。
Ⅱ.已知常温下,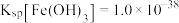 ,欲使
,欲使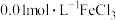 溶液开始产生
溶液开始产生 沉淀,应调整溶液
沉淀,应调整溶液 ,使
,使
____________ ,若要使其沉淀完全, 应
应____________ 。
 的
的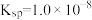 ,饱和溶液中存在平衡:
,饱和溶液中存在平衡: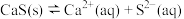 。
。(1)①该温度下,将
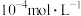 氯化钙溶液与
氯化钙溶液与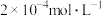 硫化钠溶液等体积混合,能否产生沉淀并说明理由:
硫化钠溶液等体积混合,能否产生沉淀并说明理由:
②向
 悬浊液中滴加少量浓盐酸,
悬浊液中滴加少量浓盐酸,
(2)若向
 悬浊液中加入
悬浊液中加入 溶液,生成一种黑色固体物质,写出该过程中发生反应的离子方程式:
溶液,生成一种黑色固体物质,写出该过程中发生反应的离子方程式:Ⅱ.已知常温下,
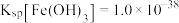 ,欲使
,欲使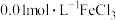 溶液开始产生
溶液开始产生 沉淀,应调整溶液
沉淀,应调整溶液 ,使
,使
 应
应
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】I.我国《生活饮用水卫生标准》中规定生活用水中镉的排放量不超过0.005mg•L-1。处理含镉废水可采用化学沉淀法。
(1)写出磷酸镉[Cd3(PO4)2]沉淀溶解平衡常数的表达式:Ksp[Cd3(PO4)2]=____ 。
(2)一定温度下,CdCO3的Ksp=4.0×10-12,Cd(OH)2的Ksp=3.2×10-14,该温度下____ [填“CdCO3”或“Cd(OH)2”]的饱和溶液中Cd2+浓度较大。
(3)向某含镉废水中加入Na2S,当S2-浓度达到7.9×10-8mol•L-1时,废水中Cd2+的浓度为____ mol•L-1[已知:Ksp(CdS)=7.9×10-27],此时_____ (填“符合”或“不符合”)《生活饮用水卫生标准》。
II.根据题目提供的溶度积数据进行计算并回答下列问题:
(4)已知25℃时,Ksp[Mg(OH)2]=5.6×10-12;酸碱指示剂百里酚蓝变色的pH范围如表:
25℃时,向Mg(OH)2饱和溶液中滴加2滴百里酚蓝指示剂,溶液所呈现的颜色为____ 。
(5)常温下,向50mL0.018mol•L-1的AgNO3溶液中加入50mL0.020mol•L-1的盐酸,生成沉淀。已知该温度下,Ksp(AgCl)=1.8×10-10,忽略溶液体积的变化。
①反应后,溶液的pH=____ 。
②如果向反应后的溶液中继续加入50mL0.001mol•L-1的盐酸,____ (填“有”或“无”)白色沉淀生成。
(1)写出磷酸镉[Cd3(PO4)2]沉淀溶解平衡常数的表达式:Ksp[Cd3(PO4)2]=
(2)一定温度下,CdCO3的Ksp=4.0×10-12,Cd(OH)2的Ksp=3.2×10-14,该温度下
(3)向某含镉废水中加入Na2S,当S2-浓度达到7.9×10-8mol•L-1时,废水中Cd2+的浓度为
II.根据题目提供的溶度积数据进行计算并回答下列问题:
(4)已知25℃时,Ksp[Mg(OH)2]=5.6×10-12;酸碱指示剂百里酚蓝变色的pH范围如表:
| pH | <8.0 | 8.0~9.6 | >9.6 |
| 颜色 | 黄色 | 绿色 | 蓝色 |
(5)常温下,向50mL0.018mol•L-1的AgNO3溶液中加入50mL0.020mol•L-1的盐酸,生成沉淀。已知该温度下,Ksp(AgCl)=1.8×10-10,忽略溶液体积的变化。
①反应后,溶液的pH=
②如果向反应后的溶液中继续加入50mL0.001mol•L-1的盐酸,
您最近一年使用:0次
【推荐2】金属铬坚硬,耐腐蚀,可做镀层金属,并且在制皮革,羊毛,火柴,颜料等方面均有其应用。但是 致癌,因而工业废水中如果含有
致癌,因而工业废水中如果含有 需要处理后再排放。
需要处理后再排放。
已知: ,
,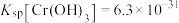 ,
, 完全沉淀时的
完全沉淀时的 约为5.6。
约为5.6。
(1)沉淀法
利用 试剂可处理含
试剂可处理含 废水,离子方程式为
废水,离子方程式为_______ 。
(2)还原法
①可以选择还原剂 ,对酸性含铬废水进行处理。将下述反应的离子方程式补充完整:
,对酸性含铬废水进行处理。将下述反应的离子方程式补充完整:_______ 。

②可以选择焦亚硫酸钠( )处理含铬
)处理含铬 废水,处理费用低。其工艺流程如图:
废水,处理费用低。其工艺流程如图:

资料:焦亚硫酸钠 为白色或黄色结晶粉末,遇强酸放出
为白色或黄色结晶粉末,遇强酸放出 。
。
ⅰ反应池中发生反应的离子方程式_______ 。
ⅱ 在酸性条件下氧化性强,在实际工业中
在酸性条件下氧化性强,在实际工业中 过低,则需要的焦亚硫酸钠的量比理论值高出许多,结合化学用语解释可能的原因是
过低,则需要的焦亚硫酸钠的量比理论值高出许多,结合化学用语解释可能的原因是_______ 。
(3) /纳米
/纳米 去除法
去除法
①某研究小组经查阅资料,发现磁铁矿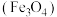 辅助纳米
辅助纳米 可能会降解含
可能会降解含 的废水。为探究其真实性,进行了如下实验,相同时间内得到如下实验结果,请补全实验结论。
的废水。为探究其真实性,进行了如下实验,相同时间内得到如下实验结果,请补全实验结论。
结论ⅰ:单独使用纳米铁可以降解
ⅱ:单独使用 可以降解
可以降解 ,降解率偏低
,降解率偏低
ⅲ:_______ 。
②经查阅资料,依据如下两个图示信息,上述实验3降解 效率增大的原因是
效率增大的原因是_______ 。

 致癌,因而工业废水中如果含有
致癌,因而工业废水中如果含有 需要处理后再排放。
需要处理后再排放。已知:
 ,
,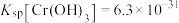 ,
, 完全沉淀时的
完全沉淀时的 约为5.6。
约为5.6。(1)沉淀法
利用
 试剂可处理含
试剂可处理含 废水,离子方程式为
废水,离子方程式为(2)还原法
①可以选择还原剂
 ,对酸性含铬废水进行处理。将下述反应的离子方程式补充完整:
,对酸性含铬废水进行处理。将下述反应的离子方程式补充完整:
②可以选择焦亚硫酸钠(
 )处理含铬
)处理含铬 废水,处理费用低。其工艺流程如图:
废水,处理费用低。其工艺流程如图:
资料:焦亚硫酸钠
 为白色或黄色结晶粉末,遇强酸放出
为白色或黄色结晶粉末,遇强酸放出 。
。ⅰ反应池中发生反应的离子方程式
ⅱ
 在酸性条件下氧化性强,在实际工业中
在酸性条件下氧化性强,在实际工业中 过低,则需要的焦亚硫酸钠的量比理论值高出许多,结合化学用语解释可能的原因是
过低,则需要的焦亚硫酸钠的量比理论值高出许多,结合化学用语解释可能的原因是(3)
 /纳米
/纳米 去除法
去除法①某研究小组经查阅资料,发现磁铁矿
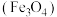 辅助纳米
辅助纳米 可能会降解含
可能会降解含 的废水。为探究其真实性,进行了如下实验,相同时间内得到如下实验结果,请补全实验结论。
的废水。为探究其真实性,进行了如下实验,相同时间内得到如下实验结果,请补全实验结论。| 实验编号 | 纳米 |  |  实际降解率 实际降解率 |
| 1 | 0.05 | 0 | 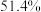 |
| 2 | 0 | 2 |  |
| 3 | 0.05 | 2 |  |

ⅱ:单独使用
 可以降解
可以降解 ,降解率偏低
,降解率偏低ⅲ:
②经查阅资料,依据如下两个图示信息,上述实验3降解
 效率增大的原因是
效率增大的原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】锰及其化合物间的转化如下图。

请回答下列问题:
(1)反应①发生的主要化学反应的方程式为:___________ 。反应③发生的主要化学反应的方程式为:___________ 。
(2)粗KMnO4晶体中含有少量的K2CO3,检验其中的少量CO32-用______ 试剂;为了得到纯的KMnO4晶体,操作Ⅲ的名称为___________ 。
(3)测定高锰酸钾样品纯度采用硫酸锰滴定:向高锰酸钾溶液中滴加硫酸锰溶液,产生黑色沉淀。当高锰酸钾溶液由紫红色刚好褪色且半分钟不恢复,表明达到滴定终点。写出该反应的离子方程式:___________ 。
(4)已知:常温下,Ksp[Mn(OH)2]=2.4×10-13。工业上,调节pH可以沉淀废水中Mn2+,当pH=10时,溶液中c(Mn2+)=___________________ 。
(5)如图,用Fe、C作电极电解含MnO4-的污水,使之转化为沉淀除去。A电极是_____ (填“Fe”或“C”),污水中MnO4-转化为沉淀除去的离子方程式为___________ 。

请回答下列问题:
(1)反应①发生的主要化学反应的方程式为:
(2)粗KMnO4晶体中含有少量的K2CO3,检验其中的少量CO32-用
(3)测定高锰酸钾样品纯度采用硫酸锰滴定:向高锰酸钾溶液中滴加硫酸锰溶液,产生黑色沉淀。当高锰酸钾溶液由紫红色刚好褪色且半分钟不恢复,表明达到滴定终点。写出该反应的离子方程式:
(4)已知:常温下,Ksp[Mn(OH)2]=2.4×10-13。工业上,调节pH可以沉淀废水中Mn2+,当pH=10时,溶液中c(Mn2+)=
(5)如图,用Fe、C作电极电解含MnO4-的污水,使之转化为沉淀除去。A电极是

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】镓是一种重要的半导体材料,在电子器件、激光器LED、太赫兹电子学等领域中具有广泛应用,是一种非常重要的国家战略金属。下图是综合利用炼锌矿渣[主要含铁酸镓Ga2(Fe2O4)3、铁酸锌ZnFe2O4,还含少量Fe及一些难溶于酸的物质]获得金属盐,并进一步利用镓盐制备具有优异光电性能的氮化嫁(GaN)的工艺流程。

已知①Ga与Al同主族,化学性质相似。②MOCVD是一种金属有机物化学气相淀积技术。
③常温下,Ksp[Fe(OH)2]=10-15,Ksp[Zn(OH)2]=1.5×10-17,Ksp[Ga(OH)3]=3×10-36,Ksp[Fe(OH)3]=4×10-39
④金属离子在此工艺条件下的萃取率(进入有机层中金属离子的百分数)见下表:
回答下列问题:
(1)基态镓原子的简化电子排布式为___________ ; 在酸性条件下不稳定,易转化为Fe3+,写出稀硫酸酸浸时铁酸锌参与反应的化学方程式:
在酸性条件下不稳定,易转化为Fe3+,写出稀硫酸酸浸时铁酸锌参与反应的化学方程式:___________ 。
(2)"转化1”中加入H2O2发生反应的离子方程式为___________ 。
(3)常温下,若酸浸后镓离子浓度为3.0×10-3mol/L,将pH调至5.4后,滤液1中残余的Ga3+的浓度为___________ 。
(4)“转化2”中加入固体铁的目的是___________ ;Ga与Al同主族,化学性质相似,“反萃取”过程中,水溶液中Ga的存在形式为___________ 。
(5)精炼时,以粗镓为阳极,纯镓为阴极,NaOH水溶液为电解质溶液。通电时,粗镓溶解进入电解质溶液,并在阴极放电析出高纯镓,则阴极的电极反应式为___________ ;精炼时,若外电路通过0.25mole-时,阴极得到3.5g的镓。则该电解装置的电解效率η=___________ (η=生成目标产物转移的电子数/转移的电子总数)。

已知①Ga与Al同主族,化学性质相似。②MOCVD是一种金属有机物化学气相淀积技术。
③常温下,Ksp[Fe(OH)2]=10-15,Ksp[Zn(OH)2]=1.5×10-17,Ksp[Ga(OH)3]=3×10-36,Ksp[Fe(OH)3]=4×10-39
④金属离子在此工艺条件下的萃取率(进入有机层中金属离子的百分数)见下表:
| 金属离子 | Fe2+ | Fe3+ | Zn2+ | Ga3+ |
| 萃取率/% | 0 | 99 | 0 | 97~98.5 |
(1)基态镓原子的简化电子排布式为
 在酸性条件下不稳定,易转化为Fe3+,写出稀硫酸酸浸时铁酸锌参与反应的化学方程式:
在酸性条件下不稳定,易转化为Fe3+,写出稀硫酸酸浸时铁酸锌参与反应的化学方程式:(2)"转化1”中加入H2O2发生反应的离子方程式为
(3)常温下,若酸浸后镓离子浓度为3.0×10-3mol/L,将pH调至5.4后,滤液1中残余的Ga3+的浓度为
(4)“转化2”中加入固体铁的目的是
(5)精炼时,以粗镓为阳极,纯镓为阴极,NaOH水溶液为电解质溶液。通电时,粗镓溶解进入电解质溶液,并在阴极放电析出高纯镓,则阴极的电极反应式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】活性氧化锌能对太阳光线和其他大气物质形成防护,常用于敏感皮肤的面霜和化妆品。工业上用菱锌矿(主要成分为ZnCO3,还含有Ni、Cd、Fe、Cu等元素及少量不溶于成的杂质)制备ZnO,工艺流程图所示:

(1)为了提高“溶浸”效果,可采取的措施有_________ 。(任写一点)
(2)“除铁”时,加入H2O2发生反应的离子方程式为________ 。如果用NaClO3代替H2O2,恰好完全反应时,理论上消耗n(NaClO3):n(H2O2)=________ 。
(3)常温下,“调pH=5”时,Fe3+的浓度降到了8×10-11mol/L,此时Fe(OH)3的溶度积常数的数值为________ 。
(4)已知三种硫化物的Ksp如表。当溶液中某离子物质的量浓度≤10-5mol/L时视为沉淀完全。假设原溶液中Cu2+、Cd2+、Ni2+的物质的量浓度均为0.1mol/L,则在加Na2S使Cu2+在溶液中的残留浓度为6.3×10-11mol/L时,此时Cd2+的去除率为________ (去除率=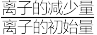 ×100%,不考虑溶液的体积变化)
×100%,不考虑溶液的体积变化)
(5)“沉锌”时,在近中性条件下加入Na2CO3可得碱式碳酸锌[ZnCO3•2Zn(OH)2•H2O]固体,同时产生大量的气体。该反应的离子方程式为_________ 。
(6)用锌与铜侧得的高纯铜锌合金滤料被广泛应用于各种水处理设备。一种铜锌合金的晶胞结构如图,已知:晶胞参数为anm。
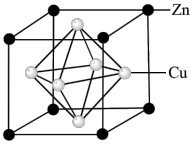
①与Zn原子等距离且最近的Zn原子有________ 个。
②该铜锌合金晶体密度为_________ g•cm-3(设NA为阿伏加德罗常数的值)

(1)为了提高“溶浸”效果,可采取的措施有
(2)“除铁”时,加入H2O2发生反应的离子方程式为
(3)常温下,“调pH=5”时,Fe3+的浓度降到了8×10-11mol/L,此时Fe(OH)3的溶度积常数的数值为
(4)已知三种硫化物的Ksp如表。当溶液中某离子物质的量浓度≤10-5mol/L时视为沉淀完全。假设原溶液中Cu2+、Cd2+、Ni2+的物质的量浓度均为0.1mol/L,则在加Na2S使Cu2+在溶液中的残留浓度为6.3×10-11mol/L时,此时Cd2+的去除率为
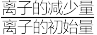 ×100%,不考虑溶液的体积变化)
×100%,不考虑溶液的体积变化)| 物质 | CdS | CuS | NiS |
| Ksp | 8.0×10-27 | 6.3×10-36 | 1.0×10-26 |
(5)“沉锌”时,在近中性条件下加入Na2CO3可得碱式碳酸锌[ZnCO3•2Zn(OH)2•H2O]固体,同时产生大量的气体。该反应的离子方程式为
(6)用锌与铜侧得的高纯铜锌合金滤料被广泛应用于各种水处理设备。一种铜锌合金的晶胞结构如图,已知:晶胞参数为anm。

①与Zn原子等距离且最近的Zn原子有
②该铜锌合金晶体密度为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】利用菱锰矿(主要成分是MnCO3,含少量A12O3、Fe2O3、FeO、CaO、MgO等)为原料制备MnO2的工艺流程如下:
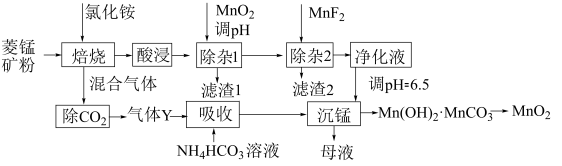
已知:①25℃时,
②相关金属离子 形成氢氧化物沉淀pH范围如下:
形成氢氧化物沉淀pH范围如下:
(1)“除杂1”中加入适量MnO2的作用是____ ,应调节溶液pH不小于____ 。
(2)“除杂2”的主要目的将Ca2+、Mg2+转化为相应的氟化物沉淀而除去,除去Ca2+的离子方程式为____ ,该反应的平衡常数为____ 。
(3)“沉锰”中生成Mn(OH)2'MnCO3沉淀的离子方程式为____ ,“母液”经加热等系列操作后可返回“____ ”工序循环使用。
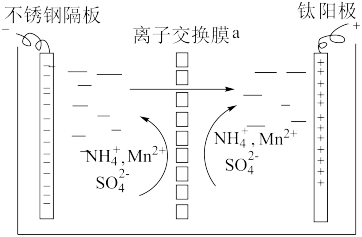
(4)以MnSO4-(NH4)2SO4为电解质溶液,利用下图装置可同时制备金属锰和MnO2。离子交换膜a为____ ,阳极电极反应式为____ 。

已知:①25℃时,

②相关金属离子
 形成氢氧化物沉淀pH范围如下:
形成氢氧化物沉淀pH范围如下:| 金属离子 | 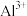 | 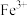 | 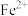 |  | 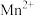 | 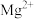 |
| 开始沉淀时的pH | 3.8 | 1.5 | 6.3 | 10.6 | 8.8 | 9.6 |
| 沉淀完全时的pH | 5.2 | 2.8 | 8.3 | 12.6 | 10.8 | 11.6 |
(2)“除杂2”的主要目的将Ca2+、Mg2+转化为相应的氟化物沉淀而除去,除去Ca2+的离子方程式为
(3)“沉锰”中生成Mn(OH)2'MnCO3沉淀的离子方程式为
(4)以MnSO4-(NH4)2SO4为电解质溶液,利用下图装置可同时制备金属锰和MnO2。离子交换膜a为

您最近一年使用:0次





