I.常温下, 的
的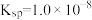 ,饱和溶液中存在平衡:
,饱和溶液中存在平衡: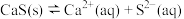 。
。
(1)①该温度下,将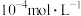 氯化钙溶液与
氯化钙溶液与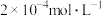 硫化钠溶液等体积混合,能否产生沉淀并说明理由:
硫化钠溶液等体积混合,能否产生沉淀并说明理由:_________ ;温度升高时,
_________ (填“增大”“减小”或“不变”,下同)。
②向 悬浊液中滴加少量浓盐酸,
悬浊液中滴加少量浓盐酸,
______ ,原因是_______ (用文字和离子方程式说明)。
(2)若向 悬浊液中加入
悬浊液中加入 溶液,生成一种黑色固体物质,写出该过程中发生反应的离子方程式:
溶液,生成一种黑色固体物质,写出该过程中发生反应的离子方程式:_________ 。
Ⅱ.已知常温下,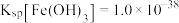 ,欲使
,欲使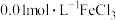 溶液开始产生
溶液开始产生 沉淀,应调整溶液
沉淀,应调整溶液 ,使
,使
____________ ,若要使其沉淀完全, 应
应____________ 。
 的
的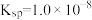 ,饱和溶液中存在平衡:
,饱和溶液中存在平衡: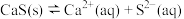 。
。(1)①该温度下,将
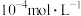 氯化钙溶液与
氯化钙溶液与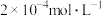 硫化钠溶液等体积混合,能否产生沉淀并说明理由:
硫化钠溶液等体积混合,能否产生沉淀并说明理由:
②向
 悬浊液中滴加少量浓盐酸,
悬浊液中滴加少量浓盐酸,
(2)若向
 悬浊液中加入
悬浊液中加入 溶液,生成一种黑色固体物质,写出该过程中发生反应的离子方程式:
溶液,生成一种黑色固体物质,写出该过程中发生反应的离子方程式:Ⅱ.已知常温下,
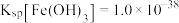 ,欲使
,欲使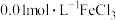 溶液开始产生
溶液开始产生 沉淀,应调整溶液
沉淀,应调整溶液 ,使
,使
 应
应
19-20高二·全国·课时练习 查看更多[5]
高中必刷题高二选择性必修1第三章 水溶液中的离子反应与平衡 第四节综合训练(已下线)3.4 难溶电解质的溶解平衡(重点练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)(已下线)3.4.2 沉淀溶解平衡的应用(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)云南省澄江市第一中学2021-2022年高二下学期3月月考化学试题云南省景东彝族自治县第一中学2021-2022学年高二下学期3月份考试化学试题
更新时间:2020-09-21 09:59:54
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
【推荐1】铬及其化合物有许多独特的性质和用途,如炼钢时加入一定量的铬可得到不锈钢。
(1)K2Cr2O7是实验中常用的强氧化剂之一,其中铬元素的化合价为_ 。向一支盛有5mL0.1mol/LK2Cr2O7溶液中滴加10~20滴6mol/LNaOH溶液,可观察到的现象是__ ,原因是(结合方程式解释)___ 。
(2)某化工厂从湿法炼锌的铜铬渣【主要含有锌、铜、铁、铬、钴(Co)等单质】中回收铬的流程如图:
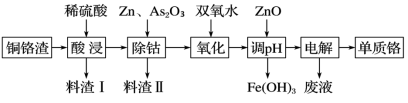
几种金属离子生成氢氧化物沉淀的pH如表所示:
①酸浸时形成的金属离子的价态均相同。料渣Ⅰ中只含有一种金属单质,该单质是___ 。
②料渣Ⅱ中含有大量的CoAs合金(提示:合金中金属元素化合价皆为0),请写出除钴时反应的离子方程式为___ 。
③加入双氧水时铁、铬形成的离子均被氧化,写出H2O2氧化铬形成Cr3+的离子方程式为___ 。
④加入ZnO调节pH的范围为___ 。
⑤单质铬在___ 极生成,另一电极的电极反应式为___ 。
(1)K2Cr2O7是实验中常用的强氧化剂之一,其中铬元素的化合价为
(2)某化工厂从湿法炼锌的铜铬渣【主要含有锌、铜、铁、铬、钴(Co)等单质】中回收铬的流程如图:

几种金属离子生成氢氧化物沉淀的pH如表所示:
| 氢氧化物 | Fe(OH)3 | Zn(OH)2 | Cr(OH)3 |
| 开始沉淀的pH | 2.2 | 6.5 | 4.6 |
| 沉淀完全的pH | 3.5 | 8.5 | 5.9 |
②料渣Ⅱ中含有大量的CoAs合金(提示:合金中金属元素化合价皆为0),请写出除钴时反应的离子方程式为
③加入双氧水时铁、铬形成的离子均被氧化,写出H2O2氧化铬形成Cr3+的离子方程式为
④加入ZnO调节pH的范围为
⑤单质铬在
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】工业上从铬铁矿废渣(主要含Cr2O3、SiO2、Al2O3、Fe2O3)中回收提取铬的工艺流程如下:
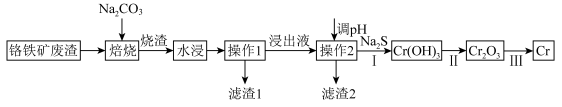
注:焙烧可将Al、Si氧化物转化为可溶性钠盐。
(1)为加快“水浸”速率,可采取的措施为_______ (写出一种即可)。
(2)已知“浸出液”的主要成分为Na2CrO4,则Cr2O3焙烧时反应的化学方式为_______ 。
(3)滤渣1的主要成分是_______ 。 实验室中进行操作2用到的玻璃仪器有_______ 。
(4)常温下,溶液中部分离子的物质的量浓度的对数lgc与pH的关系如图所示。已知溶液中离子浓度≤10-5 mol/L时认为沉淀完全。

浸出液用H2SO4调节pH的最佳范围是_______ 。
调pH时 转化的离子方程式为
转化的离子方程式为_______ 。
(5)一定温度下,利用K2Cr2O7可实现含苯酚废水的有效处理,工作原理如图所示,负极电极反应式为_______ ,一段时间后,N极附近溶液pH_______ (填“增大”、“减小”或“不变”)。


注:焙烧可将Al、Si氧化物转化为可溶性钠盐。
(1)为加快“水浸”速率,可采取的措施为
(2)已知“浸出液”的主要成分为Na2CrO4,则Cr2O3焙烧时反应的化学方式为
(3)滤渣1的主要成分是
(4)常温下,溶液中部分离子的物质的量浓度的对数lgc与pH的关系如图所示。已知溶液中离子浓度≤10-5 mol/L时认为沉淀完全。

浸出液用H2SO4调节pH的最佳范围是
调pH时
 转化的离子方程式为
转化的离子方程式为(5)一定温度下,利用K2Cr2O7可实现含苯酚废水的有效处理,工作原理如图所示,负极电极反应式为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】工业上以锂辉石(Li2O·A12O3·4SiO2,含少量Ca、Mg元素)为原料生产碳酸锂。其部分工艺流程如下:

已知:①Li2O·Al2O3·4SiO2+H2SO4(浓) =Li2SO4+Al2O3·4SiO2·H2O↓
②某些物质的溶解度(S)如下表所示。
(1)从滤渣1中分离出Al2O3的部分流程如下图所示,括号表示加入的试剂,方框表示所得到的物质。则步骤Ⅱ中反应的离子方程式是____________________________________________________________________ 。
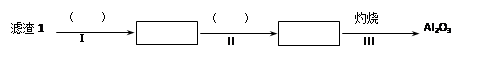
(2)已知滤渣2的主要成分有Mg(OH)2和CaCO3。
向滤液1中加入石灰乳的作用是(运用化学平衡移动原理解释)__________________________________________________ 。
(3)向滤液2中加入饱和Na2CO3溶液,过滤后,用“热水洗涤”的原因是________________________________________________________ 。
(4)工业上,将Li2CO3粗品制备成高纯Li2CO3的部分工艺如下。
a.将Li2CO3溶于盐酸作电解槽的阳极液,LiOH溶液作阴极液,两者用离子选择透过膜隔开,用惰性电极电解。
b.电解后向LiOH溶液中加入过量NH4HCO3溶液,过滤、烘干得高纯Li2CO3。
① a中,阳极的电极反应式是_____________________________ 。
②b中,生成Li2CO3反应的化学方程式是__________________________________ 。

已知:①Li2O·Al2O3·4SiO2+H2SO4(浓) =Li2SO4+Al2O3·4SiO2·H2O↓
②某些物质的溶解度(S)如下表所示。
| T/℃ | 20 | 40 | 60 | 80 |
| S(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 |
| S(Li2SO4)/g | 34.2 | 32.8 | 31.9 | 30.7 |
(1)从滤渣1中分离出Al2O3的部分流程如下图所示,括号表示加入的试剂,方框表示所得到的物质。则步骤Ⅱ中反应的离子方程式是
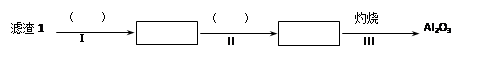
(2)已知滤渣2的主要成分有Mg(OH)2和CaCO3。
向滤液1中加入石灰乳的作用是(运用化学平衡移动原理解释)
(3)向滤液2中加入饱和Na2CO3溶液,过滤后,用“热水洗涤”的原因是
(4)工业上,将Li2CO3粗品制备成高纯Li2CO3的部分工艺如下。
a.将Li2CO3溶于盐酸作电解槽的阳极液,LiOH溶液作阴极液,两者用离子选择透过膜隔开,用惰性电极电解。
b.电解后向LiOH溶液中加入过量NH4HCO3溶液,过滤、烘干得高纯Li2CO3。
① a中,阳极的电极反应式是
②b中,生成Li2CO3反应的化学方程式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】二氧化锰是制造锌锰干电池的基本材料。工业上以软锰矿为原料,利用硫酸亚铁制备高纯度二氧化锰的流程如图1:

某软锰矿的主要成分为MnO2,还含有Si(16.27%)、Fe(5.86%)、Al(3.42%)、Zn(2.68%)和Cu(0.86%)等元素的化合物.部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH如表,回答下列问题
(1)硫酸亚铁在酸性条件下将MnO2还原为MnSO4,酸浸时发生的主要反应的化学方程式为__________ ;
(2)滤渣A的主要成分是____________ ;滤渣B的主要成分是__________________ ;
(3)加入MnS的目的是除去Cu2+、Zn2+杂质,可能原因是_________________ ;
(4)碱性锌锰电池是一种一次性电池,其结构如图2所示.该电池放电过程产生MnOOH.该电池的正极反应式为________________ ,电池总反应的方程式为_______________________ ;
(5)利用该碱性锌锰电池电解NO制备NH4NO3,其工作原理如图3所示,X电极__________ 极,电解时阳极的电极反应为________________ ,使电解产物全部转化为NH4NO3,需补充物质A,A是__________ ;

某软锰矿的主要成分为MnO2,还含有Si(16.27%)、Fe(5.86%)、Al(3.42%)、Zn(2.68%)和Cu(0.86%)等元素的化合物.部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH如表,回答下列问题
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Cu(OH)2 | Zn(OH)2 | CuS | ZnS | MnS | FeS |
| pH | 5.2 | 3.2 | 9.7 | 10.4 | 6.7 | 8.0 | ≥-0.42 | ≥2.5 | ≥7 | ≥7 |
(1)硫酸亚铁在酸性条件下将MnO2还原为MnSO4,酸浸时发生的主要反应的化学方程式为
(2)滤渣A的主要成分是
(3)加入MnS的目的是除去Cu2+、Zn2+杂质,可能原因是
(4)碱性锌锰电池是一种一次性电池,其结构如图2所示.该电池放电过程产生MnOOH.该电池的正极反应式为
(5)利用该碱性锌锰电池电解NO制备NH4NO3,其工作原理如图3所示,X电极
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】我国重晶石(BaSO4含量为90%以上)资源丰富,某工厂以重晶石为原料,生产“电子陶瓷工业支柱”——钛酸钡(BaTiO3)的工艺流程如下:
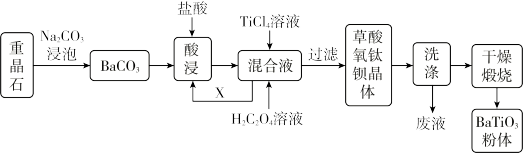
查阅资料可知:
①常温下: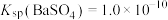 ,
,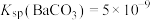 。
。
②草酸氧钛钡晶体的化学式为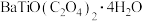 。
。
回答下列问题:
(1)为提高BaCO3的酸浸速率,可采取的措施为_____ (写出一条)。
(2)配制TiCl4溶液时通常将TiCl4固体溶于浓盐酸再加水稀释,其目的是_____ 。
(3)工业上用饱和Na2CO3溶液处理重晶石(假设杂质不与Na2CO3溶液作用),待达到平衡后,移走上层清液,重复多次操作,将BaSO4转化为易溶于酸的BaCO3,该过程用离子方程式可表示为_____ ,此反应的平衡常数K=_____ (填写计算结果)。若不考虑 的水解,则至少需要使用
的水解,则至少需要使用_____ mol·L-1的Na2CO3溶液浸泡BaSO4才能实现该转化过程。
(4)可循环使用的物质X是_____ (填化学式),设计实验方案验证草酸氧钛钡晶体是否洗涤干净:_____ 。
(5)在隔绝空气条件下,煅烧草酸氧钛钡晶体时有两种气体(水蒸气除外)生成,该反应的化学方程式为_____ 。

查阅资料可知:
①常温下:
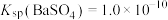 ,
,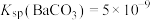 。
。②草酸氧钛钡晶体的化学式为
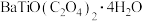 。
。回答下列问题:
(1)为提高BaCO3的酸浸速率,可采取的措施为
(2)配制TiCl4溶液时通常将TiCl4固体溶于浓盐酸再加水稀释,其目的是
(3)工业上用饱和Na2CO3溶液处理重晶石(假设杂质不与Na2CO3溶液作用),待达到平衡后,移走上层清液,重复多次操作,将BaSO4转化为易溶于酸的BaCO3,该过程用离子方程式可表示为
 的水解,则至少需要使用
的水解,则至少需要使用(4)可循环使用的物质X是
(5)在隔绝空气条件下,煅烧草酸氧钛钡晶体时有两种气体(水蒸气除外)生成,该反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】利用废铅蓄电池的铅泥(含PbSO4、PbO2和Pb)制备碱式碳酸铅[2PbCO3·Pb(OH)2]的工艺流程如下图所示:

已知:25℃时, ,
, ,
,
(1)“还原”时PbO2转化为PbO,则氧化剂与还原剂的物质的量之比为___________ 。
(2)“转化”时溶液中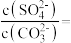
___________ 。
(3)“酸溶”时生成气体的化学方程式有___________ 。
(4)“调pH”获得2PbCO3·Pb(OH)2的相关反应:
ⅰ.
ⅱ.
产物产率与反应温度、反应后溶液pH关系如下表。
①85℃时,产物中PbCO3含量高于2PbCO3·Pb(OH)2是因为尿素水解速率___________ (填“大于”或“小于”) CO 结合Pb2+速率。
结合Pb2+速率。
②85~95℃,升高温度,2PbCO3·Pb(OH)2产率增加的原因为___________ 。
(5)称取9.085g粗产品,加热分解,测得产生1.100gCO2和0.180gH2O,则产品纯度为___________ (假设杂质只有PbCO3,计算结果保留3位有效数字)。

已知:25℃时,
 ,
, ,
,
(1)“还原”时PbO2转化为PbO,则氧化剂与还原剂的物质的量之比为
(2)“转化”时溶液中
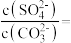
(3)“酸溶”时生成气体的化学方程式有
(4)“调pH”获得2PbCO3·Pb(OH)2的相关反应:
ⅰ.

ⅱ.

产物产率与反应温度、反应后溶液pH关系如下表。
| 反应温度/℃ | 反应终液pH值 | 2PbCO3·Pb(OH)2产率/% |
| 70 | 4.35 | 0 |
| 85 | 4.67 | 47.8 |
| 95 | 5.90 | 83.4 |
| 105 | 5.36 | 86.6 |
 结合Pb2+速率。
结合Pb2+速率。②85~95℃,升高温度,2PbCO3·Pb(OH)2产率增加的原因为
(5)称取9.085g粗产品,加热分解,测得产生1.100gCO2和0.180gH2O,则产品纯度为
您最近一年使用:0次
【推荐1】工业上以石煤(主要成分为V2O3,含有少量SiO2、P2O5等杂质)为原料制备钒的主要流程如图:
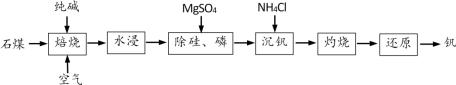
已知:①NH4VO3难溶于水。②Ksp(MgSiO3)=2.4×10-5,Ksp[Mg3(PO4)2]=2.7×10-27。
(1)焙烧:通入空气的条件下,向石煤中加纯碱焙烧,将V2O3转化为NaVO3的化学方程式为___ 。
(2)除硅、磷:
①用MgSO4溶液除硅、磷时,Si、P会形成Mg3(PO4)2、MgSiO3沉淀。若沉淀后溶液中c(PO )=1.0×10-8mol•L-1,则c(SiO
)=1.0×10-8mol•L-1,则c(SiO )=
)=___ mol•L-1。
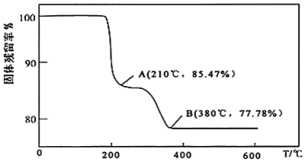
②如图所示,随着温度升高,除磷率下降,其原因是Mg3(PO4)2溶解度增大、___ ;随着温度升高,除硅率升高,其原因是___ 。

(3)沉钒:此过程反应温度需控制在50℃左右,温度不能过高的原因为___ 。
(4)灼烧:在灼烧NH4VO3的过程中,固体的残留率(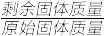 ×100%)随温度变化的曲线如图所示,则A~B段发生反应的方程式为
×100%)随温度变化的曲线如图所示,则A~B段发生反应的方程式为___ 。

已知:①NH4VO3难溶于水。②Ksp(MgSiO3)=2.4×10-5,Ksp[Mg3(PO4)2]=2.7×10-27。
(1)焙烧:通入空气的条件下,向石煤中加纯碱焙烧,将V2O3转化为NaVO3的化学方程式为
(2)除硅、磷:
①用MgSO4溶液除硅、磷时,Si、P会形成Mg3(PO4)2、MgSiO3沉淀。若沉淀后溶液中c(PO
 )=1.0×10-8mol•L-1,则c(SiO
)=1.0×10-8mol•L-1,则c(SiO )=
)=②如图所示,随着温度升高,除磷率下降,其原因是Mg3(PO4)2溶解度增大、

(3)沉钒:此过程反应温度需控制在50℃左右,温度不能过高的原因为
(4)灼烧:在灼烧NH4VO3的过程中,固体的残留率(
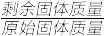 ×100%)随温度变化的曲线如图所示,则A~B段发生反应的方程式为
×100%)随温度变化的曲线如图所示,则A~B段发生反应的方程式为
您最近一年使用:0次
【推荐2】已知氢氧化钙和钨酸钙(CaWO4)都是微溶电解质,两者的溶解度均随温度升高而减小。在钨冶炼工艺中,将氢氧化钙加入钨酸钠碱性溶液中得到钨酸钙,发生反应Ⅰ: (aq)+Ca(OH)2(s)
(aq)+Ca(OH)2(s) CaWO4(s)+2OH-(aq)
CaWO4(s)+2OH-(aq)
(1)如图为不同温度下Ca(OH)2、CaWO4 的沉淀溶解平衡曲线。

①计算T1时,Ksp(CaWO4)=________ 。
②T1________ T2(填“>”“=”或“<”)。
(2)反应Ⅰ的平衡常数K理论值如表:
①该反应平衡常数K的表达式为________ 。
②该反应的ΔH________ 0(“>”“=”或“<”)。
③由于溶液中离子间的相互作用,实验测得的平衡常数与理论值相距甚远。50℃时,向一定体积的钨酸钠碱性溶液[c(Na2WO4)=c(NaOH)=0.5 mol·L-1]中,加入过量Ca(OH)2,反应达到平衡后 的沉淀率为60%,此时
的沉淀率为60%,此时 的平衡浓度为
的平衡浓度为________ mol·L-1,实验测得的平衡常数为________ (保留小数点后两位)。
(3)制取钨酸钙时,适时向反应混合液中添加适量盐酸,其作用是________ 。
 (aq)+Ca(OH)2(s)
(aq)+Ca(OH)2(s) CaWO4(s)+2OH-(aq)
CaWO4(s)+2OH-(aq)(1)如图为不同温度下Ca(OH)2、CaWO4 的沉淀溶解平衡曲线。

①计算T1时,Ksp(CaWO4)=
②T1
(2)反应Ⅰ的平衡常数K理论值如表:
| 温度/℃ | 25 | 50 | 90 | 100 |
| K | 79.96 | 208.06 | 222.88 | 258.05 |
①该反应平衡常数K的表达式为
②该反应的ΔH
③由于溶液中离子间的相互作用,实验测得的平衡常数与理论值相距甚远。50℃时,向一定体积的钨酸钠碱性溶液[c(Na2WO4)=c(NaOH)=0.5 mol·L-1]中,加入过量Ca(OH)2,反应达到平衡后
 的沉淀率为60%,此时
的沉淀率为60%,此时 的平衡浓度为
的平衡浓度为(3)制取钨酸钙时,适时向反应混合液中添加适量盐酸,其作用是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】草酸(H2C2O4)是一种二元酸。已知在常温下,草酸的电离常数K1=6×10-2,K2=6×10-5。草酸钙Ksp(CaC2O4)=4×10-8。请回答下列问题:
(1)常温下,NaHC2O4溶液的pH值_______ 7(填“>”“<”或“=”)。
(2)常温下,在足量NaHC2O4溶液中加入少量CaCl2固体,发生反应:Ca2++2HC2O =CaC2O4↓+H2C2O4。
=CaC2O4↓+H2C2O4。
①该反应的化学平衡常数表达式为:K=_______ 。
②若反应后溶液的pH值为2,此时,溶液中c(HC2O )×c(Ca2+)=
)×c(Ca2+)=_______ (计算结果保留两位有效数字)。
(3)一水草酸钙(CaC2O4∙H2O)制备方法如下:
步骤Ⅰ:用精制氯化钙溶液与草酸溶液共热,过滤,洗涤,将固体溶于热盐酸中;
步骤Ⅱ:加氨水反应得一水草酸钙,过滤,热水洗涤,在105℃干燥得产品。
步骤Ⅰ中反应需加热,关于加热的作用下列选项中正确的有_______ 。
A.加快反应速率 B.促进草酸电离 C.减少沉淀吸附杂质
(4)等物质的量的H2C2O4与NaOH反应生成NaHC2O4。基于此原理,某学生试图用甲基橙作指示剂,通过酸碱滴定测定草酸溶液浓度。
①甲基橙(用化学式HIn表示)本身是一种有机弱酸,其电离方程式为:HIn H++In-。酸根离子In-的颜色是
H++In-。酸根离子In-的颜色是_______ 。甲基橙的酸性与草酸相比,_______ (填“前者强”“前者弱”“几乎相等”或“无法判断”)。
②若在接近滴定终点时,用少量蒸馏水将锥形瓶内壁冲洗一下,再继续滴定至终点,则所测得草酸浓度会_______ (填“偏大”“偏小”或“无影响”)。
(1)常温下,NaHC2O4溶液的pH值
(2)常温下,在足量NaHC2O4溶液中加入少量CaCl2固体,发生反应:Ca2++2HC2O
 =CaC2O4↓+H2C2O4。
=CaC2O4↓+H2C2O4。①该反应的化学平衡常数表达式为:K=
②若反应后溶液的pH值为2,此时,溶液中c(HC2O
 )×c(Ca2+)=
)×c(Ca2+)=(3)一水草酸钙(CaC2O4∙H2O)制备方法如下:
步骤Ⅰ:用精制氯化钙溶液与草酸溶液共热,过滤,洗涤,将固体溶于热盐酸中;
步骤Ⅱ:加氨水反应得一水草酸钙,过滤,热水洗涤,在105℃干燥得产品。
步骤Ⅰ中反应需加热,关于加热的作用下列选项中正确的有
A.加快反应速率 B.促进草酸电离 C.减少沉淀吸附杂质
(4)等物质的量的H2C2O4与NaOH反应生成NaHC2O4。基于此原理,某学生试图用甲基橙作指示剂,通过酸碱滴定测定草酸溶液浓度。
①甲基橙(用化学式HIn表示)本身是一种有机弱酸,其电离方程式为:HIn
 H++In-。酸根离子In-的颜色是
H++In-。酸根离子In-的颜色是②若在接近滴定终点时,用少量蒸馏水将锥形瓶内壁冲洗一下,再继续滴定至终点,则所测得草酸浓度会
您最近一年使用:0次



