1 . 现有含AgBr的饱和溶液:
(1)AgBr的沉淀溶解平衡方程式:___________ ,Ksp的表达式是___________ ;
(2)加入固体AgNO3,则c(Ag+)___________ (填“变大”、“变小”或“不变”,下同);
(3)加入更多的AgBr固体,则c(Ag+)___________ ;
(1)AgBr的沉淀溶解平衡方程式:
(2)加入固体AgNO3,则c(Ag+)
(3)加入更多的AgBr固体,则c(Ag+)
您最近半年使用:0次
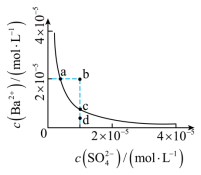
2 . 某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是 (aq)的平衡常数Ksp=c(Ba2+)·c(
(aq)的平衡常数Ksp=c(Ba2+)·c( ),称为溶度积常数。
),称为溶度积常数。
 (aq)的平衡常数Ksp=c(Ba2+)·c(
(aq)的平衡常数Ksp=c(Ba2+)·c( ),称为溶度积常数。
),称为溶度积常数。| A.加入Na2SO4可以使溶液由a点变到b点 |
| B.通过蒸发可以使溶液由d点变到c点 |
| C.d点有BaSO4沉淀生成 |
| D.a点对应的Ksp等于c点对应的Ksp |
您最近半年使用:0次
3 . 下列实验事实引出的结论不正确的是
| 选项 | 事实 | 结论 |
| A | 室温下,分别向2支试管中加入相同体积、相同浓度的Na2S2O3溶液,再分别加入相同体积不同浓度的稀硫酸,比较析出沉淀所需时间 | 当其他条件不变时,反应物浓度增大,化学反应速率加快 |
| B | 向FeCl3溶液中加入几滴KSCN溶液,溶液变红,然后加入少量铁粉,红色变浅 | 铁粉与KSCN溶液反应,减少了FeCl3与KSCN的反应 |
| C | 往浅黄色固体难溶物AgBr中加水,振荡,静置。取上层清液,然后加入NaI固体,产生黄色沉淀 | 难溶物存在沉淀溶解平衡 |
| D | A、B两支试管中分别加入等体积5%的H2O2溶液,在B中加入2~3滴FeCl3溶液,B试管中产生气泡快 | 当其他条件不变时,催化剂可以改变化学反应速率 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
4 . 下列有关电解质溶液的说法不正确的是
A.向0.1 的氨水中加入少量水,溶液中 的氨水中加入少量水,溶液中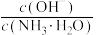 增大 增大 |
B.将 溶液从20℃升温至30℃,溶液中 溶液从20℃升温至30℃,溶液中 增大 增大 |
C.向氢氧化钠溶液中加入醋酸溶液至中性,溶液中 |
D.向 的饱和溶液中加入 的饱和溶液中加入 固体,溶液中的 固体,溶液中的 |
您最近半年使用:0次
名校
5 . 钒被称为“工业味精”,在发展现代工业、国防等方面发挥着重要的作用。 有强氧化性,在实验室以
有强氧化性,在实验室以 为原料制备氧钒(Ⅳ)碱式碳酸铵晶体,此晶体难溶于水,其化学式为
为原料制备氧钒(Ⅳ)碱式碳酸铵晶体,此晶体难溶于水,其化学式为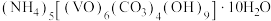 ,是制备热敏材料
,是制备热敏材料 的原料。过程如下:
的原料。过程如下:

已知:①氧化性: ;②
;② 能被
能被 氧化。
氧化。
1.步骤I中除生成 外,还生成绿色环保,无毒无害的产物,则反应的化学方程式为
外,还生成绿色环保,无毒无害的产物,则反应的化学方程式为___________ 。若只用浓盐酸与 反应也能制备
反应也能制备 溶液,从环保角度分析,使用
溶液,从环保角度分析,使用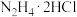 的目的是
的目的是___________ 。
步骤Ⅱ可在如图装置中进行: 被氧化,上述装置依次连接的合理顺序为c→
被氧化,上述装置依次连接的合理顺序为c→___________ (按气流方向,用小写字母表示)。盛有 溶液的仪器名称为
溶液的仪器名称为___________ 。
3.连接好装置,检查气密性良好后,加入试剂,开始实验,具体操作为___________ 。
4.实验结束时,将析出的产品过滤,用饱和 溶液洗涤。请从化学平衡的角度解释使用饱和
溶液洗涤。请从化学平衡的角度解释使用饱和 溶液洗涤晶体的原因:
溶液洗涤晶体的原因:___________ 。证明沉淀已经洗涤干净的方法是___________ 。
测定粗产品中钒的含量。实验步骤如下:
称量a g产品于锥形瓶中,用稀硫酸溶解后得到的溶液,加入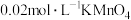 溶液至稍过量,加入某还原剂除去过量
溶液至稍过量,加入某还原剂除去过量 溶液,最后用
溶液,最后用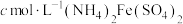 标准溶液滴定至终点(
标准溶液滴定至终点( ),消耗标准溶液的体积为b mL。
),消耗标准溶液的体积为b mL。
5.粗产品中钒的质量分数表达式为___________ (以 计,式量为67)。
计,式量为67)。
6.若 标准溶液部分变质,则测定结果
标准溶液部分变质,则测定结果___________ 。
A.偏高 B.偏低 C.无影响
 有强氧化性,在实验室以
有强氧化性,在实验室以 为原料制备氧钒(Ⅳ)碱式碳酸铵晶体,此晶体难溶于水,其化学式为
为原料制备氧钒(Ⅳ)碱式碳酸铵晶体,此晶体难溶于水,其化学式为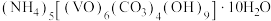 ,是制备热敏材料
,是制备热敏材料 的原料。过程如下:
的原料。过程如下:
已知:①氧化性:
 ;②
;② 能被
能被 氧化。
氧化。1.步骤I中除生成
 外,还生成绿色环保,无毒无害的产物,则反应的化学方程式为
外,还生成绿色环保,无毒无害的产物,则反应的化学方程式为 反应也能制备
反应也能制备 溶液,从环保角度分析,使用
溶液,从环保角度分析,使用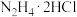 的目的是
的目的是步骤Ⅱ可在如图装置中进行:

 被氧化,上述装置依次连接的合理顺序为c→
被氧化,上述装置依次连接的合理顺序为c→ 溶液的仪器名称为
溶液的仪器名称为3.连接好装置,检查气密性良好后,加入试剂,开始实验,具体操作为
4.实验结束时,将析出的产品过滤,用饱和
 溶液洗涤。请从化学平衡的角度解释使用饱和
溶液洗涤。请从化学平衡的角度解释使用饱和 溶液洗涤晶体的原因:
溶液洗涤晶体的原因:测定粗产品中钒的含量。实验步骤如下:
称量a g产品于锥形瓶中,用稀硫酸溶解后得到的溶液,加入
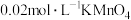 溶液至稍过量,加入某还原剂除去过量
溶液至稍过量,加入某还原剂除去过量 溶液,最后用
溶液,最后用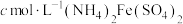 标准溶液滴定至终点(
标准溶液滴定至终点( ),消耗标准溶液的体积为b mL。
),消耗标准溶液的体积为b mL。5.粗产品中钒的质量分数表达式为
 计,式量为67)。
计,式量为67)。6.若
 标准溶液部分变质,则测定结果
标准溶液部分变质,则测定结果A.偏高 B.偏低 C.无影响
您最近半年使用:0次
名校
6 . 黑色 的水溶性很差.已知:
的水溶性很差.已知: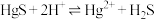 平衡常数
平衡常数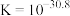 ,
,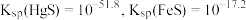 .下列有关说法错误的是
.下列有关说法错误的是
 的水溶性很差.已知:
的水溶性很差.已知: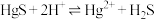 平衡常数
平衡常数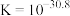 ,
,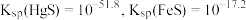 .下列有关说法错误的是
.下列有关说法错误的是A.降低 可以增大 可以增大 的溶解量 的溶解量 |
B.可将 气体通入 气体通入 水溶液中制备 水溶液中制备 |
C. 的电离平衡常数的乘积 的电离平衡常数的乘积 |
D.用 除废水中 除废水中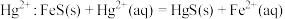 ,平衡常数 ,平衡常数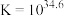 |
您最近半年使用:0次
2024-04-20更新
|
188次组卷
|
3卷引用:安徽省淮北市2024届高三第一次质量检测(一模)化学试题
安徽省淮北市2024届高三第一次质量检测(一模)化学试题(已下线)通关练10 盘点溶液中的“四大”平衡-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)2024届天津市宁河区芦台第一中学高三下学期第三次模拟化学试题
7 . 常温下,向含 、
、 和
和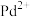 的溶液中滴加
的溶液中滴加 溶液,混合物中
溶液,混合物中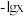 [
[ 、
、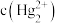 、
、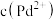 ]与
]与 关系如图所示。已知常温下,
关系如图所示。已知常温下,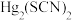 的溶解度大于
的溶解度大于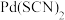 ;溶液为过饱和状态时,振荡或搅拌即可使晶体析出。下列叙述错误的是
;溶液为过饱和状态时,振荡或搅拌即可使晶体析出。下列叙述错误的是
 、
、 和
和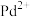 的溶液中滴加
的溶液中滴加 溶液,混合物中
溶液,混合物中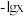 [
[ 、
、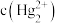 、
、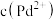 ]与
]与 关系如图所示。已知常温下,
关系如图所示。已知常温下,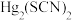 的溶解度大于
的溶解度大于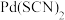 ;溶液为过饱和状态时,振荡或搅拌即可使晶体析出。下列叙述错误的是
;溶液为过饱和状态时,振荡或搅拌即可使晶体析出。下列叙述错误的是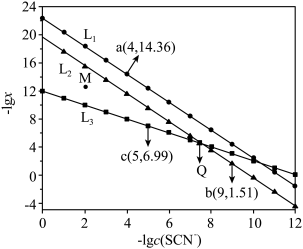
A.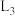 代表 代表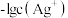 和 和 的关系 的关系 |
B.在M点对应溶液中须加入 才能使 才能使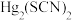 晶体析出 晶体析出 |
C.Q点坐标为 |
D.当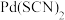 和 和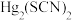 完全共沉时,上层清液中 完全共沉时,上层清液中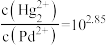 |
您最近半年使用:0次
2024-04-19更新
|
79次组卷
|
2卷引用:2024届陕西省商洛市高三下学期第三次尖子生学情诊断考试理综试题-高中化学
8 . 一定温度下,AgCl和Ag2C2O4两种难溶化合物的溶解平衡曲线如图所示,下列说法中错误的是
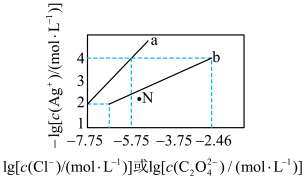
| A.a代表AgCl溶解平衡图像 |
| B.N点为Ag2C2O4的过饱和溶液 |
C.该温度下,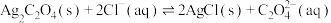 的平衡常数为10-0.71 的平衡常数为10-0.71 |
| D.向NaCl、Na2C2O4均为0.1 mol/L的混合溶液中滴加AgNO3溶液,Cl-先沉淀 |
您最近半年使用:0次
9 . 某温度下,两种难溶盐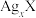 、
、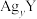 的饱和溶液中
的饱和溶液中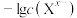 或
或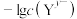 与
与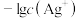 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是
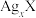 、
、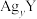 的饱和溶液中
的饱和溶液中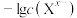 或
或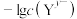 与
与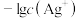 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是
A.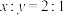 |
B.a点时, , ,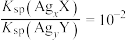 |
C. 平衡常数 平衡常数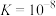 |
| D.向浓度均为0.1mol/L的NaxX、NayY混合溶液中滴加AgNO3溶液,先产生AgyY沉淀 |
您最近半年使用:0次
2024-04-17更新
|
237次组卷
|
3卷引用:广西壮族自治区柳州市2024届高三第三次模拟考试化学试题
广西壮族自治区柳州市2024届高三第三次模拟考试化学试题广西柳州市2024届高三下学期第三次模拟考试(三模)化学试题(已下线)通关练10 盘点溶液中的“四大”平衡-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)
解题方法
10 . 结合已有知识,根据下列实验操作,其对应的现象和结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将乙醇和浓硫酸混合溶液加热到170℃,并将产生的气体经过氢氧化钠溶液洗气,再通入溴水 | 溴水褪色 | 有乙烯生成 |
| B | 常温下将铁片分别插入稀硝酸和浓硝酸中 | 前者产生无色气体,后者无明显现象 | 稀硝酸的氧化性比浓硝酸强 |
| C | 已知 : : 、 、 : :  ,向饱和溶液中滴加碳酸钠溶液 ,向饱和溶液中滴加碳酸钠溶液 | 无明显现象 |  与碳酸钠不反应 与碳酸钠不反应 |
| D | 向少量 悬浊液中加入足量饱和 悬浊液中加入足量饱和 溶液 溶液 | 沉淀颜色会由黑色变为浅红色( 为浅红色) 为浅红色) | Ksp(FeS)>Ksp(MnS) |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次



