名校
1 . 钒被称为“工业味精”,在发展现代工业、国防等方面发挥着重要的作用。 有强氧化性,在实验室以
有强氧化性,在实验室以 为原料制备氧钒(Ⅳ)碱式碳酸铵晶体,此晶体难溶于水,其化学式为
为原料制备氧钒(Ⅳ)碱式碳酸铵晶体,此晶体难溶于水,其化学式为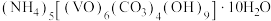 ,是制备热敏材料
,是制备热敏材料 的原料。过程如下:
的原料。过程如下:

已知:①氧化性: ;②
;② 能被
能被 氧化。
氧化。
1.步骤I中除生成 外,还生成绿色环保,无毒无害的产物,则反应的化学方程式为
外,还生成绿色环保,无毒无害的产物,则反应的化学方程式为___________ 。若只用浓盐酸与 反应也能制备
反应也能制备 溶液,从环保角度分析,使用
溶液,从环保角度分析,使用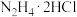 的目的是
的目的是___________ 。
步骤Ⅱ可在如图装置中进行: 被氧化,上述装置依次连接的合理顺序为c→
被氧化,上述装置依次连接的合理顺序为c→___________ (按气流方向,用小写字母表示)。盛有 溶液的仪器名称为
溶液的仪器名称为___________ 。
3.连接好装置,检查气密性良好后,加入试剂,开始实验,具体操作为___________ 。
4.实验结束时,将析出的产品过滤,用饱和 溶液洗涤。请从化学平衡的角度解释使用饱和
溶液洗涤。请从化学平衡的角度解释使用饱和 溶液洗涤晶体的原因:
溶液洗涤晶体的原因:___________ 。证明沉淀已经洗涤干净的方法是___________ 。
测定粗产品中钒的含量。实验步骤如下:
称量a g产品于锥形瓶中,用稀硫酸溶解后得到的溶液,加入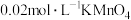 溶液至稍过量,加入某还原剂除去过量
溶液至稍过量,加入某还原剂除去过量 溶液,最后用
溶液,最后用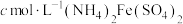 标准溶液滴定至终点(
标准溶液滴定至终点( ),消耗标准溶液的体积为b mL。
),消耗标准溶液的体积为b mL。
5.粗产品中钒的质量分数表达式为___________ (以 计,式量为67)。
计,式量为67)。
6.若 标准溶液部分变质,则测定结果
标准溶液部分变质,则测定结果___________ 。
A.偏高 B.偏低 C.无影响
 有强氧化性,在实验室以
有强氧化性,在实验室以 为原料制备氧钒(Ⅳ)碱式碳酸铵晶体,此晶体难溶于水,其化学式为
为原料制备氧钒(Ⅳ)碱式碳酸铵晶体,此晶体难溶于水,其化学式为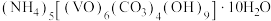 ,是制备热敏材料
,是制备热敏材料 的原料。过程如下:
的原料。过程如下:
已知:①氧化性:
 ;②
;② 能被
能被 氧化。
氧化。1.步骤I中除生成
 外,还生成绿色环保,无毒无害的产物,则反应的化学方程式为
外,还生成绿色环保,无毒无害的产物,则反应的化学方程式为 反应也能制备
反应也能制备 溶液,从环保角度分析,使用
溶液,从环保角度分析,使用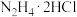 的目的是
的目的是步骤Ⅱ可在如图装置中进行:

 被氧化,上述装置依次连接的合理顺序为c→
被氧化,上述装置依次连接的合理顺序为c→ 溶液的仪器名称为
溶液的仪器名称为3.连接好装置,检查气密性良好后,加入试剂,开始实验,具体操作为
4.实验结束时,将析出的产品过滤,用饱和
 溶液洗涤。请从化学平衡的角度解释使用饱和
溶液洗涤。请从化学平衡的角度解释使用饱和 溶液洗涤晶体的原因:
溶液洗涤晶体的原因:测定粗产品中钒的含量。实验步骤如下:
称量a g产品于锥形瓶中,用稀硫酸溶解后得到的溶液,加入
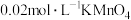 溶液至稍过量,加入某还原剂除去过量
溶液至稍过量,加入某还原剂除去过量 溶液,最后用
溶液,最后用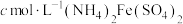 标准溶液滴定至终点(
标准溶液滴定至终点( ),消耗标准溶液的体积为b mL。
),消耗标准溶液的体积为b mL。5.粗产品中钒的质量分数表达式为
 计,式量为67)。
计,式量为67)。6.若
 标准溶液部分变质,则测定结果
标准溶液部分变质,则测定结果A.偏高 B.偏低 C.无影响
您最近半年使用:0次
名校
解题方法
2 . T℃时, 和
和 的沉淀溶解平衡曲线如图所示。已知:
的沉淀溶解平衡曲线如图所示。已知: ,
, 或
或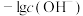 。下列说法正确的是
。下列说法正确的是

 和
和 的沉淀溶解平衡曲线如图所示。已知:
的沉淀溶解平衡曲线如图所示。已知: ,
, 或
或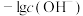 。下列说法正确的是
。下列说法正确的是
A.T℃时, |
B.Y点对应的 溶液是不饱和溶液 溶液是不饱和溶液 |
C.Z点对应的溶液中,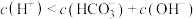 |
D.向 悬浊液中通入 悬浊液中通入 气体(忽略溶液体积的变化),溶液中 气体(忽略溶液体积的变化),溶液中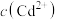 保持不变 保持不变 |
您最近半年使用:0次
名校
3 . I.请回答。
(1)按照有机物的命名规则,下列命名正确的是___________ 。
A.3-乙基己烷 B.2-乙基戊烷, C.1,2-二甲基丁烷 D.4-甲基戊烷
写出该物质的结构简式:___________ 。
Ⅱ.如图所示,U形管的左端用橡胶塞封闭,充有甲烷和氯气(体积比为1:4)的混合气体,假定氯气在水中的溶解可以忽略不计。将封闭有甲烷和氯气混合气体的装置放置在有漫射光的地方让混合气体缓慢反应一段时间。
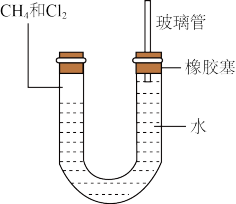
(2)经过几个小时的反应,U形管右端的水面变化是___________ (A升高;B降低;C不变);右端玻璃管的作用是___________ 。
(3)若水中含有Na2SiO3,则在U形管左端会观察到现象是___________ ;若水中含有AgNO3,则水中反应离子方程式___________ 。
(4)若题目中甲烷与氯气的体积比为1:1,则得到的产物为___________(填字母)。
(5)若把1体积CH4和4体积Cl2组成的混合气体充入大试管中,将此试管倒立在盛有饱和食盐水的水槽里,放在光亮处,试推测可观察到的现象是___________ 。
①黄绿色逐渐消失 ②试管壁上有黄色油珠出现
③水位在试管内上升到一定高度 ④水槽内有少量晶体析出
⑤液面上有白雾
(1)按照有机物的命名规则,下列命名正确的是
A.3-乙基己烷 B.2-乙基戊烷, C.1,2-二甲基丁烷 D.4-甲基戊烷
写出该物质的结构简式:
Ⅱ.如图所示,U形管的左端用橡胶塞封闭,充有甲烷和氯气(体积比为1:4)的混合气体,假定氯气在水中的溶解可以忽略不计。将封闭有甲烷和氯气混合气体的装置放置在有漫射光的地方让混合气体缓慢反应一段时间。

(2)经过几个小时的反应,U形管右端的水面变化是
(3)若水中含有Na2SiO3,则在U形管左端会观察到现象是
(4)若题目中甲烷与氯气的体积比为1:1,则得到的产物为___________(填字母)。
| A.CH3Cl、HCl | B.CCl4、HCl |
| C.CH3Cl、CH2Cl2 | D.CH3Cl、CH2Cl2、CHCl3、CCl4、HCl |
(5)若把1体积CH4和4体积Cl2组成的混合气体充入大试管中,将此试管倒立在盛有饱和食盐水的水槽里,放在光亮处,试推测可观察到的现象是
①黄绿色逐渐消失 ②试管壁上有黄色油珠出现
③水位在试管内上升到一定高度 ④水槽内有少量晶体析出
⑤液面上有白雾
您最近半年使用:0次
名校
4 . 下列关于沉淀溶解平衡的说法正确的是
| A.沉淀溶解达到平衡时,溶液中溶质的离子浓度相等,且保持不变 |
| B.沉淀溶解平衡是可逆的 |
C.在平衡状态时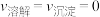 |
| D.达到沉淀溶解平衡的溶液不一定是饱和溶液 |
您最近半年使用:0次
名校
解题方法
5 . I.钴的配合物制取
实验室以活性炭为催化剂,用CoCl2制取[Co(NH3)6]Cl3,装置如图所示。

(1)仪器a的名称是___________ ;仪器b中的试剂是___________ ;冷凝管作用是___________ 。
II.将0.1 mol/L CoCl2、NH4Cl混合液在三颈烧瓶中混合,滴加浓氨水,溶液变为棕色。已知:①[Co(NH3)6]2+具有较强还原性;溶液呈棕色。②Ksp[Co(OH)2] = 6×10-15
(2)请计算常温下该混合液中Co2+开始沉淀的pH值(精确到0.01),列出必要过程________ 。NH4Cl的作用是___________ 。
(3)充分反应后缓慢滴加双氧水,水浴加热20 min(该过程生成OH-)。发生反应的离子方程式为___________ 。将反应后的混合液冷却后加入适量浓盐酸,过滤、洗涤、干燥,得到[Co(NH3)6]Cl3晶体。
III.已知[Co(NH3)6]Cl3可溶于热水,微溶于冷水,难溶于乙醇。
(4)请运用平衡移动原理解释加入浓盐酸的目的是_____________ 。
(5)[Co(NH3)6]3+ Co3+ + 6NH3 K1;
Co3+ + 6NH3 K1;
 NH3 + H+ K2,判断K1
NH3 + H+ K2,判断K1____ (K2)6。(填“>”“<”或“=”)
(6)洗涤[Co(NH3)6]Cl3时可用___________。
IV.测定产品中配体NH3与外界Cl-的物质的量之比。实验如下:
①蒸氨:取0.100 g样品加入三颈烧瓶中,再加入足量NaOH溶液并充分加热,蒸出的气体全部通入V1 mL c1 mol/L的H2SO4中。
②滴定:用c2 mol/L NaOH溶液滴定①中溶液,消耗V2 mL NaOH溶液。
③沉淀:另取0.100 g样品溶解,加入足量AgNO3溶液,过滤、洗涤、干燥、恒重,得到沉淀m3 g。(MAgCl = 143.5 g/mol)
(7)滴定时选用的指示剂为___________ 。
(8)测得产品中配体NH3与外界Cl-的物质的量比值为________ 。(用含c1、V1等数据的代数式表示)若测得n(NH3) : n(Cl-)比值偏小,可能的原因是________ 。
A.蒸氨结束时,未用蒸馏水洗涤冷凝管,并将洗涤液一并倒入H2SO4中
B.滴定步骤的NaOH溶液使用前敞口放置于空气中一段时间
C.滴定步骤中盛放NaOH溶液的滴定管未用NaOH溶液润洗
D.沉淀步骤中,沉淀未完全转移至漏斗中
实验室以活性炭为催化剂,用CoCl2制取[Co(NH3)6]Cl3,装置如图所示。

(1)仪器a的名称是
II.将0.1 mol/L CoCl2、NH4Cl混合液在三颈烧瓶中混合,滴加浓氨水,溶液变为棕色。已知:①[Co(NH3)6]2+具有较强还原性;溶液呈棕色。②Ksp[Co(OH)2] = 6×10-15
(2)请计算常温下该混合液中Co2+开始沉淀的pH值(精确到0.01),列出必要过程
(3)充分反应后缓慢滴加双氧水,水浴加热20 min(该过程生成OH-)。发生反应的离子方程式为
III.已知[Co(NH3)6]Cl3可溶于热水,微溶于冷水,难溶于乙醇。
(4)请运用平衡移动原理解释加入浓盐酸的目的是
(5)[Co(NH3)6]3+
 Co3+ + 6NH3 K1;
Co3+ + 6NH3 K1;
 NH3 + H+ K2,判断K1
NH3 + H+ K2,判断K1(6)洗涤[Co(NH3)6]Cl3时可用___________。
| A.蒸馏水 | B.冰水 | C.无水乙醇 | D.50%乙醇水溶液 |
IV.测定产品中配体NH3与外界Cl-的物质的量之比。实验如下:
①蒸氨:取0.100 g样品加入三颈烧瓶中,再加入足量NaOH溶液并充分加热,蒸出的气体全部通入V1 mL c1 mol/L的H2SO4中。
②滴定:用c2 mol/L NaOH溶液滴定①中溶液,消耗V2 mL NaOH溶液。
③沉淀:另取0.100 g样品溶解,加入足量AgNO3溶液,过滤、洗涤、干燥、恒重,得到沉淀m3 g。(MAgCl = 143.5 g/mol)
(7)滴定时选用的指示剂为
(8)测得产品中配体NH3与外界Cl-的物质的量比值为
A.蒸氨结束时,未用蒸馏水洗涤冷凝管,并将洗涤液一并倒入H2SO4中
B.滴定步骤的NaOH溶液使用前敞口放置于空气中一段时间
C.滴定步骤中盛放NaOH溶液的滴定管未用NaOH溶液润洗
D.沉淀步骤中,沉淀未完全转移至漏斗中
您最近半年使用:0次
名校
解题方法
6 . 门捷列夫最早预言了具有半导体特性类硅元素锗(32Ge),工业上用精硫锗矿(主要成分为 )制取高纯度锗,其工艺流程如图所示:
)制取高纯度锗,其工艺流程如图所示:
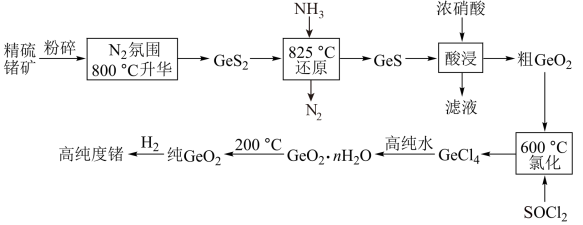
已知:①硅和锗是同主族相邻元素,结构和性质类似;
② 在
在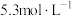 的盐酸中溶解度最小。
的盐酸中溶解度最小。
(1)基态锗原子的价层电子排布式为___________ ,晶体锗的晶体类型是___________ 。
(2)① ,使精硫锗矿在
,使精硫锗矿在 氛围中升华的原因是
氛围中升华的原因是___________ 。
②还原时发生反应:___________ ___________
___________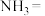 ___________
___________ ___________
___________ ___________
___________ 。配平上述反应的化学方程式,标出电子转移的方向和数目
。配平上述反应的化学方程式,标出电子转移的方向和数目______________ 。
③比较键角:
___________  (选填编号)。其原因是
(选填编号)。其原因是___________ 。
A.> B.< C.=
(3)酸浸时温度不能过高的原因是___________ 。氯化除生成 外,反应还生成一种V形分子,相应的化学方程式为
外,反应还生成一种V形分子,相应的化学方程式为___________ 。 水解得到
水解得到 ,该步骤高纯水不能过量,原因是
,该步骤高纯水不能过量,原因是___________ 。
(4) 与碱反应可生成锗酸盐,其中
与碱反应可生成锗酸盐,其中 是一种难溶电解质,一定温度下,
是一种难溶电解质,一定温度下, 在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是___________(选填编号)。
在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是___________(选填编号)。
 )制取高纯度锗,其工艺流程如图所示:
)制取高纯度锗,其工艺流程如图所示:
已知:①硅和锗是同主族相邻元素,结构和性质类似;
②
 在
在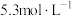 的盐酸中溶解度最小。
的盐酸中溶解度最小。(1)基态锗原子的价层电子排布式为
(2)①
 ,使精硫锗矿在
,使精硫锗矿在 氛围中升华的原因是
氛围中升华的原因是②还原时发生反应:___________
 ___________
___________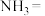 ___________
___________ ___________
___________ ___________
___________ 。配平上述反应的化学方程式,标出电子转移的方向和数目
。配平上述反应的化学方程式,标出电子转移的方向和数目③比较键角:

 (选填编号)。其原因是
(选填编号)。其原因是A.> B.< C.=
(3)酸浸时温度不能过高的原因是
 外,反应还生成一种V形分子,相应的化学方程式为
外,反应还生成一种V形分子,相应的化学方程式为 水解得到
水解得到 ,该步骤高纯水不能过量,原因是
,该步骤高纯水不能过量,原因是(4)
 与碱反应可生成锗酸盐,其中
与碱反应可生成锗酸盐,其中 是一种难溶电解质,一定温度下,
是一种难溶电解质,一定温度下, 在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是___________(选填编号)。
在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是___________(选填编号)。
A.n点与p点对应的 相等 相等 |
B.q点无 沉淀生成 沉淀生成 |
| C.通过蒸发可以使溶液由q点变到p点 |
D.加入 可以使溶液由n点变到m点 可以使溶液由n点变到m点 |
您最近半年使用:0次
名校
7 . 25℃时,用 沉淀
沉淀 、
、 两种金属离子(
两种金属离子( ),所需
),所需 最低浓度的对数值
最低浓度的对数值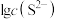 与
与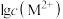 的关系如图所示,请回答:
的关系如图所示,请回答:

(1)25℃时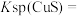
___________ 。
(2)25℃时向50mL的 、
、 浓度均为0.01mol/L的混合溶液中逐滴加入
浓度均为0.01mol/L的混合溶液中逐滴加入 溶液,当
溶液,当 溶液加到150mL时开始生成SnS沉淀,则此时溶液中
溶液加到150mL时开始生成SnS沉淀,则此时溶液中 浓度为
浓度为___________ mol/L。
 沉淀
沉淀 、
、 两种金属离子(
两种金属离子( ),所需
),所需 最低浓度的对数值
最低浓度的对数值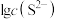 与
与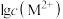 的关系如图所示,请回答:
的关系如图所示,请回答:
(1)25℃时
(2)25℃时向50mL的
 、
、 浓度均为0.01mol/L的混合溶液中逐滴加入
浓度均为0.01mol/L的混合溶液中逐滴加入 溶液,当
溶液,当 溶液加到150mL时开始生成SnS沉淀,则此时溶液中
溶液加到150mL时开始生成SnS沉淀,则此时溶液中 浓度为
浓度为
您最近半年使用:0次
名校
8 . 硫化镉(CdS)是一种难溶于水的黄色颜料,其在水中的沉淀溶解平衡曲线如下图所示。下列说法错误的是
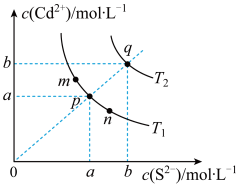

A.图中p和q分别为 、 、 温度下CdS达到沉淀溶解平衡 温度下CdS达到沉淀溶解平衡 |
B.图中各点对应的 的关系为: 的关系为: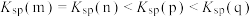 |
C.向m点的溶液中加入少量 固体,溶液中 固体,溶液中 浓度降低 浓度降低 |
| D.温度降低时,q点饱和溶液的组成由q沿qp线向p方向移动 |
您最近半年使用:0次
2023-07-11更新
|
969次组卷
|
7卷引用:上海市行知中学2023-2024学年高三上学期第二次质量监测化学试题
9 . 钴配合物 溶于热水,在冷水中微溶,可通过如下反应制备:
溶于热水,在冷水中微溶,可通过如下反应制备: 。
。
具体步骤如下:
Ⅰ.称取 ,用
,用 水溶解。
水溶解。
Ⅱ.分批加入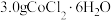 后,将溶液温度降至
后,将溶液温度降至 以下,加入
以下,加入 活性炭、
活性炭、 浓氨水,搅拌下逐滴加入
浓氨水,搅拌下逐滴加入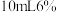 的双氧水。
的双氧水。
Ⅲ.加热至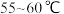 反应
反应 。冷却,过滤。
。冷却,过滤。
Ⅳ.将滤得的固体转入含有少量盐酸的 沸水中,趁热过滤。
沸水中,趁热过滤。
Ⅴ.滤液转入烧杯,加入 浓盐酸,冷却、过滤、干燥,得到橙黄色晶体。
浓盐酸,冷却、过滤、干燥,得到橙黄色晶体。
回答下列问题:
(1)步骤Ⅰ中使用的部分仪器如下。_______ 。加快NH4Cl溶解的操作有_______ 。
(2)步骤Ⅱ中,将温度降至10℃以下以避免_______ 、_______ ;可选用_______ 降低溶液温度。
(3)指出下列过滤操作中不规范之处:_______ 。_______ 。
(5)步骤Ⅴ中加入浓盐酸的目的是_______ 。
 溶于热水,在冷水中微溶,可通过如下反应制备:
溶于热水,在冷水中微溶,可通过如下反应制备: 。
。具体步骤如下:
Ⅰ.称取
 ,用
,用 水溶解。
水溶解。Ⅱ.分批加入
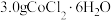 后,将溶液温度降至
后,将溶液温度降至 以下,加入
以下,加入 活性炭、
活性炭、 浓氨水,搅拌下逐滴加入
浓氨水,搅拌下逐滴加入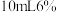 的双氧水。
的双氧水。Ⅲ.加热至
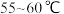 反应
反应 。冷却,过滤。
。冷却,过滤。Ⅳ.将滤得的固体转入含有少量盐酸的
 沸水中,趁热过滤。
沸水中,趁热过滤。Ⅴ.滤液转入烧杯,加入
 浓盐酸,冷却、过滤、干燥,得到橙黄色晶体。
浓盐酸,冷却、过滤、干燥,得到橙黄色晶体。回答下列问题:
(1)步骤Ⅰ中使用的部分仪器如下。
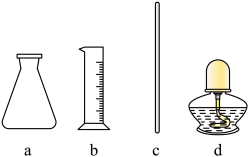
(2)步骤Ⅱ中,将温度降至10℃以下以避免
(3)指出下列过滤操作中不规范之处:
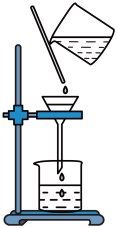
(5)步骤Ⅴ中加入浓盐酸的目的是
您最近半年使用:0次
2023-06-09更新
|
12597次组卷
|
16卷引用:上海市华东师范大学第二附属中学(紫竹校区)2023-2024学年高三下学期三模考试 化学试题
上海市华东师范大学第二附属中学(紫竹校区)2023-2024学年高三下学期三模考试 化学试题2023年高考全国甲卷化学真题(已下线)T27-实验题(已下线)2023年高考化学真题完全解读(全国甲卷)(ppt+word)(已下线)专题19 实验综合题(已下线)2023年高考山东卷化学真题变式题(实验综合题)(已下线)专题19 实验综合题(已下线)专题19 实验综合题(已下线)第18练 化学实验综合题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)考点巩固卷13 化学实验基础(二)(3个考点30题)-2024年高考化学一轮复习考点通关卷(新高考通用)(已下线)专题15 化学实验综合题-2023年高考化学真题题源解密(新高考专用)(已下线)专题14 化学实验综合题-2023年高考化学真题题源解密(全国通用)(已下线)第14讲化学实验常用仪器及基本操作(已下线)考点44 化学实验基础(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)题型一 实验简答题答题规范-备战2024年高考化学答题技巧与模板构建甘肃省平凉市泾川县第三中学2023-2024学年高三上学期第3次月考化学试题
名校
10 . 已知25℃时,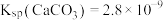 ,
, 式量为100。
式量为100。
(1)书写表示 沉淀溶解平衡的方程式
沉淀溶解平衡的方程式___________ 。
(2)计算25℃ 的溶解度
的溶解度___________  水。(保留2位有效数字)
水。(保留2位有效数字)
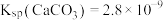 ,
, 式量为100。
式量为100。(1)书写表示
 沉淀溶解平衡的方程式
沉淀溶解平衡的方程式(2)计算25℃
 的溶解度
的溶解度 水。(保留2位有效数字)
水。(保留2位有效数字)
您最近半年使用:0次



