25℃时,用 沉淀
沉淀 、
、 两种金属离子(
两种金属离子( ),所需
),所需 最低浓度的对数值
最低浓度的对数值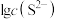 与
与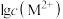 的关系如图所示,请回答:
的关系如图所示,请回答:

(1)25℃时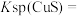
___________ 。
(2)25℃时向50mL的 、
、 浓度均为0.01mol/L的混合溶液中逐滴加入
浓度均为0.01mol/L的混合溶液中逐滴加入 溶液,当
溶液,当 溶液加到150mL时开始生成SnS沉淀,则此时溶液中
溶液加到150mL时开始生成SnS沉淀,则此时溶液中 浓度为
浓度为___________ mol/L。
 沉淀
沉淀 、
、 两种金属离子(
两种金属离子( ),所需
),所需 最低浓度的对数值
最低浓度的对数值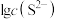 与
与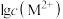 的关系如图所示,请回答:
的关系如图所示,请回答:
(1)25℃时
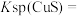
(2)25℃时向50mL的
 、
、 浓度均为0.01mol/L的混合溶液中逐滴加入
浓度均为0.01mol/L的混合溶液中逐滴加入 溶液,当
溶液,当 溶液加到150mL时开始生成SnS沉淀,则此时溶液中
溶液加到150mL时开始生成SnS沉淀,则此时溶液中 浓度为
浓度为
更新时间:2023-09-18 13:03:57
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】(1)常温下,有浓度均为0.1mol/L的三种溶液:a.NaHCO3;b.NaClO;c.CH3COONa。
①三种溶液pH由大到小的顺序为:__________________ 填序号)。
②溶液a的pH大于8,则溶液中c(H2CO3)____ c(CO32-) (填“>”、“<”或“=”)。
(2)已知25℃时,Ksp[AgCl]=1.8×10-10,现将足量氯化银分别放入:a.100mL蒸馏水中;b.100mL 0.2 mol/LAgNO3溶液中;c.100mL 0.1 mol/L氯化铝溶液中;d.100mL 0.1 mol/L盐酸溶液中。充分搅拌后,相同温度下银离子浓度由大到小的顺序是________ 。 (填写序号);b中氯离子的浓度为_______ mol/L。
①三种溶液pH由大到小的顺序为:
②溶液a的pH大于8,则溶液中c(H2CO3)
(2)已知25℃时,Ksp[AgCl]=1.8×10-10,现将足量氯化银分别放入:a.100mL蒸馏水中;b.100mL 0.2 mol/LAgNO3溶液中;c.100mL 0.1 mol/L氯化铝溶液中;d.100mL 0.1 mol/L盐酸溶液中。充分搅拌后,相同温度下银离子浓度由大到小的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题:
(1) 溶液显酸性,试用离子方程式解释其原因
溶液显酸性,试用离子方程式解释其原因________ 。
(2)氯化银在水中存在沉淀溶解平衡:AgCl(s)⇌Ag+(aq)+Cl-(aq),在25C时,氯化银的 ,现将足量氯化银分别放入:①
,现将足量氯化银分别放入:①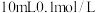 氯化镁溶液中,②
氯化镁溶液中,②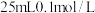 硝酸银溶液中,③
硝酸银溶液中,③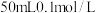 氯化铝溶液中,④
氯化铝溶液中,④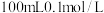 盐酸溶液中。充分搅拌后,相同温度下银离子浓度由大到小的顺序是
盐酸溶液中。充分搅拌后,相同温度下银离子浓度由大到小的顺序是___________ (填写序号)。
(3)下表所示的是常温下,某些弱酸的电离常数,请根据要求作答。
①相同物质的量浓度的 和
和 的混合溶液中离子浓度由大到小的顺序为
的混合溶液中离子浓度由大到小的顺序为_________ 。
②请判断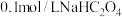 溶液显
溶液显_________ 性(填“酸”、“碱”或“中”)。
③下列离子方程式书写正确的是_______ 。
A. HC2O4-+SO32-═HSO3-+C2O42-
B. 2CH3COOH+SO32-═2CH3COO-+H2O+SO2↑
C. SO2+H2O+2CH3COO-═2CH3COOH+SO32-
D. 2CO32-+SO2+H2O═2HCO3-+SO32-
(1)
 溶液显酸性,试用离子方程式解释其原因
溶液显酸性,试用离子方程式解释其原因(2)氯化银在水中存在沉淀溶解平衡:AgCl(s)⇌Ag+(aq)+Cl-(aq),在25C时,氯化银的
 ,现将足量氯化银分别放入:①
,现将足量氯化银分别放入:①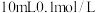 氯化镁溶液中,②
氯化镁溶液中,②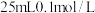 硝酸银溶液中,③
硝酸银溶液中,③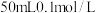 氯化铝溶液中,④
氯化铝溶液中,④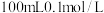 盐酸溶液中。充分搅拌后,相同温度下银离子浓度由大到小的顺序是
盐酸溶液中。充分搅拌后,相同温度下银离子浓度由大到小的顺序是(3)下表所示的是常温下,某些弱酸的电离常数,请根据要求作答。
| 弱酸 | 电离常数 | 弱酸 | 电离常数 |
 |  |  |  |
 | 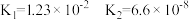 |  | 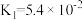 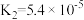 |
①相同物质的量浓度的
 和
和 的混合溶液中离子浓度由大到小的顺序为
的混合溶液中离子浓度由大到小的顺序为②请判断
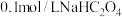 溶液显
溶液显③下列离子方程式书写正确的是
A. HC2O4-+SO32-═HSO3-+C2O42-
B. 2CH3COOH+SO32-═2CH3COO-+H2O+SO2↑
C. SO2+H2O+2CH3COO-═2CH3COOH+SO32-
D. 2CO32-+SO2+H2O═2HCO3-+SO32-
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】现有25℃时0.1mol•L-1的氨水,请回答以下问题:
(1)氨水呈碱性的原因为(用离子方程式表示)___ 。
(2)若向氨水中加入稀盐酸,使其恰好中和,写出反应的离子方程式___ ;若所得溶液的pH=5,则溶液中水所电离出的氢离子浓度为___ 。
(3)若向氨水中加入少量硫酸铵固体,此时溶液中
__ (填“增大”、“减小”或“不变”)。
(4)若向氨水中加入稀硫酸至溶液的pH=7,此时c(NH4+)=amol•L-1,则c(SO42-)=__ 。
(5)若向氨水中加入pH=1的硫酸,且氨水与硫酸的体积比为1∶1,则所得溶液中各离子的物质的量浓度由大到小的顺序是___ 。
(6)二氧化硫通入0.1mol/L的氯化钡溶液中至饱和,无现象,若继续加入氨水,产生白色沉淀,用电离平衡解释原因___ 。
(1)氨水呈碱性的原因为(用离子方程式表示)
(2)若向氨水中加入稀盐酸,使其恰好中和,写出反应的离子方程式
(3)若向氨水中加入少量硫酸铵固体,此时溶液中

(4)若向氨水中加入稀硫酸至溶液的pH=7,此时c(NH4+)=amol•L-1,则c(SO42-)=
(5)若向氨水中加入pH=1的硫酸,且氨水与硫酸的体积比为1∶1,则所得溶液中各离子的物质的量浓度由大到小的顺序是
(6)二氧化硫通入0.1mol/L的氯化钡溶液中至饱和,无现象,若继续加入氨水,产生白色沉淀,用电离平衡解释原因
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】铍铜是广泛应用于制造高级弹性元件的良好合金。某科研小组从某废旧铍铜元件(主要含BeO、CuS,还含少量FeS和SiO2)中回收铍和铜两种金属的工艺流程如下:
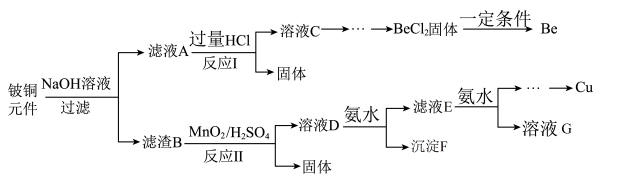
已知:i.铍、铝元素化学性质相似;BeCl2熔融时能微弱电离。
ii.常温下,Ksp[Cu(OH)2]=2.2×10-20,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Mn(OH)2]=2.1×10-13
常温下,若滤液D中c(Cu2+)=2.2mol·L-1、c(Fe3+)=0.008mol·L-1、c(Mn2+)=0.21mol·L-1,向其中逐滴加入稀氨水,生成沉淀F是___________ (填化学式);为了尽可能多的回收铜,所得滤液G的pH最大值为___________ 。

已知:i.铍、铝元素化学性质相似;BeCl2熔融时能微弱电离。
ii.常温下,Ksp[Cu(OH)2]=2.2×10-20,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Mn(OH)2]=2.1×10-13
常温下,若滤液D中c(Cu2+)=2.2mol·L-1、c(Fe3+)=0.008mol·L-1、c(Mn2+)=0.21mol·L-1,向其中逐滴加入稀氨水,生成沉淀F是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知难溶于水的盐在水中存在溶解平衡:
AgCl(s) Ag+(aq)+Cl-(aq)
Ag+(aq)+Cl-(aq)
在一定温度下,水溶液中Ag+的物质的量浓度和Cl-的物质的量浓度的乘积为一常数,可用 Ksp表示:Ksp=c(Ag+) c(Cl-)=1.8×10-10。
若把足量AgCl分别放入:
① 100 mL蒸馏水;
② 100 mL 0.1 mol/L NaCl溶液;
③ 100 mL 0.1 mol/L AlCl3溶液;
④ 100 mL 0.1 mol/L MgCl2溶液中;
搅拌后,在相同温度下Ag+浓度由大到小的顺序(用序号回答)是______ > ______ > ______ > ______ 。
AgCl(s)
 Ag+(aq)+Cl-(aq)
Ag+(aq)+Cl-(aq)在一定温度下,水溶液中Ag+的物质的量浓度和Cl-的物质的量浓度的乘积为一常数,可用 Ksp表示:Ksp=c(Ag+) c(Cl-)=1.8×10-10。
若把足量AgCl分别放入:
① 100 mL蒸馏水;
② 100 mL 0.1 mol/L NaCl溶液;
③ 100 mL 0.1 mol/L AlCl3溶液;
④ 100 mL 0.1 mol/L MgCl2溶液中;
搅拌后,在相同温度下Ag+浓度由大到小的顺序(用序号回答)是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】如图所示,横坐标为溶液的pH,纵坐标为Zn2+或[Zn(OH)4]2-(配离子)物质的量浓度的对数。
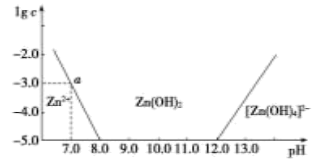
回答下列问题:
(1)向ZnCl2溶液中加入足量的氢氧化钠溶液,反应过程的离子方程式可表示为___________ 。
(2)由图中数据计算可得Zn(OH)2的溶度积(K)=___________ 。
(3)某废液中含Zn2+,为提取Zn2+,可以控制溶液中pH的范围是___________ 。
(4)向1L1.00mol/LZnCl2溶液中加入NaOH固体至pH=6.0,需NaOH___________ mol(精确到小数点后2位)。

回答下列问题:
(1)向ZnCl2溶液中加入足量的氢氧化钠溶液,反应过程的离子方程式可表示为
(2)由图中数据计算可得Zn(OH)2的溶度积(K)=
(3)某废液中含Zn2+,为提取Zn2+,可以控制溶液中pH的范围是
(4)向1L1.00mol/LZnCl2溶液中加入NaOH固体至pH=6.0,需NaOH
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】水溶液中存在着多种平衡,按要求回答下列问题。
(1)常温下,0.1 mol/L的一元弱酸HA,加水稀释过程中,溶液的pH将_______ (填“增大”、“减小”或“不变”,下同),HA的电离度_______ ,HA的电离平衡常数(K)将_______ 。
(2)常温下,向10 mL 0.2 mol/L的草酸(H2C2O4,二元弱酸)溶液中加入0.1 mol/L的NaOH溶液30 mL,则2c(OH-)+c( )- 2c(H+)=
)- 2c(H+)=_______ (用微粒的物质的量浓度符号表示)。若此时溶液的pH=4.5,则溶液中水的电离程度_______ (填“>”、“<”、“=”或“无法判断”)纯水的电离程度。
(3)已知常温下Fe(OH)3的Ksp=2.7×10-39,lg3=0.48。试计算0.1 mol/L的FeCl3溶液中,Fe3+开始生成沉淀时的pH=_______ 。
(1)常温下,0.1 mol/L的一元弱酸HA,加水稀释过程中,溶液的pH将
(2)常温下,向10 mL 0.2 mol/L的草酸(H2C2O4,二元弱酸)溶液中加入0.1 mol/L的NaOH溶液30 mL,则2c(OH-)+c(
 )- 2c(H+)=
)- 2c(H+)=(3)已知常温下Fe(OH)3的Ksp=2.7×10-39,lg3=0.48。试计算0.1 mol/L的FeCl3溶液中,Fe3+开始生成沉淀时的pH=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】运用化学反应原理知识回答下列有关碳和碳的化合物的问题
⑴汽车尾气的主要污染物是NO以及燃料燃烧不完全所产生的CO,它们是现代化城市的重要大气污染物,为了减轻汽车尾气造成的大气污染,人们开始探索利用NO和CO在一定条件下转化为两种无毒气体E和F的方法(已知该反应在一定条件下可以自发进行)。在2L密闭容器中加入一定量NO和CO,当温度分别在T1和T2时,测得各物质平衡时物质的量如下表:
①请结合上表数据,写出NO与CO反应的化学方程式___________________ ,该反应的△S_______ 0 (填“<”或“>”)。
②上述反应T1℃时的平衡常数为K1,T2℃时的平衡常数为K2。根据表中数据计算K1=_________ ,根据表中数据判断,温度T1和T2关系是(填序号)______________ 。
A. T1>T2B. T1<T2C.无法比较
(2)生成的CO2经常用氢氧化钠来吸收,现有0.4molCO2,若用200mL3mol/LNaOH溶液将其完全吸收,溶液中离子浓度由大到小的顺序为____________ 。
(3)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10-9。CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为2×10-4mol/L,则生成沉淀所需CaCl2溶液的最小浓度为:___________ mol/L。(忽略混合前后溶液体积的变化)
(4)已知14gCO完全燃烧时放出141.5 kJ 的热量,则写出CO燃烧热的热化学方程式:_____________ 。
(5)CO还可以用做燃料电池的燃料,某熔融盐燃料电池具有高的发电效率,因而受到重视,该电池用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混合气为正极助燃气,制得在650℃下工作的燃料电池,写出其负极和正极电极反应方程式:负极:_________ ;正极:________
⑴汽车尾气的主要污染物是NO以及燃料燃烧不完全所产生的CO,它们是现代化城市的重要大气污染物,为了减轻汽车尾气造成的大气污染,人们开始探索利用NO和CO在一定条件下转化为两种无毒气体E和F的方法(已知该反应在一定条件下可以自发进行)。在2L密闭容器中加入一定量NO和CO,当温度分别在T1和T2时,测得各物质平衡时物质的量如下表:
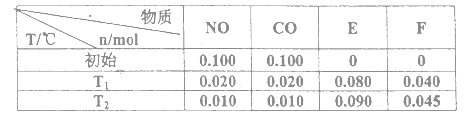
①请结合上表数据,写出NO与CO反应的化学方程式
②上述反应T1℃时的平衡常数为K1,T2℃时的平衡常数为K2。根据表中数据计算K1=
A. T1>T2B. T1<T2C.无法比较
(2)生成的CO2经常用氢氧化钠来吸收,现有0.4molCO2,若用200mL3mol/LNaOH溶液将其完全吸收,溶液中离子浓度由大到小的顺序为
(3)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10-9。CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为2×10-4mol/L,则生成沉淀所需CaCl2溶液的最小浓度为:
(4)已知14gCO完全燃烧时放出141.5 kJ 的热量,则写出CO燃烧热的热化学方程式:
(5)CO还可以用做燃料电池的燃料,某熔融盐燃料电池具有高的发电效率,因而受到重视,该电池用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混合气为正极助燃气,制得在650℃下工作的燃料电池,写出其负极和正极电极反应方程式:负极:
您最近一年使用:0次
【推荐3】物质在水溶液中可能存在电离平衡、盐的水解平衡或沉淀溶解平衡,它们都可看作化学平衡的一种,请根据所学化学知识回答下列问题:
(1)已知 溶液呈中性。常温下,浓度均为
溶液呈中性。常温下,浓度均为 的8种溶液:①
的8种溶液:① 溶液;②
溶液;② 溶液;③
溶液;③ 溶液:④
溶液:④ ;⑤
;⑤ 溶液;⑥
溶液;⑥ 溶液;⑦
溶液;⑦ 溶液:⑧
溶液:⑧ 溶液。这些溶液中水的电离程度由大到小的顺序是
溶液。这些溶液中水的电离程度由大到小的顺序是___________ (填序号)。
(2)25℃时,向 的氯化铵溶液中加入
的氯化铵溶液中加入 的氨水,判断铵离子的水解程度如何变化并说明理由:
的氨水,判断铵离子的水解程度如何变化并说明理由:___________ 。
(3)室温下,如果将
 和
和
 全部溶于水,形成混合溶液(假设无损失),两种粒子
全部溶于水,形成混合溶液(假设无损失),两种粒子___________ (填两种粒子的化学式)的物质的量之和比 多
多 。
。
(4)如图所示,横坐标为溶液的 ,纵坐标为
,纵坐标为 或
或 物质的量浓度的对数。回答下列问题:
物质的量浓度的对数。回答下列问题:
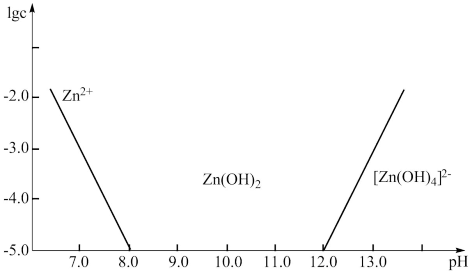
①向 溶液中加入足量的氢氧化钠溶液,写出该反应的化学方程式:
溶液中加入足量的氢氧化钠溶液,写出该反应的化学方程式:___________ 。
②从图中数据计算可得 的溶度积
的溶度积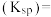
___________ 。
(5) 饱和溶液中存在:
饱和溶液中存在: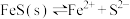 ,常温下
,常温下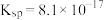 。
。
①理论上 的溶解度为
的溶解度为___________ g。
②又知 饱和溶液中
饱和溶液中 与
与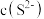 之间存在以下限量关系:
之间存在以下限量关系: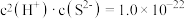 ,为了使溶液里
,为了使溶液里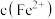 达到
达到 ,现将适量
,现将适量 投入其饱和溶液中,应调节溶液中的
投入其饱和溶液中,应调节溶液中的 为
为___________ 。
(1)已知
 溶液呈中性。常温下,浓度均为
溶液呈中性。常温下,浓度均为 的8种溶液:①
的8种溶液:① 溶液;②
溶液;② 溶液;③
溶液;③ 溶液:④
溶液:④ ;⑤
;⑤ 溶液;⑥
溶液;⑥ 溶液;⑦
溶液;⑦ 溶液:⑧
溶液:⑧ 溶液。这些溶液中水的电离程度由大到小的顺序是
溶液。这些溶液中水的电离程度由大到小的顺序是(2)25℃时,向
 的氯化铵溶液中加入
的氯化铵溶液中加入 的氨水,判断铵离子的水解程度如何变化并说明理由:
的氨水,判断铵离子的水解程度如何变化并说明理由:(3)室温下,如果将

 和
和
 全部溶于水,形成混合溶液(假设无损失),两种粒子
全部溶于水,形成混合溶液(假设无损失),两种粒子 多
多 。
。(4)如图所示,横坐标为溶液的
 ,纵坐标为
,纵坐标为 或
或 物质的量浓度的对数。回答下列问题:
物质的量浓度的对数。回答下列问题:
①向
 溶液中加入足量的氢氧化钠溶液,写出该反应的化学方程式:
溶液中加入足量的氢氧化钠溶液,写出该反应的化学方程式:②从图中数据计算可得
 的溶度积
的溶度积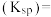
(5)
 饱和溶液中存在:
饱和溶液中存在: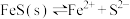 ,常温下
,常温下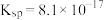 。
。①理论上
 的溶解度为
的溶解度为②又知
 饱和溶液中
饱和溶液中 与
与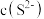 之间存在以下限量关系:
之间存在以下限量关系: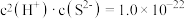 ,为了使溶液里
,为了使溶液里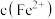 达到
达到 ,现将适量
,现将适量 投入其饱和溶液中,应调节溶液中的
投入其饱和溶液中,应调节溶液中的 为
为
您最近一年使用:0次



