水溶液中存在着多种平衡,按要求回答下列问题。
(1)常温下,0.1 mol/L的一元弱酸HA,加水稀释过程中,溶液的pH将_______ (填“增大”、“减小”或“不变”,下同),HA的电离度_______ ,HA的电离平衡常数(K)将_______ 。
(2)常温下,向10 mL 0.2 mol/L的草酸(H2C2O4,二元弱酸)溶液中加入0.1 mol/L的NaOH溶液30 mL,则2c(OH-)+c( )- 2c(H+)=
)- 2c(H+)=_______ (用微粒的物质的量浓度符号表示)。若此时溶液的pH=4.5,则溶液中水的电离程度_______ (填“>”、“<”、“=”或“无法判断”)纯水的电离程度。
(3)已知常温下Fe(OH)3的Ksp=2.7×10-39,lg3=0.48。试计算0.1 mol/L的FeCl3溶液中,Fe3+开始生成沉淀时的pH=_______ 。
(1)常温下,0.1 mol/L的一元弱酸HA,加水稀释过程中,溶液的pH将
(2)常温下,向10 mL 0.2 mol/L的草酸(H2C2O4,二元弱酸)溶液中加入0.1 mol/L的NaOH溶液30 mL,则2c(OH-)+c(
 )- 2c(H+)=
)- 2c(H+)=(3)已知常温下Fe(OH)3的Ksp=2.7×10-39,lg3=0.48。试计算0.1 mol/L的FeCl3溶液中,Fe3+开始生成沉淀时的pH=
22-23高二上·河北唐山·期末 查看更多[3]
更新时间:2023-02-14 22:20:11
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】溶液的酸碱性在生产生活和科学实验中有重要的作用。
(1)已知t℃时,水的离子积常数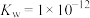 ,请回答下列问题:
,请回答下列问题:
①该温度下,在pH=9的 溶液中,由水电离出来的氢离子浓度为
溶液中,由水电离出来的氢离子浓度为___________ 。
②该温度下,将10ml pH=2的 溶液加水稀释到1000ml,则该溶液的pH为
溶液加水稀释到1000ml,则该溶液的pH为___________ 。
③该温度下,将100ml pH=a的HCl溶液与1ml pH=b的NaOH溶液混合,混合液呈中性,则a+b=___________ 。
(2)25℃,有浓度均为0.1 三种溶液:a.
三种溶液:a. ;b.HClO;c.
;b.HClO;c. 。(已知25℃时电离常数:
。(已知25℃时电离常数:
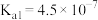 ,
,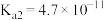 ;HClO
;HClO  ;
;
 )。
)。
① 的电离平衡常数表达式
的电离平衡常数表达式
___________ 。
②若把 、
、 、HClO、
、HClO、 都看作为酸,则其中酸性最强的是
都看作为酸,则其中酸性最强的是___________ (填化学式,下同),这四种酸对应的酸根离子中结合 能力最强的是
能力最强的是___________ 。
③足量的次氯酸与碳酸钠的反应离子方程式为___________ 。
(1)已知t℃时,水的离子积常数
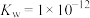 ,请回答下列问题:
,请回答下列问题:①该温度下,在pH=9的
 溶液中,由水电离出来的氢离子浓度为
溶液中,由水电离出来的氢离子浓度为②该温度下,将10ml pH=2的
 溶液加水稀释到1000ml,则该溶液的pH为
溶液加水稀释到1000ml,则该溶液的pH为③该温度下,将100ml pH=a的HCl溶液与1ml pH=b的NaOH溶液混合,混合液呈中性,则a+b=
(2)25℃,有浓度均为0.1
 三种溶液:a.
三种溶液:a. ;b.HClO;c.
;b.HClO;c. 。(已知25℃时电离常数:
。(已知25℃时电离常数:
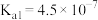 ,
,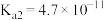 ;HClO
;HClO  ;
;
 )。
)。①
 的电离平衡常数表达式
的电离平衡常数表达式
②若把
 、
、 、HClO、
、HClO、 都看作为酸,则其中酸性最强的是
都看作为酸,则其中酸性最强的是 能力最强的是
能力最强的是③足量的次氯酸与碳酸钠的反应离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题
(1)写出 的价电子排布式
的价电子排布式______ 。
(2)实验室用软锰矿和浓盐酸制氯气,写出该反应的化学方程式______ 。
(3)在常温下, 溶液的pH=9,则溶液中由水电离出来的
溶液的pH=9,则溶液中由水电离出来的
______ 。
(4)火箭发射可以用肼( ,液态)作燃料,
,液态)作燃料, 作氧化剂,两者反应生成
作氧化剂,两者反应生成 和水蒸气。
和水蒸气。
已知:
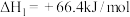 ;
;
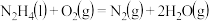
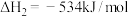
请写出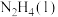 与
与 反应的热化学方程式
反应的热化学方程式______ 。
(5)下表列出了某短周期元素R的各级电离能数据(用 、
、 ……表示)。
……表示)。
关于元素R的下列推断中,正确的是______ (用相应的编号填写)
①R元素位于元素周期表中第ⅡA族
②R元素基态原子的电子排布式为
③R元素的最高价氧化物可表示为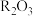
④R元素的第一电离能高于同周期相邻元素的第一电离能
(1)写出
 的价电子排布式
的价电子排布式(2)实验室用软锰矿和浓盐酸制氯气,写出该反应的化学方程式
(3)在常温下,
 溶液的pH=9,则溶液中由水电离出来的
溶液的pH=9,则溶液中由水电离出来的
(4)火箭发射可以用肼(
 ,液态)作燃料,
,液态)作燃料, 作氧化剂,两者反应生成
作氧化剂,两者反应生成 和水蒸气。
和水蒸气。已知:

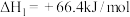 ;
;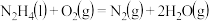
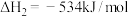
请写出
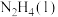 与
与 反应的热化学方程式
反应的热化学方程式(5)下表列出了某短周期元素R的各级电离能数据(用
 、
、 ……表示)。
……表示)。元素 | 电离能 | |||||
|
|
|
|
| … | |
| 740 | 1500 | 7700 | 10500 | 13630 | … |
①R元素位于元素周期表中第ⅡA族
②R元素基态原子的电子排布式为

③R元素的最高价氧化物可表示为
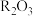
④R元素的第一电离能高于同周期相邻元素的第一电离能
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】下表是不同温度下水的离子积数据:
回答下列问题:
(1)若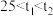 ,则a
,则a______ (填“>”“<”或“=”)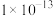 ,作此判断的理由是
,作此判断的理由是______ 。
(2)25℃时,某 溶液中
溶液中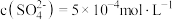 ,取该溶液1mL加水稀释至100mL,则稀释后溶液中
,取该溶液1mL加水稀释至100mL,则稀释后溶液中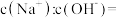
______ 。
(3)在 ℃下pH=10的NaOH溶液中,由水电离产生的
℃下pH=10的NaOH溶液中,由水电离产生的 浓度为
浓度为______ 。
(4) ℃下,将
℃下,将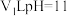 的苛性钠溶液与
的苛性钠溶液与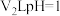 的稀硫酸混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,则
的稀硫酸混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,则
______ 。
(5)常温下, 的下列溶液中,水电离出的
的下列溶液中,水电离出的 由大到小的顺序是
由大到小的顺序是______ (填序号,下同),pH由大到小的顺序是______ 。
① ②
② ③
③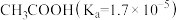 ④
④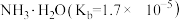 ⑤NaOH⑥
⑤NaOH⑥
温度/℃ | 25 |
|
|
水的离子积 |
| a |
|
(1)若
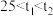 ,则a
,则a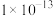 ,作此判断的理由是
,作此判断的理由是(2)25℃时,某
 溶液中
溶液中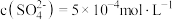 ,取该溶液1mL加水稀释至100mL,则稀释后溶液中
,取该溶液1mL加水稀释至100mL,则稀释后溶液中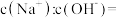
(3)在
 ℃下pH=10的NaOH溶液中,由水电离产生的
℃下pH=10的NaOH溶液中,由水电离产生的 浓度为
浓度为(4)
 ℃下,将
℃下,将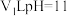 的苛性钠溶液与
的苛性钠溶液与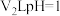 的稀硫酸混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,则
的稀硫酸混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,则
(5)常温下,
 的下列溶液中,水电离出的
的下列溶液中,水电离出的 由大到小的顺序是
由大到小的顺序是①
 ②
② ③
③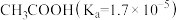 ④
④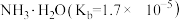 ⑤NaOH⑥
⑤NaOH⑥
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】25℃时,三种酸的电离平衡常数如下:
回答下列问题:
(1)一般情况下,当温度升高时,
___________ (填“增大”、“减小”或“不变”)。
(2)下列四种离子结合质子能力由大到小的顺序是___________ (填序号);
a. b.
b. c.
c. d.
d.
(3)次氯酸能否与碳酸钠溶液发生化学反应,若能,请写出相关离子方程式,若不能,请填写不能即可:___________ 。
(4)用蒸馏水稀释0.10mol/L的醋酸,下列各式表示的数值随水量的增加而增大的是___________ (填序号);
a.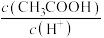 b.
b. c.
c. d.
d.
(5)25℃下, 反应的化学平衡常数为
反应的化学平衡常数为___________ 。
| 化学式 |  |  | HClO |
| 电离平衡常数 |  | 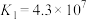 , , |  |
(1)一般情况下,当温度升高时,

(2)下列四种离子结合质子能力由大到小的顺序是
a.
 b.
b. c.
c. d.
d.
(3)次氯酸能否与碳酸钠溶液发生化学反应,若能,请写出相关离子方程式,若不能,请填写不能即可:
(4)用蒸馏水稀释0.10mol/L的醋酸,下列各式表示的数值随水量的增加而增大的是
a.
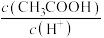 b.
b. c.
c. d.
d.
(5)25℃下,
 反应的化学平衡常数为
反应的化学平衡常数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】水溶液存在离子平衡,回答下列问题:
(1)水的电离平衡曲线如图所示。若以A点表示25°C时水在电离平衡时的离子浓度。当温度升到100°C时,水的电离平衡状态到B点,该温度时0.1mol/LNaOH溶液pH为___________ 。___________ (填“正”或“逆”)反应方向移动:水的电离程度将___________ (填“增大”、“减小”或“不变”)。
(3)常温下向20.00mL0.100mol/LHX(一元酸)溶液中滴加0.100mol/LNaOH的pH变化如图所示。___________ 。
②C点溶液中c(X-)___________ c(Na+)(填“>”、“<”或“=”)。
(1)水的电离平衡曲线如图所示。若以A点表示25°C时水在电离平衡时的离子浓度。当温度升到100°C时,水的电离平衡状态到B点,该温度时0.1mol/LNaOH溶液pH为
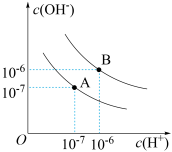
(3)常温下向20.00mL0.100mol/LHX(一元酸)溶液中滴加0.100mol/LNaOH的pH变化如图所示。

②C点溶液中c(X-)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题:
(1)向 醋酸溶液中加入少量水,
醋酸溶液中加入少量水,
_______ ,
_______ (填“增大”、“减小”或“不变”)。
(2) 醋酸溶液a、
醋酸溶液a、 盐酸溶液b分别与足量Zn粉充分反应,初始反应速率a
盐酸溶液b分别与足量Zn粉充分反应,初始反应速率a_______ b,溶液的导电能力a_______ b;最终产生氢气的质量a_______ b(填“<”、“>”或“=”)。
(3)已知 时部分弱电解质的电离平衡常数数据如表所示:
时部分弱电解质的电离平衡常数数据如表所示:
以下说法不正确的是_______。(填选项)
(1)向
 醋酸溶液中加入少量水,
醋酸溶液中加入少量水,

(2)
 醋酸溶液a、
醋酸溶液a、 盐酸溶液b分别与足量Zn粉充分反应,初始反应速率a
盐酸溶液b分别与足量Zn粉充分反应,初始反应速率a(3)已知
 时部分弱电解质的电离平衡常数数据如表所示:
时部分弱电解质的电离平衡常数数据如表所示:| 化学式 |  |  |  |
| 电离平衡常数 |  | 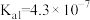  | 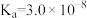 |
A.向弱酸溶液中加入少量 溶液,电离平衡常数变大 溶液,电离平衡常数变大 |
| B.多元弱酸的酸性主要由第一步电离决定 |
C.表中三种酸,酸性最强的是 |
D.向 溶液中通入 溶液中通入 气体,可以生成 气体,可以生成 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】室温时,向amL0.10mol/L的稀氨水中逐滴加入bmL0.10mol/L的稀盐酸,试分析:
(1)滴加过程中反应的离子方程式为:____ 。
(2)当b=a时,溶液呈___ 性(填“酸”“碱”或“中”),此时溶液中,c(NH )
)___ c(Cl-)(填“>”“<”或“=”)。
(3)当溶液呈中性时,a___ b(填“>”“<”或“=”),此时溶液中c(NH )
)___ c(Cl-)(填“>”“<”或“=”)。
(1)滴加过程中反应的离子方程式为:
(2)当b=a时,溶液呈
 )
)(3)当溶液呈中性时,a
 )
)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】室温下,在1L 0.1mol·L-1NH4Cl溶液中,
(1)水解的离子反应方程式________
(2)溶液中存在的微粒种类:H2O、________
(3)溶液中各种离子浓度从大到小的顺序为:________
(4)溶液中存在的电荷守恒等式________
(5)溶液中存在的物料守恒等式________
(1)水解的离子反应方程式
(2)溶液中存在的微粒种类:H2O、
(3)溶液中各种离子浓度从大到小的顺序为:
(4)溶液中存在的电荷守恒等式
(5)溶液中存在的物料守恒等式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】已知常温下部分弱电解质的电离平衡常数如表:
(1)常温下,物质的量浓度相同的三种溶液①NaF溶液、②NaClO溶液、③Na2CO3溶液,其pH由大到小的顺序是_______ (填序号)。
(2)NaClO溶液中的电荷守恒关系为_______ 。
(3)向NaClO溶液中通入少量的CO2,所发生反应的离子方程式为_______
(4)向Na2CO3溶液中加入明矾会产生沉淀和气体,请写出相关反应的离子方程式_______ 。
(5)TiCl4水解可制得二氧化钛水合物(TiO2·xH2O),再将其固体焙烧可制得二氧化钛,写出制得二氧化钛水合物的化学方程式_______ ,制备时加入大量的水并加热,其目的是_______ 。
(6)已知某溶液中存在OH-、H+、 、Cl-四种离子,某同学推测其离子浓度大小顺序有如下四种关系:
、Cl-四种离子,某同学推测其离子浓度大小顺序有如下四种关系:
A.c(Cl-)>c( )>c(H+)>c(OH-) B.c(Cl-)>c(
)>c(H+)>c(OH-) B.c(Cl-)>c( )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
C.c( )>c(Cl-)>c(OH-)>c(H+) D.c(Cl-)>c(H+)>c(
)>c(Cl-)>c(OH-)>c(H+) D.c(Cl-)>c(H+)>c( )>c(OH-)
)>c(OH-)
①若上述关系中C是正确的,则溶液中的溶质为_______ 。
②若该溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)_______ c(NH3·H2O)(填“大于”、“小于”或“等于”,下同),混合前酸中c(H+)和碱中c(OH-)的关系为c(H+)_______ c(OH-)。
| 化学式 | HF | HClO | H2CO3 | NH3·H2O |
| 电离 常数 | 6.8×10-4 | 4.7×10-8 | Ka1=4.3×10-7 Ka2=5.6×10-11 | 1.7×10-5 |
(2)NaClO溶液中的电荷守恒关系为
(3)向NaClO溶液中通入少量的CO2,所发生反应的离子方程式为
(4)向Na2CO3溶液中加入明矾会产生沉淀和气体,请写出相关反应的离子方程式
(5)TiCl4水解可制得二氧化钛水合物(TiO2·xH2O),再将其固体焙烧可制得二氧化钛,写出制得二氧化钛水合物的化学方程式
(6)已知某溶液中存在OH-、H+、
 、Cl-四种离子,某同学推测其离子浓度大小顺序有如下四种关系:
、Cl-四种离子,某同学推测其离子浓度大小顺序有如下四种关系:A.c(Cl-)>c(
 )>c(H+)>c(OH-) B.c(Cl-)>c(
)>c(H+)>c(OH-) B.c(Cl-)>c( )>c(OH-)>c(H+)
)>c(OH-)>c(H+) C.c(
 )>c(Cl-)>c(OH-)>c(H+) D.c(Cl-)>c(H+)>c(
)>c(Cl-)>c(OH-)>c(H+) D.c(Cl-)>c(H+)>c( )>c(OH-)
)>c(OH-)①若上述关系中C是正确的,则溶液中的溶质为
②若该溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】钼酸钠晶体(Na2MoO4·2H2O)是一种金属腐蚀抑制剂。如图是利用钼精矿(主要成分是MoS2,含少量PbS等)为原料生产钼酸钠晶体的工艺流程图。
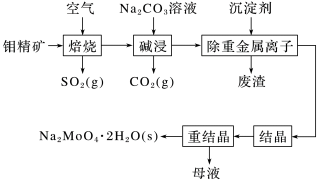
“结晶”前需向滤液中加入Ba(OH)2固体以除去 。若滤液中c(MoO
。若滤液中c(MoO )=0.40mol·L-1,c(
)=0.40mol·L-1,c( )=0.10mol/L,当BaMoO4开始沉淀时,
)=0.10mol/L,当BaMoO4开始沉淀时, 的去除率是
的去除率是___________ %[已知:Ksp(BaCO3)=1.0×10-9,Ksp(BaMoO4)=4.0×10-8,溶液体积变化忽略不计]。

“结晶”前需向滤液中加入Ba(OH)2固体以除去
 。若滤液中c(MoO
。若滤液中c(MoO )=0.40mol·L-1,c(
)=0.40mol·L-1,c( )=0.10mol/L,当BaMoO4开始沉淀时,
)=0.10mol/L,当BaMoO4开始沉淀时, 的去除率是
的去除率是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】人体内尿酸(HUr)含量偏高,关节滑液中产生尿酸钠晶体(NaUr)会引发痛风和关节炎,有关平衡有:①HUr(尿酸,aq) (尿酸根,aq)
(尿酸根,aq) 、
、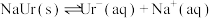 ②。某课题组配制“模拟关节滑液”进行研究,回答下列问题:
②。某课题组配制“模拟关节滑液”进行研究,回答下列问题:
已知:①37℃时, ,
, ,
,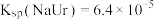 。
。
②37℃时,模拟关节滑液pH=7.4, 。
。
(1)37℃时, HUr溶液的pH约为
HUr溶液的pH约为_______ (已知 )。
)。
(2)下列事实可以证明尿酸是弱电解质的是_______(填字母)。
(3)37℃时,向HUr溶液中加入NaOH溶液配制“模拟关节滑液”,溶液中
_______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(4)37℃时,向模拟关节滑液中加入NaCl(s)至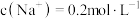 时,通过计算判断是否有NaUr晶体析出,请写出判断过程:
时,通过计算判断是否有NaUr晶体析出,请写出判断过程:_______ 。
(5)关节炎发作大都在脚趾和手指的关节处,反应②是_______ (填“放热”或“吸热”)反应。
(6)对于尿酸偏高的人群,下列建议正确的是_______(填字母)。
 (尿酸根,aq)
(尿酸根,aq) 、
、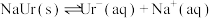 ②。某课题组配制“模拟关节滑液”进行研究,回答下列问题:
②。某课题组配制“模拟关节滑液”进行研究,回答下列问题:已知:①37℃时,
 ,
, ,
,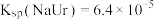 。
。②37℃时,模拟关节滑液pH=7.4,
 。
。(1)37℃时,
 HUr溶液的pH约为
HUr溶液的pH约为 )。
)。(2)下列事实可以证明尿酸是弱电解质的是_______(填字母)。
| A.NaUr溶液显碱性 |
| B.HUr溶液可使石蕊溶液变红 |
| C.常温下,等浓度的尿酸溶液导电性比盐酸弱 |
D.10mL 溶液与10mL 溶液与10mL NaOH溶液完全反应 NaOH溶液完全反应 |

 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(4)37℃时,向模拟关节滑液中加入NaCl(s)至
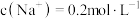 时,通过计算判断是否有NaUr晶体析出,请写出判断过程:
时,通过计算判断是否有NaUr晶体析出,请写出判断过程:(5)关节炎发作大都在脚趾和手指的关节处,反应②是
(6)对于尿酸偏高的人群,下列建议正确的是_______(填字母)。
| A.多喝水,食用新鲜蔬果 |
| B.饮食宜多盐、多脂 |
| C.适度运动,注意关节保暖 |
| D.减少摄入易代谢出尿酸的食物 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】酸、碱、盐的水溶液在生产生活及化学实验中有广泛的应用,请同学们运用所学知识解决下列问题。已知25℃时部分弱电解质的电离常数如下表:
(1)浓度相同的①NaCN② ③
③ 三种溶液,其pH由大到小的顺序为
三种溶液,其pH由大到小的顺序为___________ (填序号)。
(2)在室温下, 醋酸钠溶液的pH约为
醋酸钠溶液的pH约为___________ 。
(3)已知次磷酸 是一种一元弱酸,向10mL
是一种一元弱酸,向10mL 溶液中加入10mL等物质的量浓度的NaOH溶液后,所得溶液中的阴离子有:
溶液中加入10mL等物质的量浓度的NaOH溶液后,所得溶液中的阴离子有:___________ ;常温下, 的
的 溶液在加水稀释过程中,下列表达式的数据一定变小的是
溶液在加水稀释过程中,下列表达式的数据一定变小的是___________ (填序号)。
A. B.
B. C.
C. D.
D.
(4)请写出往 溶液中滴加过量HCN溶液反应的离子方程式:
溶液中滴加过量HCN溶液反应的离子方程式:___________ 。
(5)25℃时,氨水与 的混合溶液
的混合溶液 ,该溶液中
,该溶液中
___________ 。
(6)分析化学中,以 标准溶液滴定溶液中的
标准溶液滴定溶液中的 时,采用
时,采用 作指示剂,利用
作指示剂,利用 与
与 反应生成砖红色沉淀指示滴定终点。当溶液中的
反应生成砖红色沉淀指示滴定终点。当溶液中的 恰好沉淀完全(浓度等于
恰好沉淀完全(浓度等于 )时,溶液中
)时,溶液中
___________  。(结果保留两位有效数字,已知
。(结果保留两位有效数字,已知 ,
,
 )
)
| 物质 | HCN |  |  |  |  |
| 电离常数 | 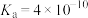 |  |  |  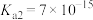 |  |
 ③
③ 三种溶液,其pH由大到小的顺序为
三种溶液,其pH由大到小的顺序为(2)在室温下,
 醋酸钠溶液的pH约为
醋酸钠溶液的pH约为(3)已知次磷酸
 是一种一元弱酸,向10mL
是一种一元弱酸,向10mL 溶液中加入10mL等物质的量浓度的NaOH溶液后,所得溶液中的阴离子有:
溶液中加入10mL等物质的量浓度的NaOH溶液后,所得溶液中的阴离子有: 的
的 溶液在加水稀释过程中,下列表达式的数据一定变小的是
溶液在加水稀释过程中,下列表达式的数据一定变小的是A.
 B.
B. C.
C. D.
D.
(4)请写出往
 溶液中滴加过量HCN溶液反应的离子方程式:
溶液中滴加过量HCN溶液反应的离子方程式:(5)25℃时,氨水与
 的混合溶液
的混合溶液 ,该溶液中
,该溶液中
(6)分析化学中,以
 标准溶液滴定溶液中的
标准溶液滴定溶液中的 时,采用
时,采用 作指示剂,利用
作指示剂,利用 与
与 反应生成砖红色沉淀指示滴定终点。当溶液中的
反应生成砖红色沉淀指示滴定终点。当溶液中的 恰好沉淀完全(浓度等于
恰好沉淀完全(浓度等于 )时,溶液中
)时,溶液中
 。(结果保留两位有效数字,已知
。(结果保留两位有效数字,已知 ,
,
 )
)
您最近一年使用:0次











