如图所示,横坐标为溶液的pH,纵坐标为Zn2+或[Zn(OH)4]2-(配离子)物质的量浓度的对数。
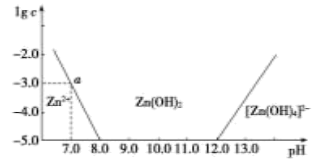
回答下列问题:
(1)向ZnCl2溶液中加入足量的氢氧化钠溶液,反应过程的离子方程式可表示为___________ 。
(2)由图中数据计算可得Zn(OH)2的溶度积(K)=___________ 。
(3)某废液中含Zn2+,为提取Zn2+,可以控制溶液中pH的范围是___________ 。
(4)向1L1.00mol/LZnCl2溶液中加入NaOH固体至pH=6.0,需NaOH___________ mol(精确到小数点后2位)。

回答下列问题:
(1)向ZnCl2溶液中加入足量的氢氧化钠溶液,反应过程的离子方程式可表示为
(2)由图中数据计算可得Zn(OH)2的溶度积(K)=
(3)某废液中含Zn2+,为提取Zn2+,可以控制溶液中pH的范围是
(4)向1L1.00mol/LZnCl2溶液中加入NaOH固体至pH=6.0,需NaOH
24-25高二上·全国·假期作业 查看更多[1]
(已下线)BBWYhjhx1107.pdf
更新时间:2023-12-11 22:01:52
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】已知:常温下Ksp[Fe(OH)3]=8.0×10-38,Ksp[Al(OH)3]=1.3×10-33,当Fe3+完全沉淀时,溶液中Al3+理论最大浓度为___________
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】工业上用重晶石(BaSO4)制备BaCO3的常用方法主要有高温煅烧还原法、沉淀转化法等。高温煅烧还原法的工艺流程可简单的表示如下:
已知:BaSO4(s)+4C(s)=BaS(s)+4CO(g)△H = +571.2 kJ•mol-1
Ba(s)+S(s)+2O2(g):BaSO4(s)△H = -1473.2 kJ•mol-1
Ba(s)+S(s)=BaS(g)△H = -460 kJ•mol-1
请回答:
(1)工业上煅烧重晶石矿粉时,为使BaSO4得到充分还原和维持反应所需的高温,应采取的措施是_________________________________ 。
(2)沉淀转化法制备BaCO3可用饱和Na2CO3溶液将BaSO4转化为BaCO3:
BaSO4(s)+CO2-3(aq)=BaCO3(s)+SO2-4(aq)
则:在实验室中将少量BaSO4沉淀全部转化为BaCO3的实验操作方法与步骤为
________________________________________________________________________________________________________________________________________________
(3)与高温煅烧还原法相比,用饱和Na2CO3溶液沉淀转化法的优点主要有
________________________________________________________________________________________________________________________________________________
已知:BaSO4(s)+4C(s)=BaS(s)+4CO(g)△H = +571.2 kJ•mol-1
Ba(s)+S(s)+2O2(g):BaSO4(s)△H = -1473.2 kJ•mol-1
Ba(s)+S(s)=BaS(g)△H = -460 kJ•mol-1
请回答:
(1)工业上煅烧重晶石矿粉时,为使BaSO4得到充分还原和维持反应所需的高温,应采取的措施是
(2)沉淀转化法制备BaCO3可用饱和Na2CO3溶液将BaSO4转化为BaCO3:
BaSO4(s)+CO2-3(aq)=BaCO3(s)+SO2-4(aq)
则:在实验室中将少量BaSO4沉淀全部转化为BaCO3的实验操作方法与步骤为
(3)与高温煅烧还原法相比,用饱和Na2CO3溶液沉淀转化法的优点主要有
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】反应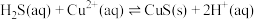 的平衡常数为
的平衡常数为___________ 。[已知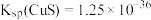 ;
; 的
的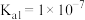 ,
,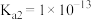 ]
]
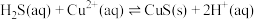 的平衡常数为
的平衡常数为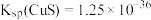 ;
; 的
的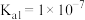 ,
,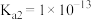 ]
]
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】请按要求回答下列问题:
(1) 时,物质的量浓度均为
时,物质的量浓度均为 的几种盐溶液的
的几种盐溶液的 如下表所示。
如下表所示。
①溶液Ⅰ显酸性的原因是_______ (用离子方程式表示)。
②溶液Ⅱ中,
_______ (填“>”“<”或“=”) 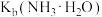 。
。
③写出溶液Ⅲ中阴离子浓度由大到小的关系:_______ 。
(2)几种离子开始沉淀时的 如下表所示。
如下表所示。
①当向含相同浓度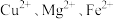 的溶液中滴加氢氧化钠溶液时,
的溶液中滴加氢氧化钠溶液时,_______ (填离子符号)最先沉淀。
② 时,要使
时,要使 硫酸铜溶液中铜离子浓度降至原来的千分之一,则应向溶液里加入氢氧化钠溶液,使溶液
硫酸铜溶液中铜离子浓度降至原来的千分之一,则应向溶液里加入氢氧化钠溶液,使溶液 为
为_______ 。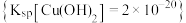
(3)已知: 时,
时, 的电离常数
的电离常数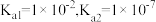 ,则该温度下
,则该温度下 的水解平衡常数
的水解平衡常数
_______ ,若向 溶液中加入少量的
溶液中加入少量的 ,则溶液中
,则溶液中 将
将_______ (填“增大”“减小”或“不变”)。
(4)已知常温下 和
和 的
的 分别为
分别为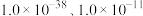 ,浓度均为
,浓度均为 的
的 、
、 的混合溶液中.要使
的混合溶液中.要使 完全沉淀(离子浓度小于
完全沉淀(离子浓度小于 )而
)而 不沉淀,应该调节溶液
不沉淀,应该调节溶液 的范围是
的范围是_______ ,调节 应选用的试剂是
应选用的试剂是_______ .(填化学式)。
(1)
 时,物质的量浓度均为
时,物质的量浓度均为 的几种盐溶液的
的几种盐溶液的 如下表所示。
如下表所示。| 序号 | Ⅰ | Ⅱ | Ⅲ |
| 溶液 |  溶液 溶液 |  溶液 溶液 |  溶液 溶液 |
 | 5 | 7 | 8.4 |
②溶液Ⅱ中,

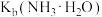 。
。③写出溶液Ⅲ中阴离子浓度由大到小的关系:
(2)几种离子开始沉淀时的
 如下表所示。
如下表所示。| 离子 |  |  |  |
 | 7.6 | 5.2 | 10.4 |
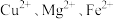 的溶液中滴加氢氧化钠溶液时,
的溶液中滴加氢氧化钠溶液时,②
 时,要使
时,要使 硫酸铜溶液中铜离子浓度降至原来的千分之一,则应向溶液里加入氢氧化钠溶液,使溶液
硫酸铜溶液中铜离子浓度降至原来的千分之一,则应向溶液里加入氢氧化钠溶液,使溶液 为
为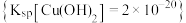
(3)已知:
 时,
时, 的电离常数
的电离常数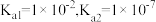 ,则该温度下
,则该温度下 的水解平衡常数
的水解平衡常数
 溶液中加入少量的
溶液中加入少量的 ,则溶液中
,则溶液中 将
将(4)已知常温下
 和
和 的
的 分别为
分别为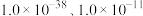 ,浓度均为
,浓度均为 的
的 、
、 的混合溶液中.要使
的混合溶液中.要使 完全沉淀(离子浓度小于
完全沉淀(离子浓度小于 )而
)而 不沉淀,应该调节溶液
不沉淀,应该调节溶液 的范围是
的范围是 应选用的试剂是
应选用的试剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
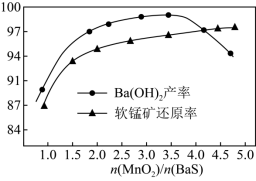
【推荐3】MnO2是一种两性氧化物,用软锰矿(主要成分为MnO2,含少量铁的氧化物)和BaS可制备高纯MnCO3。
(1)保持BaS投料量不变,随MnO2与BaS投料比增大,软锰矿还原率和氢氧化钡的产率的变化如图所示。当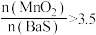 ,Ba(OH)2产率减小的原因是
,Ba(OH)2产率减小的原因是___________ 。
(2)充分反应后过滤,滤液经过______ 可获得Ba(OH)2·8H2O晶体。
(3)反应后的滤渣中还含有S和未反应的MnO2,以此滤渣为原料制备高纯度的MnCO3的流程如图。

①酸溶还原时,MnO2发生反应的离子方程式_______ 。
②MnSO4溶液和NH4HCO3溶液混合后,反应生成MnCO3,反应的离子方程式为________ 。实际制取MnCO3时,一般选择使用氨水—NH4HCO3混合溶液代替NH4HCO3溶液,这样改进的优点是______ 。
③以上制备是在常温下进行,此时 、
、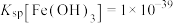 。工业上,当某离子浓度小于1×10-6mol·L-1时,认为该离子已除净,氧化后所得溶液中,
。工业上,当某离子浓度小于1×10-6mol·L-1时,认为该离子已除净,氧化后所得溶液中,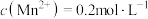 为使溶液中Fe3+除净,调节pH的范围应为
为使溶液中Fe3+除净,调节pH的范围应为___________ 。
(1)保持BaS投料量不变,随MnO2与BaS投料比增大,软锰矿还原率和氢氧化钡的产率的变化如图所示。当
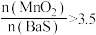 ,Ba(OH)2产率减小的原因是
,Ba(OH)2产率减小的原因是
(2)充分反应后过滤,滤液经过
(3)反应后的滤渣中还含有S和未反应的MnO2,以此滤渣为原料制备高纯度的MnCO3的流程如图。

①酸溶还原时,MnO2发生反应的离子方程式
②MnSO4溶液和NH4HCO3溶液混合后,反应生成MnCO3,反应的离子方程式为
③以上制备是在常温下进行,此时
 、
、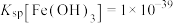 。工业上,当某离子浓度小于1×10-6mol·L-1时,认为该离子已除净,氧化后所得溶液中,
。工业上,当某离子浓度小于1×10-6mol·L-1时,认为该离子已除净,氧化后所得溶液中,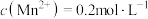 为使溶液中Fe3+除净,调节pH的范围应为
为使溶液中Fe3+除净,调节pH的范围应为
您最近一年使用:0次



