铍铜是广泛应用于制造高级弹性元件的良好合金。某科研小组从某废旧铍铜元件(主要含BeO、CuS,还含少量FeS和SiO2)中回收铍和铜两种金属的工艺流程如下:
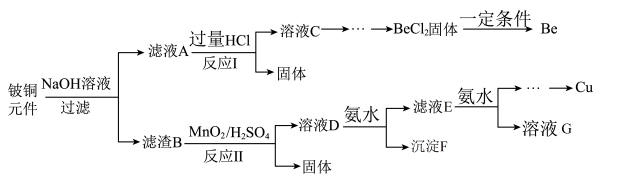
已知:i.铍、铝元素化学性质相似;BeCl2熔融时能微弱电离。
ii.常温下,Ksp[Cu(OH)2]=2.2×10-20,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Mn(OH)2]=2.1×10-13
常温下,若滤液D中c(Cu2+)=2.2mol·L-1、c(Fe3+)=0.008mol·L-1、c(Mn2+)=0.21mol·L-1,向其中逐滴加入稀氨水,生成沉淀F是___________ (填化学式);为了尽可能多的回收铜,所得滤液G的pH最大值为___________ 。

已知:i.铍、铝元素化学性质相似;BeCl2熔融时能微弱电离。
ii.常温下,Ksp[Cu(OH)2]=2.2×10-20,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Mn(OH)2]=2.1×10-13
常温下,若滤液D中c(Cu2+)=2.2mol·L-1、c(Fe3+)=0.008mol·L-1、c(Mn2+)=0.21mol·L-1,向其中逐滴加入稀氨水,生成沉淀F是
2023高三·全国·专题练习 查看更多[2]
(已下线)06 常考题空6 工艺流程中Ksp的相关计算 (解析)-备战2023年高考化学大题逐空突破系列(全国通用)(已下线)题型二 工艺流程中Ksp的相关计算-备战2024年高考化学答题技巧与模板构建
更新时间:2023-04-13 17:57:44
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】常温下,某浓度的NH4Cl溶液的pH为4,回答下列问题:
(1)该NH4Cl溶液中含氮元素的微粒有___________ 。
(2)该NH4Cl溶液中c水(H+)与pH=4盐酸中c水(H+)比值为___________ 。
(1)该NH4Cl溶液中含氮元素的微粒有
(2)该NH4Cl溶液中c水(H+)与pH=4盐酸中c水(H+)比值为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】物质在水中可能存在电离平衡、水解平衡和沉淀溶解平衡,请根据所学知识回答:
(1)某温度下,纯水中的c(H+)=1.5×10-7,则纯水中的
_______ mol/L,该温度时的水的离子积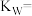
_______ 。保持温度不变,滴入稀盐酸使溶液中的 ,则溶液中的
,则溶液中的 为
为_______  。
。
(2)常温中,一定浓度的CH3COONa溶液的pH=8,已知CH3COOH的电离平衡常数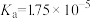 ,则该CH3COONa溶液中:
,则该CH3COONa溶液中: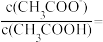
_______ 。
(3)甲酸钠(HCOONa)溶液呈碱性的原因是_______ (用离子方程式表示)。0.02mol/L的HCOONa溶液中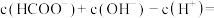
_______ mol/L。
(4)25℃,在0.10mol•L1硫酸铜溶液中加入氢氧化钠稀溶液充分反应,有蓝色氢氧化铜沉淀生成,当溶液的pH=9时,c(Cu2+)=_______ molL1(Ksp[Cu(OH)2]=2.2×1020)。
(1)某温度下,纯水中的c(H+)=1.5×10-7,则纯水中的

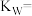
 ,则溶液中的
,则溶液中的 为
为 。
。(2)常温中,一定浓度的CH3COONa溶液的pH=8,已知CH3COOH的电离平衡常数
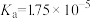 ,则该CH3COONa溶液中:
,则该CH3COONa溶液中: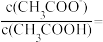
(3)甲酸钠(HCOONa)溶液呈碱性的原因是
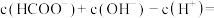
(4)25℃,在0.10mol•L1硫酸铜溶液中加入氢氧化钠稀溶液充分反应,有蓝色氢氧化铜沉淀生成,当溶液的pH=9时,c(Cu2+)=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】乙酰水杨酸(用HA表示)商品名为阿司匹林,具有解热镇痛的作用,可以由水杨酸(用H2B表示)合成。
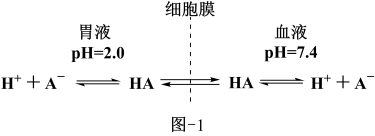
(1)阿司匹林的效率主要取决于其被血液吸收的程度。阿司匹林分子可以自由穿过细胞膜而离子不能,膜两侧HA的平衡浓度相等,示意图如图-1所示。
①胃液中的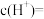
_______  。
。
②细胞膜两侧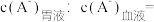
_______ 。
(2)室温下,水杨酸水溶液中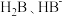 和
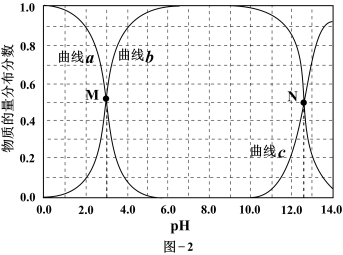
和 的物质的量分布分数随pH变化的曲线如图-2所示。
的物质的量分布分数随pH变化的曲线如图-2所示。
①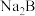 水解的离子方程式为
水解的离子方程式为_______ 。
②曲线c代表的微粒是_______ ;M点横坐标为3.0,则水杨酸的Ka1=_______ 。
③已知图中N点横坐标为12.7。当溶液pH=8.0时,溶液中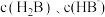 和
和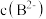 由大到小的顺序为
由大到小的顺序为_______ 。
(1)阿司匹林的效率主要取决于其被血液吸收的程度。阿司匹林分子可以自由穿过细胞膜而离子不能,膜两侧HA的平衡浓度相等,示意图如图-1所示。

①胃液中的
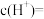
 。
。②细胞膜两侧
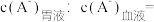
(2)室温下,水杨酸水溶液中
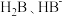 和
和 的物质的量分布分数随pH变化的曲线如图-2所示。
的物质的量分布分数随pH变化的曲线如图-2所示。
①
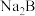 水解的离子方程式为
水解的离子方程式为②曲线c代表的微粒是
③已知图中N点横坐标为12.7。当溶液pH=8.0时,溶液中
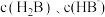 和
和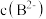 由大到小的顺序为
由大到小的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】盐酸、硫酸和醋酸是生产、生活和化学实验中常用的酸,请回答:
(1)人的胃液中含有盐酸,经测定某人胃液的pH=2,则其中的c(H+)=______ mol/L。
(2)食醋常用于食品调味,其主要成分为醋酸,已知醋酸酸性强于碳酸,写出碳酸钠溶液与足量醋酸反应的离子方程式:______ 。
(3)室温下,物质的量浓度相同、体积相同的盐酸(编号a)、硫酸(编号b)和醋酸(编号c),中和氢氧化钠的能力由大到小的顺序是______ 。(用相应编号表示);
(4)有pH均为3的盐酸、硫酸和醋酸,取同体积分别加蒸馏水稀释到pH=5,需水的体积依次为V1、V2、V3,则其关系是______ 。
(5)能证明醋酸是弱酸的实验事实是______ 。
a.室温时0.1mo/LCH3COONa溶液的pH大于7
b.可用食醋清除水壶内壁的水垢
c.与相同浓度的碳酸氢钠溶液反应,醋酸不如盐酸剧烈
d.将1mL pH=1的醋酸溶液稀释到100mL后,测其pH小于3
(6)向100mL0.1mo/L的盐酸中通入0.02mol氨气,充分吸收后测得溶液呈碱性。则该溶液中NH3·H2O、NH4+、Cl—三种微粒的物质的量浓度大小关系为______ 。
(1)人的胃液中含有盐酸,经测定某人胃液的pH=2,则其中的c(H+)=
(2)食醋常用于食品调味,其主要成分为醋酸,已知醋酸酸性强于碳酸,写出碳酸钠溶液与足量醋酸反应的离子方程式:
(3)室温下,物质的量浓度相同、体积相同的盐酸(编号a)、硫酸(编号b)和醋酸(编号c),中和氢氧化钠的能力由大到小的顺序是
(4)有pH均为3的盐酸、硫酸和醋酸,取同体积分别加蒸馏水稀释到pH=5,需水的体积依次为V1、V2、V3,则其关系是
(5)能证明醋酸是弱酸的实验事实是
a.室温时0.1mo/LCH3COONa溶液的pH大于7
b.可用食醋清除水壶内壁的水垢
c.与相同浓度的碳酸氢钠溶液反应,醋酸不如盐酸剧烈
d.将1mL pH=1的醋酸溶液稀释到100mL后,测其pH小于3
(6)向100mL0.1mo/L的盐酸中通入0.02mol氨气,充分吸收后测得溶液呈碱性。则该溶液中NH3·H2O、NH4+、Cl—三种微粒的物质的量浓度大小关系为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】请根据所学知识回答下列问题:
(1)同温同压下, ,在光照和点燃条件下的
,在光照和点燃条件下的 (化学计量数相同)分别为
(化学计量数相同)分别为 、
、 ,
,
___________  (填“>”“<”或“=”)
(填“>”“<”或“=”)
(2)已知常温时红磷比白磷稳定,比较下列反应中 的大小:
的大小:
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
① (白磷,s)
(白磷,s)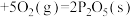

② (红磷,s)
(红磷,s)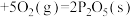

(3)已知:稀溶液中,
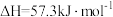 ,则浓硫酸与稀氢氧化钠溶液反应生成
,则浓硫酸与稀氢氧化钠溶液反应生成 水,放出的热量
水,放出的热量___________ 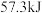 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(4)已知: 与
与 水蒸气在
水蒸气在 、
、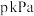 时,完全反应生成
时,完全反应生成 和
和 的混合气体,吸收了
的混合气体,吸收了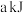 热量,该反应的热化学方程式
热量,该反应的热化学方程式___________ 。
(5)已知室温时, 的某一元酸
的某一元酸 在水中有
在水中有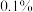 发生电离,回答下列各问题:
发生电离,回答下列各问题:
①该溶液的
___________ 。
② 的电离平衡常数
的电离平衡常数
___________ 。
③升高温度时, 将
将___________ (填“增大”、“减小”或“不变”),
(1)同温同压下,
 ,在光照和点燃条件下的
,在光照和点燃条件下的 (化学计量数相同)分别为
(化学计量数相同)分别为 、
、 ,
,
 (填“>”“<”或“=”)
(填“>”“<”或“=”)(2)已知常温时红磷比白磷稳定,比较下列反应中
 的大小:
的大小:
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。①
 (白磷,s)
(白磷,s)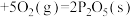

②
 (红磷,s)
(红磷,s)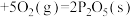

(3)已知:稀溶液中,

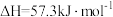 ,则浓硫酸与稀氢氧化钠溶液反应生成
,则浓硫酸与稀氢氧化钠溶液反应生成 水,放出的热量
水,放出的热量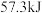 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(4)已知:
 与
与 水蒸气在
水蒸气在 、
、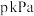 时,完全反应生成
时,完全反应生成 和
和 的混合气体,吸收了
的混合气体,吸收了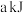 热量,该反应的热化学方程式
热量,该反应的热化学方程式(5)已知室温时,
 的某一元酸
的某一元酸 在水中有
在水中有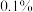 发生电离,回答下列各问题:
发生电离,回答下列各问题:①该溶液的

②
 的电离平衡常数
的电离平衡常数
③升高温度时,
 将
将
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】钡(Ba)和锶(Sr)及其化合物在工业上有着广泛的应用,它们在地壳中常以硫酸盐的形式存在,BaSO4和SrSO4都是难溶性盐。工业上提取钡和锶时首先将BaSO4和SrSO4转化成难溶弱酸盐。
已知:SrSO4(s)⇌Sr2+(aq)+SO (aq) Ksp=2.5×10-7
(aq) Ksp=2.5×10-7
SrCO3(s)⇌Sr2+(aq)+CO (aq) Ksp=2.5×10-9
(aq) Ksp=2.5×10-9
(1)将SrSO4转化成SrCO3的离子方程式为________ ;该反应的平衡常数表达式为_____ ;该反应能发生的原因是________ (用沉淀溶解平衡的有关理论解释)。
(2)对于上述反应,实验证明增大CO 的浓度或降低温度都有利于提高SrSO4的转化率。判断在下列两种情况下,平衡常数K的变化情况(填“增大”“减小”或“不变”)。
的浓度或降低温度都有利于提高SrSO4的转化率。判断在下列两种情况下,平衡常数K的变化情况(填“增大”“减小”或“不变”)。
①升高温度,平衡常数K将________ 。
②增大CO 的浓度,平衡常数K将
的浓度,平衡常数K将___________ 。
已知:SrSO4(s)⇌Sr2+(aq)+SO
 (aq) Ksp=2.5×10-7
(aq) Ksp=2.5×10-7SrCO3(s)⇌Sr2+(aq)+CO
 (aq) Ksp=2.5×10-9
(aq) Ksp=2.5×10-9(1)将SrSO4转化成SrCO3的离子方程式为
(2)对于上述反应,实验证明增大CO
 的浓度或降低温度都有利于提高SrSO4的转化率。判断在下列两种情况下,平衡常数K的变化情况(填“增大”“减小”或“不变”)。
的浓度或降低温度都有利于提高SrSO4的转化率。判断在下列两种情况下,平衡常数K的变化情况(填“增大”“减小”或“不变”)。①升高温度,平衡常数K将
②增大CO
 的浓度,平衡常数K将
的浓度,平衡常数K将
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】化合物A俗称石灰氮,以前是一种常用的肥料,其含氮量可高达 35.0%,钙含量为50%。它可以用CaCO3通过下列步骤方便地制出:

(1)已知固态二元化合物D中钙含量为62.5%,则D的化学式为___ 。
(2)请推算出A的化学式。_____ 。
(3)分别写出上述过程中生成D和A的化学方程式。______ ;_____ 。
(4)将A放入水中,会重新生成CaCO3并放出刺激性气味的气体,请写出发生反应的化学方程式。_____ 。
(5)已知CaCO3与CaSO4的溶度积分别为2.8×10-9、9.1×10-6。由此可知二者的溶解度的大小关系为CaCO3___ CaSO4。在锅炉除垢操作中,要先用碳酸钠溶液将水垢中的硫酸钙转化成为碳酸钙。其主要原因是____ 。

(1)已知固态二元化合物D中钙含量为62.5%,则D的化学式为
(2)请推算出A的化学式。
(3)分别写出上述过程中生成D和A的化学方程式。
(4)将A放入水中,会重新生成CaCO3并放出刺激性气味的气体,请写出发生反应的化学方程式。
(5)已知CaCO3与CaSO4的溶度积分别为2.8×10-9、9.1×10-6。由此可知二者的溶解度的大小关系为CaCO3
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法有还原沉淀法,该法的工艺流程为:
CrO42- Cr2O72-
Cr2O72- 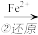 Cr3+(紫色)
Cr3+(紫色) Cr(OH)3(蓝色)
Cr(OH)3(蓝色)
其中第①步存在平衡:2CrO42-(黄色)+2H+ Cr2O72-(橙色)+H2O
Cr2O72-(橙色)+H2O
(1)若平衡体系的pH=2,则溶液显______________ 色。
(2)第②步中,还原0.1mol Cr2O72-离子,需要________ g的FeSO4。
(3)Cr3+与Al3+的化学性质相似,在Cr2(SO4)3溶液中逐滴加入NaOH溶液直至过量,可观察到的现象是_______________________ 。
第③步生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:
Cr(OH)3(s) Cr3+(aq)+3OH-(aq)
Cr3+(aq)+3OH-(aq)
(4)常温下,Cr(OH)3的溶度积Ksp=c(Cr3+)·c3(OH-)=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至________________________________ 。
(5)已知AgCl、Ag2CrO4(砖红色)的Ksp分别为2×10-10和1.12×10-12。分析化学中,测定含氯的中性溶液中Cl-的含量,以K2CrO4作指示剂,用AgNO3溶液滴定。滴定过程中首先析出沉淀________________________________ 。
CrO42-
 Cr2O72-
Cr2O72- 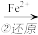 Cr3+(紫色)
Cr3+(紫色) Cr(OH)3(蓝色)
Cr(OH)3(蓝色)其中第①步存在平衡:2CrO42-(黄色)+2H+
 Cr2O72-(橙色)+H2O
Cr2O72-(橙色)+H2O(1)若平衡体系的pH=2,则溶液显
(2)第②步中,还原0.1mol Cr2O72-离子,需要
(3)Cr3+与Al3+的化学性质相似,在Cr2(SO4)3溶液中逐滴加入NaOH溶液直至过量,可观察到的现象是
第③步生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:
Cr(OH)3(s)
 Cr3+(aq)+3OH-(aq)
Cr3+(aq)+3OH-(aq)(4)常温下,Cr(OH)3的溶度积Ksp=c(Cr3+)·c3(OH-)=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至
(5)已知AgCl、Ag2CrO4(砖红色)的Ksp分别为2×10-10和1.12×10-12。分析化学中,测定含氯的中性溶液中Cl-的含量,以K2CrO4作指示剂,用AgNO3溶液滴定。滴定过程中首先析出沉淀
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】碱性锌锰电池是日常生活中消耗最大的电池,其构造如图所示。
放电时总反应为:Zn+2H2O+2MnO2=Zn(OH)2+2MnOOH
从废旧碱性锌锰电池中回收Zn和MnO2的工艺如下:
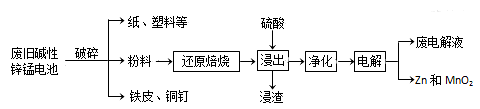
回答下列问题:
(1)MnOOH中,Mn元素的化合价为_______ 。
(2)“还原焙烧”过程中,高价金属化合物被还原为低价氧化物或金属单质(其中MnOOH、MnO2被还成MnO),主要原因是“粉料”中含有________ 。
<span style="font-size: 14px; font-family: " 宋体";"=""><span contenteditable="true">(3)</span></span>“净化”为了除去浸出液中的Fe2+,方法是:加入_______ (填化学式)溶液将Fe2+氧化为Fe3+,再调节pH使Fe3+完全沉淀。已知浸出液中Mi2+、Zn2+的浓度约为0. 1mol •L-1,根据下列数据计算,调节pH的合理范围是_____ 至_______ 。
(离子浓度小于1×mol • L-1即为沉淀完全)
(4)“电解”时,阳极的电极反应式为_______ 。本工艺中应循环利用的物质是________ (填化学式)。
<span style="font-size: 14px; font-family: "宋体";"><span contenteditable="true">(5)</span></span>若将“粉料”直接与盐酸共热反应后过滤,滤液的主要成分是ZnCl2和MnCl2。“粉料”中的MnOOH与盐酸反应的化学方程式为_____________ 。
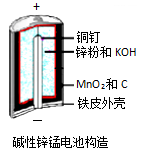
放电时总反应为:Zn+2H2O+2MnO2=Zn(OH)2+2MnOOH
从废旧碱性锌锰电池中回收Zn和MnO2的工艺如下:

回答下列问题:
(1)MnOOH中,Mn元素的化合价为
(2)“还原焙烧”过程中,高价金属化合物被还原为低价氧化物或金属单质(其中MnOOH、MnO2被还成MnO),主要原因是“粉料”中含有
<span style="font-size: 14px; font-family: " 宋体";"=""><span contenteditable="true">(3)</span></span>“净化”为了除去浸出液中的Fe2+,方法是:加入
| 化合物 | Mn(OH)3 | Zn(OH)2 | Fe(OH)3 |
| Ksp近似值 | 10-13 | 10-17 | 10-38 |
(离子浓度小于1×mol • L-1即为沉淀完全)
(4)“电解”时,阳极的电极反应式为
<span style="font-size: 14px; font-family: "宋体";"><span contenteditable="true">(5)</span></span>若将“粉料”直接与盐酸共热反应后过滤,滤液的主要成分是ZnCl2和MnCl2。“粉料”中的MnOOH与盐酸反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】电解质水溶液中存在电离平衡,水解平衡、沉淀溶解平衡。请回答下列问题:
(1)常温下,部分弱酸的电离平衡常数如表:
①等浓度CH3COONa、NaClO、 Na2CO3和NaHCO3溶液中,碱性最强的是_______ 。
②等浓度的CH3COONa与NaClO混合溶液中离子浓度由大到小的顺序为_______
(2)室温下,用0.10mol•L−1盐酸溶液滴定20mL 0.1mol•L−1氨水溶液,滴定曲线如图所示。

①该中和滴定选用_______ (填“甲基橙”或“酚酞”)作指示剂。
②室温下,0.10mol•L−1氨水溶液中NH3•H2O的电离平衡常数约为_______ mol·L−1
③b点所示的溶液中c(NH )+c(NH3•H2O)=
)+c(NH3•H2O)=_______ (用溶液的其它离子浓度表示)。
(3)工业上向锅炉里注入所得到的Na2CO3溶液浸泡,将水垢中的CaSO4转化为CaCO3,而后用醋酸除去。当把水垢中CaSO4完全转化时,混合溶液中的c(CO )=1.0×10−3mol·L−1,则c(SO
)=1.0×10−3mol·L−1,则c(SO )=
)=_______ 。Ksp(CaSO4)=9.1×10−6 Ksp(CaCO3)=3.4×10−9(保留小数点后一位)
(1)常温下,部分弱酸的电离平衡常数如表:
| 弱酸 | CH3COOH | HClO | H2CO3 |
| 电离平衡常数 | Ka=1.8×10-5 | Ka=3.1×10-8 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
②等浓度的CH3COONa与NaClO混合溶液中离子浓度由大到小的顺序为
(2)室温下,用0.10mol•L−1盐酸溶液滴定20mL 0.1mol•L−1氨水溶液,滴定曲线如图所示。

①该中和滴定选用
②室温下,0.10mol•L−1氨水溶液中NH3•H2O的电离平衡常数约为
③b点所示的溶液中c(NH
 )+c(NH3•H2O)=
)+c(NH3•H2O)=(3)工业上向锅炉里注入所得到的Na2CO3溶液浸泡,将水垢中的CaSO4转化为CaCO3,而后用醋酸除去。当把水垢中CaSO4完全转化时,混合溶液中的c(CO
 )=1.0×10−3mol·L−1,则c(SO
)=1.0×10−3mol·L−1,则c(SO )=
)=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】已知常温下,Ksp(PbSO4)=1.1×10-8,Ksp(PbCO3)=3.3×10-14,Ksp(PbS)=3.4×10-28。
(1)写出PbSO4溶解平衡的离子方程式______ 。
(2)常温下,溶解度:PbSO4_____ (填“>”“<”或“=”)PbCO3。
(3)从PbSO4固体中回收铅,关键步骤是制备硝酸铅。简单叙述由PbSO4制备Pb(NO3)2的操作原理______ 。
(4)处理废水中的Pb2+宜选择的试剂是______ (填字母)。
A.Na2SO4 B.Na2CO3 C.Na2S
(5)向浓度相等的Na2SO4和Na2CO3溶液中滴加Pb(NO3)2溶液,同时产生两种沉淀时,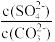 =
=____ 。
(1)写出PbSO4溶解平衡的离子方程式
(2)常温下,溶解度:PbSO4
(3)从PbSO4固体中回收铅,关键步骤是制备硝酸铅。简单叙述由PbSO4制备Pb(NO3)2的操作原理
(4)处理废水中的Pb2+宜选择的试剂是
A.Na2SO4 B.Na2CO3 C.Na2S
(5)向浓度相等的Na2SO4和Na2CO3溶液中滴加Pb(NO3)2溶液,同时产生两种沉淀时,
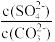 =
=
您最近一年使用:0次

 的盐酸溶液中,由水电离产生的
的盐酸溶液中,由水电离产生的 是
是 。
。 的醋酸钠溶液中,由水电离产生的
的醋酸钠溶液中,由水电离产生的 。
。 和
和 浓度的乘积为
浓度的乘积为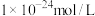 ,该溶液的
,该溶液的 可能为
可能为

