已知难溶于水的盐在水中存在溶解平衡:
AgCl(s) Ag+(aq)+Cl-(aq)
Ag+(aq)+Cl-(aq)
在一定温度下,水溶液中Ag+的物质的量浓度和Cl-的物质的量浓度的乘积为一常数,可用 Ksp表示:Ksp=c(Ag+) c(Cl-)=1.8×10-10。
若把足量AgCl分别放入:
① 100 mL蒸馏水;
② 100 mL 0.1 mol/L NaCl溶液;
③ 100 mL 0.1 mol/L AlCl3溶液;
④ 100 mL 0.1 mol/L MgCl2溶液中;
搅拌后,在相同温度下Ag+浓度由大到小的顺序(用序号回答)是______ > ______ > ______ > ______ 。
AgCl(s)
 Ag+(aq)+Cl-(aq)
Ag+(aq)+Cl-(aq)在一定温度下,水溶液中Ag+的物质的量浓度和Cl-的物质的量浓度的乘积为一常数,可用 Ksp表示:Ksp=c(Ag+) c(Cl-)=1.8×10-10。
若把足量AgCl分别放入:
① 100 mL蒸馏水;
② 100 mL 0.1 mol/L NaCl溶液;
③ 100 mL 0.1 mol/L AlCl3溶液;
④ 100 mL 0.1 mol/L MgCl2溶液中;
搅拌后,在相同温度下Ag+浓度由大到小的顺序(用序号回答)是
11-12高二上·广东揭阳·阶段练习 查看更多[1]
(已下线)2011-2012学年广东省普宁二中高二11月月考化学试卷
更新时间:2011-12-12 18:23:51
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】氢氰酸( )有剧毒,易挥发。金矿提金时,用
)有剧毒,易挥发。金矿提金时,用 溶液浸取金生成
溶液浸取金生成 ,再用锌置换出金,产生的含氰废水需处理后排放。
,再用锌置换出金,产生的含氰废水需处理后排放。
(1)① 存在着两步电离平衡,其第一步电离方程式为
存在着两步电离平衡,其第一步电离方程式为___________ 。
② 可用于制备
可用于制备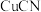 ,
,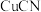 浊液中加入
浊液中加入 溶液可发生反应:
溶液可发生反应:
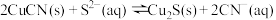 ,该反应的平衡常数
,该反应的平衡常数
___________ 。
[已知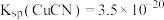 ,
,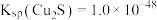 ]。
]。
(2) 可催化
可催化 氧化废水中的
氧化废水中的 。其他条件相同时,总氯化物(
。其他条件相同时,总氯化物( 、
、 等)去除率随溶液初始
等)去除率随溶液初始 变化如图所示。
变化如图所示。

①在酸性条件下, 也能氧化
也能氧化 ,但实际处理废水时却不在酸性条件下进行的原因是
,但实际处理废水时却不在酸性条件下进行的原因是___________ 。
②当溶液初始 时,总氰化物去除率下降的原因可能是
时,总氰化物去除率下降的原因可能是___________ 。
(3)通过电激发产生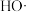 和
和 处理废水中的
处理废水中的 ,可能的反应机理如图所示。虚线方框内的过程可描述为
,可能的反应机理如图所示。虚线方框内的过程可描述为___________ 。

 )有剧毒,易挥发。金矿提金时,用
)有剧毒,易挥发。金矿提金时,用 溶液浸取金生成
溶液浸取金生成 ,再用锌置换出金,产生的含氰废水需处理后排放。
,再用锌置换出金,产生的含氰废水需处理后排放。(1)①
 存在着两步电离平衡,其第一步电离方程式为
存在着两步电离平衡,其第一步电离方程式为②
 可用于制备
可用于制备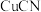 ,
,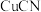 浊液中加入
浊液中加入 溶液可发生反应:
溶液可发生反应: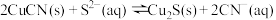 ,该反应的平衡常数
,该反应的平衡常数
[已知
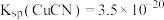 ,
,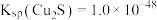 ]。
]。(2)
 可催化
可催化 氧化废水中的
氧化废水中的 。其他条件相同时,总氯化物(
。其他条件相同时,总氯化物( 、
、 等)去除率随溶液初始
等)去除率随溶液初始 变化如图所示。
变化如图所示。
①在酸性条件下,
 也能氧化
也能氧化 ,但实际处理废水时却不在酸性条件下进行的原因是
,但实际处理废水时却不在酸性条件下进行的原因是②当溶液初始
 时,总氰化物去除率下降的原因可能是
时,总氰化物去除率下降的原因可能是(3)通过电激发产生
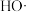 和
和 处理废水中的
处理废水中的 ,可能的反应机理如图所示。虚线方框内的过程可描述为
,可能的反应机理如图所示。虚线方框内的过程可描述为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】金属氢氧化物在酸中溶解度不同,因此可以利用这一性质,控制溶液的pH,达到分离金属离子的目的。难溶性金属氢氧化物在不同pH下的溶解度[S(mol·L-1)]如图所示。

(1)pH=6时溶液中铜元素的主要存在形式是________ 。
(2)若要除去CuCl2溶液中的少量Fe3+,下列最适宜的pH 范围是_____ (选填序号)。
A.<2 B. 3.5〜4.2 C. >6.3
(3)在Ni(OH)2溶液中含有少量的Co2+杂质,_______ (填“能”或“不能”)通过调节溶液pH的方法来除去,理由是______ .
(4)可用加入氨水的方法使Cu(OH)2沉淀溶解,生成的产物之一为[Cu(NH3)4]2+。该反应的离子方程式为______ .
已知一些难溶物的溶度积常数如下表:
(5)某工业废水中含有Cu2+、Pb2+、Hg2+,为除去这些离子,最适宜向此工业废水中加入过量的______ (选填序号)。
A.NaOH B.FeS C.Na2S

(1)pH=6时溶液中铜元素的主要存在形式是
(2)若要除去CuCl2溶液中的少量Fe3+,下列最适宜的pH 范围是
A.<2 B. 3.5〜4.2 C. >6.3
(3)在Ni(OH)2溶液中含有少量的Co2+杂质,
(4)可用加入氨水的方法使Cu(OH)2沉淀溶解,生成的产物之一为[Cu(NH3)4]2+。该反应的离子方程式为
已知一些难溶物的溶度积常数如下表:
| 物质 | FeS | MnS | CuS | PbS | HgS | ZnS |
| Ksp | 6.3×10-18 | 2.5×10-13 | 1.3×10-36 | 3.4×10-28 | 6.4×10-53 | 1.6×10-24 |
(5)某工业废水中含有Cu2+、Pb2+、Hg2+,为除去这些离子,最适宜向此工业废水中加入过量的
A.NaOH B.FeS C.Na2S
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】沉淀溶解平衡的应用
(1)沉淀的生成
(2)沉淀的溶解
如要使Mg(OH)2沉淀溶解,可加入_______________ .
(3)沉淀的转化
锅炉除垢,将CaSO4转化为CaCO3的离子方程式为_______________ ;
ZnS沉淀中滴加CuSO4溶液得到CuS沉淀的离子方程式为_______________ .
(1)沉淀的生成
方法 | 举例 | 解释 |
| 调节pH法 | 除去CuCl2溶液中的FeCl3,可向溶液中加入 | |
| 调节pH法 | 除去NH4Cl溶液中的FeCl3杂质,可加入 | |
| 沉淀剂法 | 以 |
(2)沉淀的溶解
如要使Mg(OH)2沉淀溶解,可加入
(3)沉淀的转化
锅炉除垢,将CaSO4转化为CaCO3的离子方程式为
ZnS沉淀中滴加CuSO4溶液得到CuS沉淀的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】沉淀溶解平衡在生产、科研和环保等领域有着许多应用。
(1)除去硫酸铜溶液中混有的少量铁离子,可向溶液中加入Cu(OH)2,调节溶液的PH,铁离子就会全部转化为Fe(OH)3沉淀除去。
已知:常温下Fe(OH)3的溶度积Ksp=8.0×10-38,Cu(OH)2的溶度积Ksp=3.0×10-20,通常认为残留在溶液中的离子浓度小等于1×10-5 mol•L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0mol•L-1,通过计算确定应调节溶液的pH范围是______ 。(已知lg5=0.7)
(2)为了研究沉淀溶解平衡和沉淀转化,某同学查阅资料并设计如下实验。
资料:AgSCN是白色沉淀,相同温度下,溶解度AgSCN>AgI
①写出步骤2中溶液变为红色的离子方程式:____________________ 。
②步骤3中现象a是____________________________ 。
③用化学平衡原理解释步骤4中的实验现象:_________________________________ 。
(1)除去硫酸铜溶液中混有的少量铁离子,可向溶液中加入Cu(OH)2,调节溶液的PH,铁离子就会全部转化为Fe(OH)3沉淀除去。
已知:常温下Fe(OH)3的溶度积Ksp=8.0×10-38,Cu(OH)2的溶度积Ksp=3.0×10-20,通常认为残留在溶液中的离子浓度小等于1×10-5 mol•L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0mol•L-1,通过计算确定应调节溶液的pH范围是
(2)为了研究沉淀溶解平衡和沉淀转化,某同学查阅资料并设计如下实验。
资料:AgSCN是白色沉淀,相同温度下,溶解度AgSCN>AgI
| 操作步骤 | 现象 |
| 步骤1:向2 mL 0.005 mol·L-1 AgNO3溶液中加入2 mL 0.005 mol·L-1 KSCN溶液,静置 | 出现白色沉淀 |
| 步骤2:取1 mL上层清液于试管中,滴加1滴2 mol·L-1 Fe(NO3)3溶液 | 溶液变为红色 |
| 步骤3:向步骤2的溶液中继续加入5滴3 mol·L-1 AgNO3溶液 | 现象a,溶液红色变浅 |
| 步骤4:向步骤1余下的浊液中加入5滴3 mol·L-1 KI溶液 | 出现黄色沉淀 |
①写出步骤2中溶液变为红色的离子方程式:
②步骤3中现象a是
③用化学平衡原理解释步骤4中的实验现象:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】研究化学反应意义重大,请就下列现象和实质回答问题。
(1) 可用作白色颜料和阻燃剂等。在实验室中可利用
可用作白色颜料和阻燃剂等。在实验室中可利用 的水解反应制取
的水解反应制取 (
( 的水解分三步进行,中间产物有
的水解分三步进行,中间产物有 等),写出
等),写出 水解生成
水解生成 的水解反应方程式
的水解反应方程式______ 。
(2)次磷酸( )是一种弱酸,
)是一种弱酸, 溶液和足量
溶液和足量 溶液混合,所得溶液中阴离子只有
溶液混合,所得溶液中阴离子只有 、
、 两种。写出
两种。写出 溶液与
溶液与 溶液恰好完全中和的溶液中各离子浓度由大到小的顺序为
溶液恰好完全中和的溶液中各离子浓度由大到小的顺序为_______ 。
(3)已知 与
与 溶液反应生成
溶液反应生成 ,与稀硫酸反应生成
,与稀硫酸反应生成 ,写出
,写出 在水中的两种电离方程式
在水中的两种电离方程式_______ 、_______ 。
(4)一定温度下,用水吸收 气体时,溶液中水的电离平衡
气体时,溶液中水的电离平衡_______ 移动(填“向左”“向右”或“不”);若得到 的
的 溶液,试计算溶液中
溶液,试计算溶液中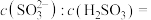
_______ (已知该温度下, 的电离常数:
的电离常数: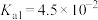 ,
, )。
)。
(5)某温度下, 的盐酸中
的盐酸中 ;该温度下
;该温度下 的
的 溶液与
溶液与 的
的 溶液混合后溶液的
溶液混合后溶液的 ,则
,则 与
与 溶液的体积比为
溶液的体积比为_______ 。
(6) 时,若向
时,若向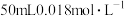 的
的 溶液中加入
溶液中加入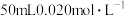 的盐酸,混合后溶液中的
的盐酸,混合后溶液中的 为
为______  (
( 时,
时, )。
)。
(1)
 可用作白色颜料和阻燃剂等。在实验室中可利用
可用作白色颜料和阻燃剂等。在实验室中可利用 的水解反应制取
的水解反应制取 (
( 的水解分三步进行,中间产物有
的水解分三步进行,中间产物有 等),写出
等),写出 水解生成
水解生成 的水解反应方程式
的水解反应方程式(2)次磷酸(
 )是一种弱酸,
)是一种弱酸, 溶液和足量
溶液和足量 溶液混合,所得溶液中阴离子只有
溶液混合,所得溶液中阴离子只有 、
、 两种。写出
两种。写出 溶液与
溶液与 溶液恰好完全中和的溶液中各离子浓度由大到小的顺序为
溶液恰好完全中和的溶液中各离子浓度由大到小的顺序为(3)已知
 与
与 溶液反应生成
溶液反应生成 ,与稀硫酸反应生成
,与稀硫酸反应生成 ,写出
,写出 在水中的两种电离方程式
在水中的两种电离方程式(4)一定温度下,用水吸收
 气体时,溶液中水的电离平衡
气体时,溶液中水的电离平衡 的
的 溶液,试计算溶液中
溶液,试计算溶液中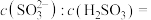
 的电离常数:
的电离常数: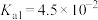 ,
, )。
)。(5)某温度下,
 的盐酸中
的盐酸中 ;该温度下
;该温度下 的
的 溶液与
溶液与 的
的 溶液混合后溶液的
溶液混合后溶液的 ,则
,则 与
与 溶液的体积比为
溶液的体积比为(6)
 时,若向
时,若向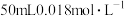 的
的 溶液中加入
溶液中加入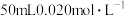 的盐酸,混合后溶液中的
的盐酸,混合后溶液中的 为
为 (
( 时,
时, )。
)。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题:
(1)有一种溶液,除含H+、OH- 外,还含有Na+、SO42- 和Cl-,测得Na+、SO42- 和Cl-三种离子的浓度分别是0.01 mol·L-1、0.0035 mol·L-1和0.004 mol·L-1,该溶液的pH为____________ 。
(2)NH4Cl溶液显酸性,试用离子方程式表示这一原理________________________ 。
(3)液氨的电离类似于水,试写出液氨的电离方程式______________________ ;在液氨中加入NH4Cl,平衡将向_________ 移动。
(4)氯化银在水中存在沉淀溶解平衡: AgCl(s)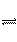 Ag+(aq)+Cl-(aq), 在25℃时,氯化银的Ksp=1.8×10-10。现将足量氯化银分别放入:①100 mL 0.1 mol·L-1氯化镁溶液中;②100 mL蒸馏水中;③100 mL 0.1 mol·L-1氯化铝溶液中;④100 mL 0.1 mol·L-1盐酸溶液中。充分搅拌后,相同温度下银离子浓度由大到小的顺序是
Ag+(aq)+Cl-(aq), 在25℃时,氯化银的Ksp=1.8×10-10。现将足量氯化银分别放入:①100 mL 0.1 mol·L-1氯化镁溶液中;②100 mL蒸馏水中;③100 mL 0.1 mol·L-1氯化铝溶液中;④100 mL 0.1 mol·L-1盐酸溶液中。充分搅拌后,相同温度下银离子浓度由大到小的顺序是____________ (填写序号)。
(1)有一种溶液,除含H+、OH- 外,还含有Na+、SO42- 和Cl-,测得Na+、SO42- 和Cl-三种离子的浓度分别是0.01 mol·L-1、0.0035 mol·L-1和0.004 mol·L-1,该溶液的pH为
(2)NH4Cl溶液显酸性,试用离子方程式表示这一原理
(3)液氨的电离类似于水,试写出液氨的电离方程式
(4)氯化银在水中存在沉淀溶解平衡: AgCl(s)
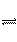 Ag+(aq)+Cl-(aq), 在25℃时,氯化银的Ksp=1.8×10-10。现将足量氯化银分别放入:①100 mL 0.1 mol·L-1氯化镁溶液中;②100 mL蒸馏水中;③100 mL 0.1 mol·L-1氯化铝溶液中;④100 mL 0.1 mol·L-1盐酸溶液中。充分搅拌后,相同温度下银离子浓度由大到小的顺序是
Ag+(aq)+Cl-(aq), 在25℃时,氯化银的Ksp=1.8×10-10。现将足量氯化银分别放入:①100 mL 0.1 mol·L-1氯化镁溶液中;②100 mL蒸馏水中;③100 mL 0.1 mol·L-1氯化铝溶液中;④100 mL 0.1 mol·L-1盐酸溶液中。充分搅拌后,相同温度下银离子浓度由大到小的顺序是
您最近一年使用:0次



