1. 电极活性物质Cu
4O(PO
4)
2的制备,可通过下列反应制备:2Na
3PO
4+4CuSO
4+2NH
3·H
2O = Cu
4O(PO
4)
2↓+3Na
2SO
4+(NH
4)
2SO
4+H
2O。
(1)上述反应涉及的元素中不属于元素周期表p区元素的是
___________,写出基态Cu
2+的电子排布式
___________。
(2)P、S元素第一电离能大小关系为P
___________S(填“>”、“<”或“=”),原因是
_____________。
(3)O的原子核外有
_____种不同能量的电子,其氢化物沸点高于同族元素H
2S的原因是
_______。
(4)CuSO
4溶液中逐滴加入氨水,先产生蓝色沉淀,后又溶解得到深蓝色溶液[Cu(NH
3)
4]SO
4,加入乙醇后有深蓝色沉淀析出,关于该深蓝色物质的说法错误的是
________。
A.该物质正离子的中心是Cu原子
B.该配合物的配体数等于配位数
C.外界离子的中心原子的杂化方式为sp
3 D.乙醇的作用是将配合物转化为Cu(OH)
2写出沉淀溶解生成深蓝色溶液的离子方程式
________。
(5)在硫酸铜溶液中加入过量KCN,生成配合物[Cu(CN)
4]
2-,则1 mol该配合物含有π键的数目为
___________(N
A表示阿伏加德罗常数的值)。
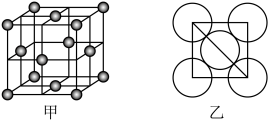
(6)晶体铜的晶胞结构如图甲所示,原子之间相对位置关系的平面图如图乙所示,铜原子的配位数为
______,已知铜原子半径为127.8 pm,N
A=6.02×10
23 mol
-1,计算晶体铜的密度
________ g·cm
-3(结果保留3位有效数字)。