T℃时, 和
和 的沉淀溶解平衡曲线如图所示。已知:
的沉淀溶解平衡曲线如图所示。已知: ,
, 或
或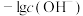 。下列说法正确的是
。下列说法正确的是

 和
和 的沉淀溶解平衡曲线如图所示。已知:
的沉淀溶解平衡曲线如图所示。已知: ,
, 或
或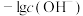 。下列说法正确的是
。下列说法正确的是
A.T℃时, |
B.Y点对应的 溶液是不饱和溶液 溶液是不饱和溶液 |
C.Z点对应的溶液中,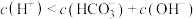 |
D.向 悬浊液中通入 悬浊液中通入 气体(忽略溶液体积的变化),溶液中 气体(忽略溶液体积的变化),溶液中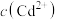 保持不变 保持不变 |
更新时间:2024-02-21 18:07:37
|
相似题推荐
多选题
|
较难
(0.4)
名校
【推荐1】常温下,下列有关溶液的叙述正确的是
A.在0.1 mol·L-1Na2C2O4溶液中: |
B.在Na2SO3溶液中: |
| C.pH=6的醋酸溶液和pH=6的NH4Cl溶液,由水电离出的c(H+)均为1×10-8 mol·L-1 |
D.浓度均为0.1 mol·L-1的硫酸氢铵溶液与氢氧化钠溶液等体积混合: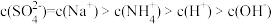 |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
解题方法
【推荐2】常温下,向10mL一定浓度的硝酸银溶液中,逐滴加入0.1mol·L-1的氨水,反应过程中-1gc(Ag+)或-1gc[Ag(NH3) ]与加入氨水体积的关系如图。下列说法错误的是
]与加入氨水体积的关系如图。下列说法错误的是
 ]与加入氨水体积的关系如图。下列说法错误的是
]与加入氨水体积的关系如图。下列说法错误的是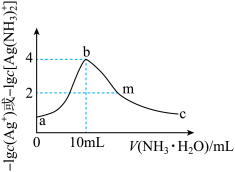
| A.原硝酸银溶液的浓度是0.1mol·L-1 |
| B.反应生成氢氧化银的Ksp(AgOH)的数量级为10-8 |
C.溶液b点NH4+的浓度小于溶液c点 的浓度 的浓度 |
D.溶液m点c( )>c(Ag+)+c[Ag(NH3) )>c(Ag+)+c[Ag(NH3) ]+c( ]+c( ) ) |
您最近一年使用:0次
多选题
|
较难
(0.4)
【推荐1】常温下,向含 、
、 、
、 的溶液中缓慢滴加
的溶液中缓慢滴加 稀溶液,溶液中
稀溶液,溶液中 [
[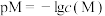 ,
,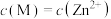 、
、 、
、 ]与
]与 [
[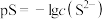 ]的关系如图所示。已知:常温下,
]的关系如图所示。已知:常温下,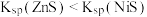 。下列叙述正确的是
。下列叙述正确的是
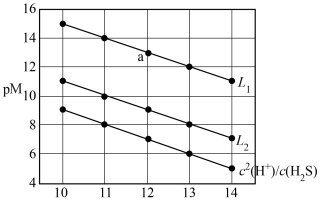
 、
、 、
、 的溶液中缓慢滴加
的溶液中缓慢滴加 稀溶液,溶液中
稀溶液,溶液中 [
[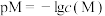 ,
,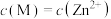 、
、 、
、 ]与
]与 [
[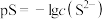 ]的关系如图所示。已知:常温下,
]的关系如图所示。已知:常温下,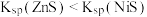 。下列叙述正确的是
。下列叙述正确的是
A. 直线代表 直线代表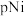 和 和 的关系 的关系 |
B.室温下, |
C.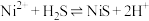 的平衡常数 的平衡常数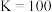 |
D.向a点溶液中滴加 浓溶液,a点沿 浓溶液,a点沿 向右移动 向右移动 |
您最近一年使用:0次
多选题
|
较难
(0.4)
解题方法
【推荐2】已知[Co(H2O)6]2+呈粉红色,[CoCl4]2-呈蓝色,[ZnCl4]2-为无色。现将CoCl2溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡: 。用该溶液做实验,溶液的颜色变化如图:
。用该溶液做实验,溶液的颜色变化如图:
以下结论和解释正确的是( )
 。用该溶液做实验,溶液的颜色变化如图:
。用该溶液做实验,溶液的颜色变化如图:
以下结论和解释正确的是( )
| A.由实验①可推知正反应的△H>0 |
| B.实验②是由于c(H2O)增大,导致平衡逆向移动 |
| C.由实验③可知配离子的稳定性:[ZnCl4]2->[CoCl4]2- |
| D.原蓝色溶液中加入少量NaCl固体,实验现象与实验③相同 |
您最近一年使用:0次
【推荐3】常温下,分别向体积均为10mL,浓度均为0.1mol·L-1的KSCN溶液、K2CrO4溶液滴加0.1mol·L-1AgNO3溶液,溶液中酸根离子浓度负对数(pM)与AgNO3溶液体积的关系如图[已知:pM=-lg(SCN-)或-lgc(CrO )]。下列说法正确的是
)]。下列说法正确的是
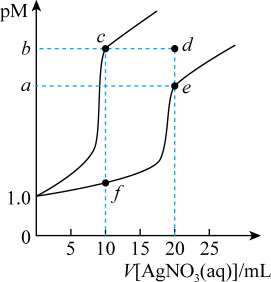
 )]。下列说法正确的是
)]。下列说法正确的是
| A.溶解度:AgSCN>Ag2CrO4 | B.Ksp(Ag2CrO4)=4×10-3a |
| C.d点Ag2CrO4溶液是不饱和溶液 | D.c(Ag+):f点溶液>e点溶液 |
您最近一年使用:0次
多选题
|
较难
(0.4)
解题方法
【推荐1】亚磷酸钠 是一种强还原剂,也是一种性能较高的催化剂。亚磷酸受热易分解,碱性条件下更易发生。以含有微量
是一种强还原剂,也是一种性能较高的催化剂。亚磷酸受热易分解,碱性条件下更易发生。以含有微量 的
的 为原料,制备高纯度氢磺酸和亚磷酸钠
为原料,制备高纯度氢磺酸和亚磷酸钠 的工业流程如下。
的工业流程如下。
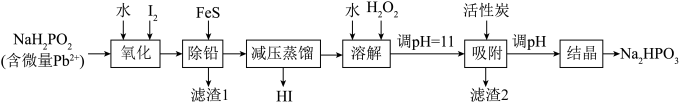
已知:减压蒸馏过程中, 的回收率超过95%。
的回收率超过95%。
下列说法正确的是
 是一种强还原剂,也是一种性能较高的催化剂。亚磷酸受热易分解,碱性条件下更易发生。以含有微量
是一种强还原剂,也是一种性能较高的催化剂。亚磷酸受热易分解,碱性条件下更易发生。以含有微量 的
的 为原料,制备高纯度氢磺酸和亚磷酸钠
为原料,制备高纯度氢磺酸和亚磷酸钠 的工业流程如下。
的工业流程如下。
已知:减压蒸馏过程中,
 的回收率超过95%。
的回收率超过95%。下列说法正确的是
A.“氧化”过程中反应的离子方程式为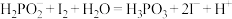 |
B.“除铅”过程说明FeS与PbS的溶度积大小关系: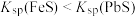 |
C.“减压蒸馏”过程后剩余固体的主要成分为 、 、 ,且物质的量比接近1:1 ,且物质的量比接近1:1 |
D.“吸附”过程中得到的滤渣2主要成分为 |
您最近一年使用:0次
【推荐2】 时,
时, 的
的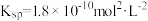 ,
, 在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是
在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是
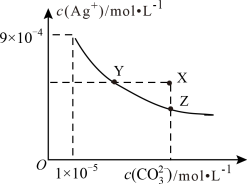
 时,
时, 的
的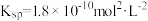 ,
, 在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是
在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是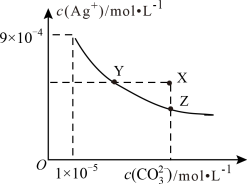
A. 的 的 为 为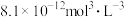 |
B.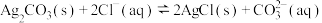 的平衡常数 的平衡常数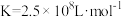 |
C.向 的饱和溶液中加入 的饱和溶液中加入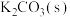 ,可使 ,可使 增大(由Y点到X点) 增大(由Y点到X点) |
D.向同浓度的 和 和 的混合溶液中滴入 的混合溶液中滴入 溶液, 溶液, 先沉淀 先沉淀 |
您最近一年使用:0次
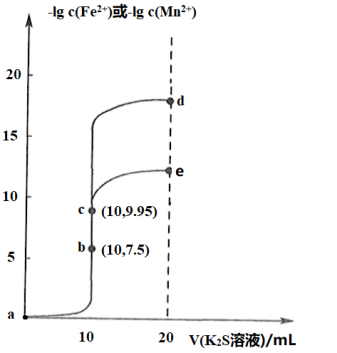
【推荐1】常温下,分别向体积均为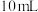 、浓度均为
、浓度均为 的
的 和
和 溶液中滴加
溶液中滴加 的
的 溶液,滴加过程中溶液
溶液,滴加过程中溶液 和
和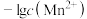 与滴入
与滴入 溶液体积(
溶液体积( )的关系如图所示。[已知:
)的关系如图所示。[已知: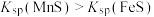 ,
, ,忽略溶液混合时温度和体积的变化],下列说法错误的是
,忽略溶液混合时温度和体积的变化],下列说法错误的是
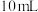 、浓度均为
、浓度均为 的
的 和
和 溶液中滴加
溶液中滴加 的
的 溶液,滴加过程中溶液
溶液,滴加过程中溶液 和
和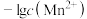 与滴入
与滴入 溶液体积(
溶液体积( )的关系如图所示。[已知:
)的关系如图所示。[已知: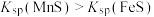 ,
, ,忽略溶液混合时温度和体积的变化],下列说法错误的是
,忽略溶液混合时温度和体积的变化],下列说法错误的是
A.加入过量难溶 可除去 可除去 溶液中混有的 溶液中混有的 |
| B.e点纵坐标约为13.5 |
C.d点钾离子的物质的量浓度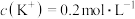 |
| D.溶液的pH:d>c>a |
您最近一年使用:0次
【推荐2】 时,
时, 的
的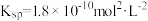 ,
, 在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是
在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是
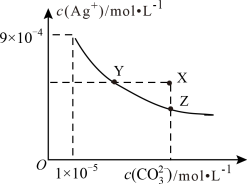
 时,
时, 的
的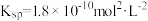 ,
, 在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是
在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是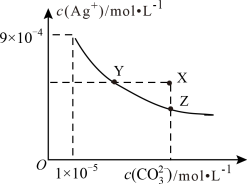
A. 的 的 为 为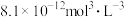 |
B.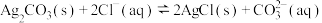 的平衡常数 的平衡常数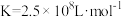 |
C.向 的饱和溶液中加入 的饱和溶液中加入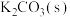 ,可使 ,可使 增大(由Y点到X点) 增大(由Y点到X点) |
D.向同浓度的 和 和 的混合溶液中滴入 的混合溶液中滴入 溶液, 溶液, 先沉淀 先沉淀 |
您最近一年使用:0次

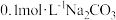 溶液中:
溶液中:
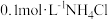 溶液中:
溶液中: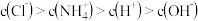
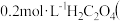 弱酸
弱酸 与
与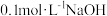 溶液等体积混合的溶液中:
溶液等体积混合的溶液中: 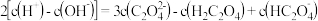
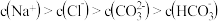
 ,溶液中存在平衡:
,溶液中存在平衡: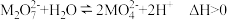 。分别在
。分别在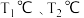 恒温条件下,向
恒温条件下,向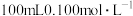 的
的 传感器连续测量溶液的
传感器连续测量溶液的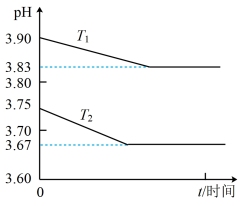

 时平衡常数的数量级是
时平衡常数的数量级是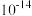
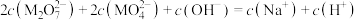
 温度下,加入
温度下,加入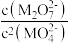 减小
减小 、
、 两种溶液,
两种溶液,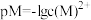 (M=Cu、Fe),pM随pH变化关系如图所示,已知水溶液中
(M=Cu、Fe),pM随pH变化关系如图所示,已知水溶液中 比
比 更难溶。下列说法错误的是
更难溶。下列说法错误的是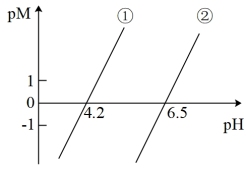

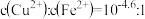
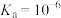 ,则
,则

