常温下,向含 、
、 、
、 的溶液中缓慢滴加
的溶液中缓慢滴加 稀溶液,溶液中
稀溶液,溶液中 [
[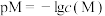 ,
,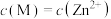 、
、 、
、 ]与
]与 [
[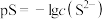 ]的关系如图所示。已知:常温下,
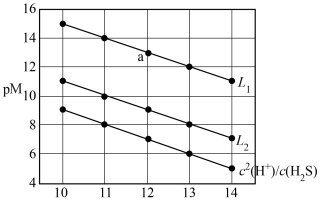
]的关系如图所示。已知:常温下,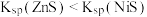 。下列叙述正确的是
。下列叙述正确的是
 、
、 、
、 的溶液中缓慢滴加
的溶液中缓慢滴加 稀溶液,溶液中
稀溶液,溶液中 [
[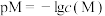 ,
,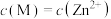 、
、 、
、 ]与
]与 [
[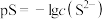 ]的关系如图所示。已知:常温下,
]的关系如图所示。已知:常温下,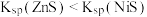 。下列叙述正确的是
。下列叙述正确的是
A. 直线代表 直线代表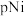 和 和 的关系 的关系 |
B.室温下, |
C.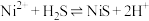 的平衡常数 的平衡常数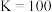 |
D.向a点溶液中滴加 浓溶液,a点沿 浓溶液,a点沿 向右移动 向右移动 |
更新时间:2023/12/16 19:48:20
|
相似题推荐
多选题
|
较难
(0.4)
解题方法
【推荐1】反应 的速率方程为
的速率方程为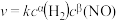 ,该反应在不同条件下的反应速率如下:
,该反应在不同条件下的反应速率如下:
下列说法正确的是
 的速率方程为
的速率方程为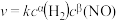 ,该反应在不同条件下的反应速率如下:
,该反应在不同条件下的反应速率如下:| 温度 |  | 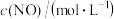 | 反应速率 |
| T1 | 0.1 | 0.1 |  |
| T1 | 0.2 | 0.2 | 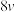 |
| T1 | 0.3 | 0.2 | 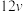 |
| T2 | 0.3 | 0.2 |  |
| A. T2> T1 |
B.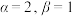 |
C.其他条件不变时,反应体系中四种物质浓度的改变,只有反应物浓度改变对 有影响,且 有影响,且 影响较大 影响较大 |
D.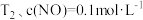 条件下,反应速率为 条件下,反应速率为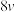 ,则 ,则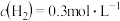 |
您最近一年使用:0次
多选题
|
较难
(0.4)
解题方法
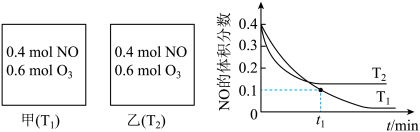
【推荐2】烟气中的NO经过O3预处理,再用CaSO3悬浊液吸收去除。预处理时发生反应:NO(g)+O3(g) NO2(g)+O2(g)。测得:v正=k正c(NO)·c(O3),v逆=k逆c(NO2)·c(O2),k正、k逆为速率常数,受温度影响。向容积均为2L的甲、乙两个密闭容器中充入一定量的NO和O3,测得NO的体积分数随时间的变化如图所示。下列说法正确的是( )
NO2(g)+O2(g)。测得:v正=k正c(NO)·c(O3),v逆=k逆c(NO2)·c(O2),k正、k逆为速率常数,受温度影响。向容积均为2L的甲、乙两个密闭容器中充入一定量的NO和O3,测得NO的体积分数随时间的变化如图所示。下列说法正确的是( )
 NO2(g)+O2(g)。测得:v正=k正c(NO)·c(O3),v逆=k逆c(NO2)·c(O2),k正、k逆为速率常数,受温度影响。向容积均为2L的甲、乙两个密闭容器中充入一定量的NO和O3,测得NO的体积分数随时间的变化如图所示。下列说法正确的是( )
NO2(g)+O2(g)。测得:v正=k正c(NO)·c(O3),v逆=k逆c(NO2)·c(O2),k正、k逆为速率常数,受温度影响。向容积均为2L的甲、乙两个密闭容器中充入一定量的NO和O3,测得NO的体积分数随时间的变化如图所示。下列说法正确的是( )
| A.高温有利于提高容器中NO的平衡转化率 |
B.T1时,反应在t1min内的平均速率v(O2)=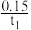 mol·L-1·min-1 mol·L-1·min-1 |
C.T1时,NO(g)+O3(g) NO2(g)+O2(g)的k正>3k逆 NO2(g)+O2(g)的k正>3k逆 |
| D.T2时,向2L密闭容器中充入0.6molNO、0.4molO3,到达平衡时c(NO2)小于乙容器中平衡时c(NO2) |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
【推荐3】用活性炭还原NO2可防止空气污染,其反应原理为2C(s)+2NO2(g)⇌N2(g)+2CO2(g)。在密闭容器中1 mol NO2和足量C发生上述反应,反应相同时间内测得NO2的生成速率与N2的生成速率随温度变化的关系如图1所示;维持温度不变,反应相同时间内测得NO2的转化率随压强的变化如图2所示。
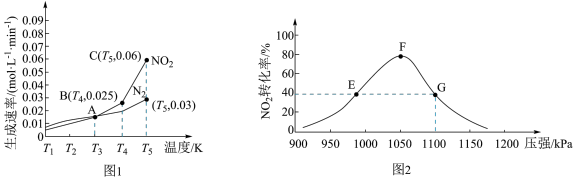
下列说法错误的是

下列说法错误的是
| A.图2中平衡常数K(E)=K(G),则NO2的平衡浓度c(E)=c(G) |
| B.图2中E点的v逆小于F点的v正 |
| C.图1中的A、B、C三个点中只有C点的v正=v逆 |
| D.在恒温恒容下,向图2中G点平衡体系中充入一定量的NO2,与原平衡相比,NO2的平衡转化率增大 |
您最近一年使用:0次
【推荐1】 时,
时, 的
的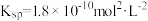 ,
, 在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是
在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是
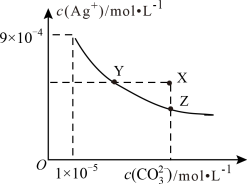
 时,
时, 的
的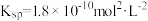 ,
, 在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是
在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是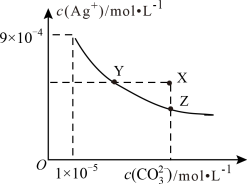
A. 的 的 为 为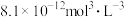 |
B.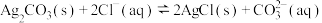 的平衡常数 的平衡常数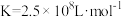 |
C.向 的饱和溶液中加入 的饱和溶液中加入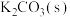 ,可使 ,可使 增大(由Y点到X点) 增大(由Y点到X点) |
D.向同浓度的 和 和 的混合溶液中滴入 的混合溶液中滴入 溶液, 溶液, 先沉淀 先沉淀 |
您最近一年使用:0次
【推荐2】已知 p(A)=-lgc平(A)。三种金属硫化物在水中的沉淀溶解平衡曲线如图 所示。下列说法不正确的是


| A.a 点有 ZnS 沉淀生成 |
| B.可用 MnS 除去 MnCl2溶液中混有的少量 ZnCl2 |
| C.向 CuS 悬浊液中加入少量水,平衡向溶解的方向移动,c平(S2-)增大 |
D.CuS 和 MnS 共存的悬浊液中,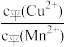 =10-20 =10-20 |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
解题方法
【推荐1】下列实验不能达到预期实验目的的是。
| 选项 | 实验 | 实验目的 |
| A | 室温下,用 计测定浓度均为 计测定浓度均为 的 的 溶液和 溶液和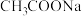 溶液的 溶液的 | 比较 和 和 的酸性强弱 的酸性强弱 |
| B | 向盛有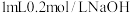 溶液的试管中滴加2滴 溶液的试管中滴加2滴 的 的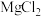 溶液,产生白色沉淀后,再滴加2滴 溶液,产生白色沉淀后,再滴加2滴 的 的 溶液,又产生红褐色沉淀 溶液,又产生红褐色沉淀 | 验证该温度下: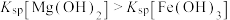 |
| C | 少量 粉加入 粉加入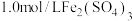 溶液中 溶液中 | 比较 、 、 的金属性强弱 的金属性强弱 |
| D | 室温下,分别向2支试管中加入相同体积、相同浓度的 溶液,再分别加入相同体积、不同浓度的稀硫酸 溶液,再分别加入相同体积、不同浓度的稀硫酸 | 研究浓度对反应速率的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
【推荐2】常温下,将0.05mol BaSO4粉末置于盛有1L蒸馏水的烧杯中,向烧杯中加入Na2CO3固体(忽略溶液体积变化)并充分搅拌,加入Na2CO3固体的过程中,溶液中各离子浓度变化曲线如图所示。已知:lg2=0.3;lg2.5=0.4;lg5=0.7,下列说法错误的是
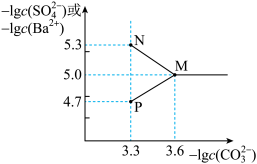

| A.图中表示c(Ba2+)的曲线是MN |
B.P点溶液中离子浓度大小为: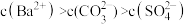 |
C.常温下 的平衡常数的数量级为10-2 的平衡常数的数量级为10-2 |
| D.若使0.05mol BaSO4全部转化为BaCO3,至少要加入1.25mol Na2CO3 |
您最近一年使用:0次
【推荐3】水垢中含有的 CaSO4,可先用 Na2CO3 溶液处理,使之转化为疏松、易溶于酸的 CaCO3。某化学兴趣小组用某浓度的 Na2CO3 溶液处理一定量的 CaSO4 固体,测得所加 Na2CO3 溶液体积与溶液中-lgc(CO32-)的关系如下:
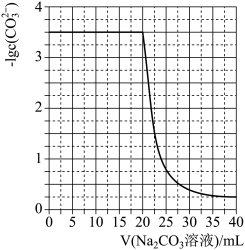
已知Ksp(CaSO4)=9×10-6,Ksp(CaCO3)=3×10-9,lg3=0.5,下列说法不正确的是

已知Ksp(CaSO4)=9×10-6,Ksp(CaCO3)=3×10-9,lg3=0.5,下列说法不正确的是
A.曲线上各点的溶液满足关系式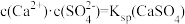 |
B.CaSO4(s)+  (aq) (aq) CaCO3(s)+ CaCO3(s)+ (aq)K=3×103 (aq)K=3×103 |
| C.该Na2CO3溶液的浓度为1.5 mol/L |
| D.相同实验条件下,若将Na2CO3溶液的浓度改为原浓度的2倍,则上图曲线整体向上平移1个单位即可 |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
【推荐1】一定温度下,金属硫化物的沉淀溶解平衡曲线如图所示。纵坐标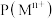 表示
表示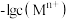 ,横坐标
,横坐标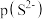 表示
表示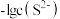 ,下列说法不正确的是
,下列说法不正确的是
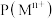 表示
表示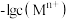 ,横坐标
,横坐标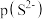 表示
表示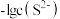 ,下列说法不正确的是
,下列说法不正确的是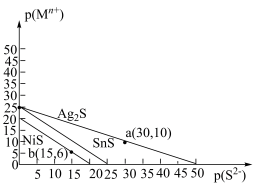
A.该温度下, 的 的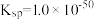 |
B.该温度下,溶解度的大小顺序为 |
C.SnS和NiS的饱和溶液中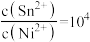 |
D.向浓度均为 的 的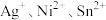 混合溶液中逐滴加入饱和 混合溶液中逐滴加入饱和 溶液, 溶液, 、 、 同时沉淀析出, 同时沉淀析出, 最后沉淀析出 最后沉淀析出 |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
解题方法
【推荐2】用下列实验方案或装置进行实验,不能达到相应实验目的的是
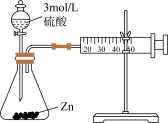
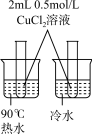
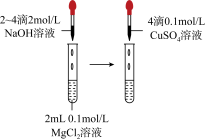
| 选项 | A | B | C | D |
| 实验方案或装置 |
|
|
|
|
| 实验目的 | 中和热的测定 | 测定锌与稀硫酸反应的化学反应速率 | 探究温度对化学平衡的影响 | 比较Mg(OH)2与Cu(OH)2的Ksp大小 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 、
、 纳米粒子。常温下,
纳米粒子。常温下, 的
的 ,
, ,溶液中平衡时相关离子浓度的关系如图所示。下列说法错误的是
,溶液中平衡时相关离子浓度的关系如图所示。下列说法错误的是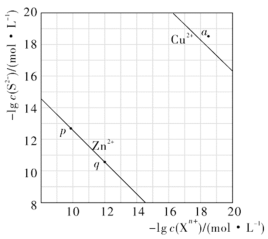
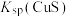 的数量级为
的数量级为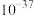
 平衡常数很大,反应趋于完全
平衡常数很大,反应趋于完全
 溶液,有黑色沉淀生成
溶液,有黑色沉淀生成
 ,溶液变为紫红色
,溶液变为紫红色
 混合,得到101 mL混合液
混合,得到101 mL混合液

