时,
时, 的
的 ,
, 在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是
在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是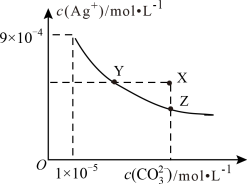
A. 的 的 为 为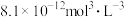 |
B.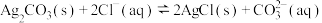 的平衡常数 的平衡常数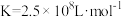 |
C.向 的饱和溶液中加入 的饱和溶液中加入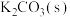 ,可使 ,可使 增大(由Y点到X点) 增大(由Y点到X点) |
D.向同浓度的 和 和 的混合溶液中滴入 的混合溶液中滴入 溶液, 溶液, 先沉淀 先沉淀 |
更新时间:2020-09-13 21:48:14
|
相似题推荐
多选题
|
较难
(0.4)
【推荐1】常温下,向含 、
、 、
、 的溶液中缓慢滴加
的溶液中缓慢滴加 稀溶液,溶液中
稀溶液,溶液中 [
[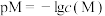 ,
,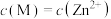 、
、 、
、 ]与
]与 [
[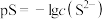 ]的关系如图所示。已知:常温下,
]的关系如图所示。已知:常温下,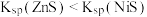 。下列叙述正确的是
。下列叙述正确的是
 、
、 、
、 的溶液中缓慢滴加
的溶液中缓慢滴加 稀溶液,溶液中
稀溶液,溶液中 [
[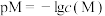 ,
,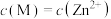 、
、 、
、 ]与
]与 [
[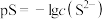 ]的关系如图所示。已知:常温下,
]的关系如图所示。已知:常温下,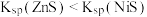 。下列叙述正确的是
。下列叙述正确的是
A. 直线代表 直线代表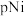 和 和 的关系 的关系 |
B.室温下, |
C.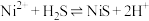 的平衡常数 的平衡常数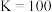 |
D.向a点溶液中滴加 浓溶液,a点沿 浓溶液,a点沿 向右移动 向右移动 |
您最近一年使用:0次
多选题
|
较难
(0.4)
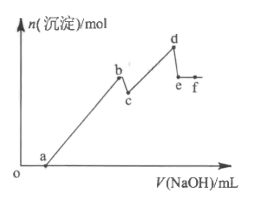
【推荐2】已知25°C时,Ksp[Mg(OH)2]=5.61×10 -12, Ksp[Al(OH)3]= 1.3×10 -33,Al(OH)3+H2O =Al(OH) +H+,Ka=6.31 ×10-13.某溶液中可能含有H+、Na+、 Mg2+、 Al3+、C1-、HCO
+H+,Ka=6.31 ×10-13.某溶液中可能含有H+、Na+、 Mg2+、 Al3+、C1-、HCO 等离子。向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示。下列有关说法正确的是
等离子。向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示。下列有关说法正确的是
 +H+,Ka=6.31 ×10-13.某溶液中可能含有H+、Na+、 Mg2+、 Al3+、C1-、HCO
+H+,Ka=6.31 ×10-13.某溶液中可能含有H+、Na+、 Mg2+、 Al3+、C1-、HCO 等离子。向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示。下列有关说法正确的是
等离子。向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示。下列有关说法正确的是
| A.各点的化学成分: b点沉淀-Al(OH)3; d点沉淀 - Al(OH)3和Mg(OH)2; e点溶质- NaCl 和NaAl(OH)4 |
B.各段只发生如下反应: ab段: A13++3OH-=Al(OH)3↓;cd段;Mg2++2OH-=Mg(OH)2↓; de段: Al(OH)3+OH-=Al(OH) |
| C.依题意,用NaOH不能完全分离Al3+和Mg2+离子 |
| D.bc段Al(OH)3部分溶解 |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
解题方法
【推荐1】铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要杂质为铁、铝、硅等的氧化物,从铬钒渣中分离提取铬和钒的一种流程如图所示。下列说法正确的是
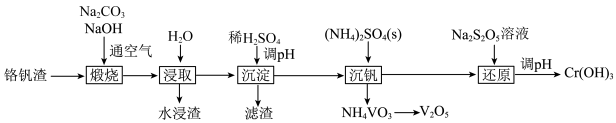
已知:①“煅烧”时铬、铝和硅的氧化物均转化为可溶性钠盐:
② 。
。

已知:①“煅烧”时铬、铝和硅的氧化物均转化为可溶性钠盐:
②
 。
。A.“煅烧”后的含铬化合物是 |
B.“滤渣”中只含有 |
C.“沉钒”时 固体可增大 固体可增大 的浓度,有利于沉淀的生成 的浓度,有利于沉淀的生成 |
D.“还原”工序中氧化剂和还原剂的物质的量之比为 |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
解题方法
【推荐2】为完成下列各组实验,所选玻璃仪器和试剂均正确、完整的是(非玻璃仪器任选;不考虑存放试剂的容器)
| 实验 | 玻璃仪器 | 试剂 | |
| A | 食盐精制 | 漏斗、烧杯、玻璃棒 | 粗食盐水、稀盐酸、NaOH溶液、BaCl2溶液、Na2CO3溶液 |
| B | 证明HCN和碳酸的酸性强弱 | 玻璃棒、玻璃片 | 0.lmol·L-1NaCN溶液和0.1mol·L-1 Na2CO3溶液 |
| C | 乙醛官能团的检验 | 试管、胶头滴管、酒精灯 | 乙醛溶液、10%NaOH溶液、2%CuSO4溶液 |
| D | 证Ksp[Mg(OH)2]>Ksp[Cu(OH)2] | 试管、胶头滴管 | 含有少量CuCl2的MgCl2溶液、稀氨水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
【推荐1】已知 p(A)=-lgc平(A)。三种金属硫化物在水中的沉淀溶解平衡曲线如图 所示。下列说法不正确的是


| A.a 点有 ZnS 沉淀生成 |
| B.可用 MnS 除去 MnCl2溶液中混有的少量 ZnCl2 |
| C.向 CuS 悬浊液中加入少量水,平衡向溶解的方向移动,c平(S2-)增大 |
D.CuS 和 MnS 共存的悬浊液中,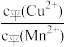 =10-20 =10-20 |
您最近一年使用:0次
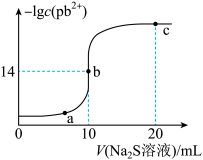
【推荐2】某温度下,向

 溶液中滴加
溶液中滴加 的
的 溶液,滴加过程中
溶液,滴加过程中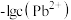 与
与 溶液体积的关系如图所示。下列有关说法正确的是
溶液体积的关系如图所示。下列有关说法正确的是


 溶液中滴加
溶液中滴加 的
的 溶液,滴加过程中
溶液,滴加过程中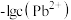 与
与 溶液体积的关系如图所示。下列有关说法正确的是
溶液体积的关系如图所示。下列有关说法正确的是
A.该温度下,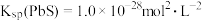 |
| B.a、b、c三点对应的溶液中,水的电离程度最小的为a点 |
C.若改用  溶液,b点应该水平左移 溶液,b点应该水平左移 |
D.若改用  溶液,b点移向右下方 溶液,b点移向右下方 |
您最近一年使用:0次
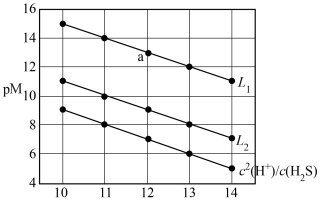
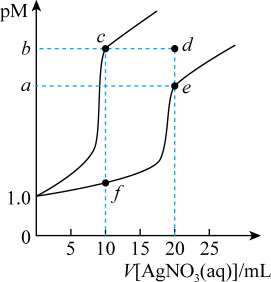
【推荐1】常温下,分别向体积均为10mL,浓度均为0.1mol·L-1的KSCN溶液、K2CrO4溶液滴加0.1mol·L-1AgNO3溶液,溶液中酸根离子浓度负对数(pM)与AgNO3溶液体积的关系如图[已知:pM=-lg(SCN-)或-lgc(CrO )]。下列说法正确的是
)]。下列说法正确的是
 )]。下列说法正确的是
)]。下列说法正确的是
| A.溶解度:AgSCN>Ag2CrO4 | B.Ksp(Ag2CrO4)=4×10-3a |
| C.d点Ag2CrO4溶液是不饱和溶液 | D.c(Ag+):f点溶液>e点溶液 |
您最近一年使用:0次
多选题
|
较难
(0.4)
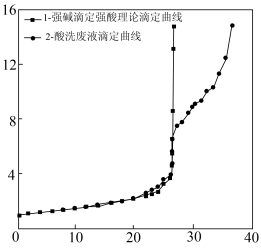
【推荐2】机车车辆配件制造过程中,为了增加配件耐腐蚀能力,要使用盐酸浸透除锈。某研究所加入屏蔽剂后使用乙基紫(变色范围 )为指示剂采取酸碱滴定的方法滴定并计算酸洗废液中的盐酸浓度,所得滴定曲线如图所示。下列说法正确的是
)为指示剂采取酸碱滴定的方法滴定并计算酸洗废液中的盐酸浓度,所得滴定曲线如图所示。下列说法正确的是
 )为指示剂采取酸碱滴定的方法滴定并计算酸洗废液中的盐酸浓度,所得滴定曲线如图所示。下列说法正确的是
)为指示剂采取酸碱滴定的方法滴定并计算酸洗废液中的盐酸浓度,所得滴定曲线如图所示。下列说法正确的是
A.酸洗废液中的主要杂质离子为 和 和 |
B.若酸洗废液中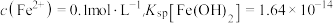 ,理论上无需屏蔽 ,理论上无需屏蔽 |
| C.滴定过程中,眼睛要紧盯滴定管的刻度变化 |
| D.图中两条曲线不能完全重合,故该方法不能达到实验目的 |
您最近一年使用:0次

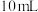 、浓度均为
、浓度均为 的
的 和
和 溶液中滴加
溶液中滴加 溶液,滴加过程中溶液
溶液,滴加过程中溶液 和
和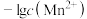 与滴入
与滴入 )的关系如图所示。[已知:
)的关系如图所示。[已知: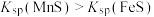 ,
, ,忽略溶液混合时温度和体积的变化],下列说法错误的是
,忽略溶液混合时温度和体积的变化],下列说法错误的是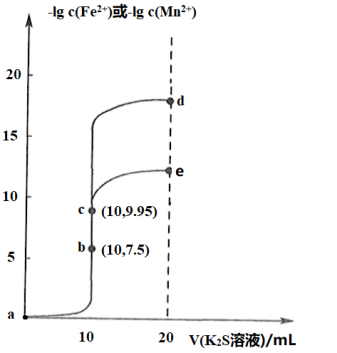
 可除去
可除去
 是一种强还原剂,也是一种性能较高的催化剂。亚磷酸受热易分解,碱性条件下更易发生。以含有微量
是一种强还原剂,也是一种性能较高的催化剂。亚磷酸受热易分解,碱性条件下更易发生。以含有微量 的
的 为原料,制备高纯度氢磺酸和亚磷酸钠
为原料,制备高纯度氢磺酸和亚磷酸钠 的工业流程如下。
的工业流程如下。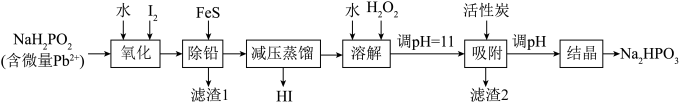
 的回收率超过95%。
的回收率超过95%。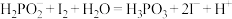
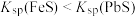
 、
、 ,且物质的量比接近1:1
,且物质的量比接近1:1
 、
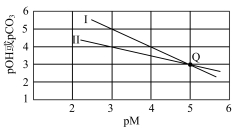
、 均是难溶物,用pM、pOH、
均是难溶物,用pM、pOH、 分别表示
分别表示 、
、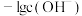 、
、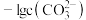 。一定温度下,
。一定温度下,