名校
解题方法
1 . 将等量的固体Mg(OH)2,置于等体积的下列液体中,最终固体剩余最少的是( )
| A.在纯水中 | B.在0.1mol/L的MgCl2溶液中 |
| C.在0.1mol/L的NH3·H2O中 | D.在0.1mol/L的CH3COOH溶液中 |
您最近一年使用:0次
2020-01-04更新
|
194次组卷
|
3卷引用:上海市静安区2020届高三上学期第一次模拟考试化学试题
名校
2 . 某温度时,TiSCN在水中的沉淀溶解平衡曲线如图所示。已知:p(Ti+)=-lgc(Ti+),p(SCN-)=-lgc(SCN-)。下列说法正确的是
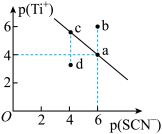

| A.该温度下,Ksp(TiSCN)=1.0×10-24 |
| B.a点的Ksp(TiSCN)小于b点的Ksp(TiSCN) |
| C.d点表示的是该温度下TiSCN的不饱和溶液 |
| D.加入TiCl(易溶于水)可以使溶液由c点变到a点 |
您最近一年使用:0次
2019-12-28更新
|
148次组卷
|
2卷引用: 上海市第二中学2022-2023学年高二下学期5月阶段测试化学试题
3 . 在25℃时,有80g饱和Ba(OH)2溶液,向其中加入纯BaO粉末ag,反应后温度恢复到25℃,下列有关该溶液的说法正确的是( )
| A.溶液中c(Ba2+)将增大 | B.溶液的pH将增大 |
| C.溶液中Ba2+的物质的量将减少 | D.溶液中c(OH-)减少 |
您最近一年使用:0次
名校
4 . 向BaCl2溶液中通入足量SO2气体,没有沉淀生成,继续滴加一定量的氨水后,生成BaSO3沉淀。用电离平衡原理解释上述现象。_______________________________
您最近一年使用:0次
2019-12-22更新
|
99次组卷
|
2卷引用:【全国百强校】上海市复旦大学附属中学2019—2020学年高三上学期期中考试化学试题
名校
5 . CH3COOH是中学化学中常用的一元弱酸,请回答下列问题:
(1)设计简单实验证明CH3COOH为弱酸__ 。
(2)向0.1mol/L CH3COOH溶液中加蒸馏水稀释至100mL,在稀释过程中,下列量的变化是(“增大”、“减小”、“不变”或“不能确定”):
n(H+)=___ , =
=___ , =
=__ ,c(OH-)=___ 。
(3)OH-浓度相同的等体积的两份溶液:盐酸和CH3COOH,分别与锌粉反应,若最后仅有一份溶液中存在锌粉,且放出氢气的质量相同,则下列说法正确的是__ (填写序号)
①反应需要的时间:CH3COOH>HCl
②开始反应的速率:HCl>CH3COOH
③参加反应的锌粉的物质的量:CH3COOH=HCl
④反应过程的平均速率:CH3COOH>HCl
⑤盐酸中有锌粉剩余
⑥CH3COOH溶液中有锌粉剩余
(4)向饱和食盐水中滴加一定浓度的盐酸,对出现现象的预测可能正确的是__ 。
A.白色沉淀 B.液体分层 C.无明显现象 D.黄绿色气体
(5)现有下列溶液:①纯水;②pH=10的NaOH溶液;③pH=3的醋酸溶液;④pH=10的CH3COONa溶液。试比较四种溶液中水的电离程度的大小关系__ 。
(1)设计简单实验证明CH3COOH为弱酸
(2)向0.1mol/L CH3COOH溶液中加蒸馏水稀释至100mL,在稀释过程中,下列量的变化是(“增大”、“减小”、“不变”或“不能确定”):
n(H+)=
 =
= =
=(3)OH-浓度相同的等体积的两份溶液:盐酸和CH3COOH,分别与锌粉反应,若最后仅有一份溶液中存在锌粉,且放出氢气的质量相同,则下列说法正确的是
①反应需要的时间:CH3COOH>HCl
②开始反应的速率:HCl>CH3COOH
③参加反应的锌粉的物质的量:CH3COOH=HCl
④反应过程的平均速率:CH3COOH>HCl
⑤盐酸中有锌粉剩余
⑥CH3COOH溶液中有锌粉剩余
(4)向饱和食盐水中滴加一定浓度的盐酸,对出现现象的预测可能正确的是
A.白色沉淀 B.液体分层 C.无明显现象 D.黄绿色气体
(5)现有下列溶液:①纯水;②pH=10的NaOH溶液;③pH=3的醋酸溶液;④pH=10的CH3COONa溶液。试比较四种溶液中水的电离程度的大小关系
您最近一年使用:0次
17-18高一上·上海·期末
名校
6 . 室温下,向饱和硫酸铜溶液中,投入不规则的胆矾,则
| A.胆矾的形状改变,质量不变 | B.体系中不再发生溶解过程 |
| C.溶液质量减小,浓度不变 | D.溶液中溶剂质量增大 |
您最近一年使用:0次
7 . 溴酸银(AgBrO3)和KNO3的溶解度随温度变化曲线如图所示:

下列分析错误的是( )

下列分析错误的是( )
| A.60℃时,AgBrO3,饱和溶液的浓度是0.596% |
| B.温度升高时AgBrO3,和KNO3溶解速度都加快 |
| C.温度对AgBrO3,溶解度的影响比对KNO3溶解度的影响大 |
| D.KNO3中少量AgBrO3可用重结晶的方法除去 |
您最近一年使用:0次
2019-11-08更新
|
167次组卷
|
2卷引用:上海市杨浦区2017-2018学年度高三第一学期高中等级考模拟调研化学试题
8 . 常温下,以MnO2为原料制得的MnCl2溶液中常合有Cu2+、Pb2+等,通过添加过量的难溶电解质MnS,可使这些金属离子形成硫化物沉淀并过滤除去,下列说法正确的是
| A.过滤后的溶液中一定没有S2- |
| B.MnS难溶于水,可溶于MnCl2溶液中 |
| C.常温时,CuS、PbS比MnS更难溶 |
| D.加入MnS后生成CuS的离子方程式是Cu2++S2-→CuS↓ |
您最近一年使用:0次
9 . 在盛有硫酸铜饱和溶液的烧杯中,投入一块不规则的硫酸铜晶体,隔一段时间后,得到的结论是( )
| A.晶体部分溶解了 | B.晶体的形状和质量不变 |
| C.晶体的质量增加了,形状也发生了改变 | D.晶体的质量不变,形状改变了 |
您最近一年使用:0次
2019-11-07更新
|
107次组卷
|
2卷引用:上海市浦东新区2016-2017学年高一上学期期末考试化学试题
10 . 请回答:
(1)写出CH3Cl的电子式____ 。
(2)甲硅烷(SiH4)是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态水。已知室温下10g甲硅烷自燃放出热量473.5kJ,其热化学方程式是____ 。
(3)工业废水中加入难溶于水的FeS使其中的Cu2+离子转化为沉淀,写出该反应的离子方程式___ 。
(4)碱性条件下发生下列反应,配平该反应的离子方程式:__ ClO3﹣+__ Fe3++__ =__ Cl﹣+__ FeO42﹣+__ 。
(1)写出CH3Cl的电子式
(2)甲硅烷(SiH4)是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态水。已知室温下10g甲硅烷自燃放出热量473.5kJ,其热化学方程式是
(3)工业废水中加入难溶于水的FeS使其中的Cu2+离子转化为沉淀,写出该反应的离子方程式
(4)碱性条件下发生下列反应,配平该反应的离子方程式:
您最近一年使用:0次



