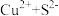请回答:
(1)写出CH3Cl的电子式____ 。
(2)甲硅烷(SiH4)是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态水。已知室温下10g甲硅烷自燃放出热量473.5kJ,其热化学方程式是____ 。
(3)工业废水中加入难溶于水的FeS使其中的Cu2+离子转化为沉淀,写出该反应的离子方程式___ 。
(4)碱性条件下发生下列反应,配平该反应的离子方程式:__ ClO3﹣+__ Fe3++__ =__ Cl﹣+__ FeO42﹣+__ 。
(1)写出CH3Cl的电子式
(2)甲硅烷(SiH4)是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态水。已知室温下10g甲硅烷自燃放出热量473.5kJ,其热化学方程式是
(3)工业废水中加入难溶于水的FeS使其中的Cu2+离子转化为沉淀,写出该反应的离子方程式
(4)碱性条件下发生下列反应,配平该反应的离子方程式:
2017·上海·模拟预测 查看更多[1]
更新时间:2019-10-27 14:08:12
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】2019年是“国际化学元素周期表年”。元素周期表中的成员数不断增加,ⅤA族元素是元素周期表中的重要组成元素。
(1)2016年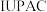 确认了四种新元素,其中之一为
确认了四种新元素,其中之一为 ,中文名为“镆”,位于第七周期ⅤA族,
,中文名为“镆”,位于第七周期ⅤA族,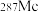 与
与 互为
互为______ 。
(2) 的同族元素氮的氧化物是大气中的主要污染物,常用氧化还原法消除,其中一种方法是:
的同族元素氮的氧化物是大气中的主要污染物,常用氧化还原法消除,其中一种方法是: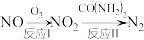
① 的电子式为
的电子式为______ ;反应Ⅰ为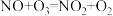 ,其中还原产物为
,其中还原产物为______ ;每消除 ,转移电子
,转移电子______  。
。
②反应Ⅱ中氧化产物与还原产物的质量比为______ 。
(3)①三碘化磷( )是一种强还原剂和脱氧剂,它遇水能水解生成亚磷酸和氢碘酸。实验室中可由白磷(
)是一种强还原剂和脱氧剂,它遇水能水解生成亚磷酸和氢碘酸。实验室中可由白磷( )与
)与 在
在 溶剂中反应制得。该反应的化学方程式为
溶剂中反应制得。该反应的化学方程式为______ 。制备时常在溶剂中加入 ,其作用是
,其作用是______ 。
②亚磷酸( )是一种中强酸,与足量的
)是一种中强酸,与足量的 溶液反应生成
溶液反应生成 和
和 。
。 属于
属于______ 元酸(填“一”“二”或“三”), 属于
属于______ (填“正盐”或“酸式盐”)。亚磷酸具有强还原性,能与 溶液反应置换出
溶液反应置换出 ,写出其离子反应方程式
,写出其离子反应方程式______ 。
(1)2016年
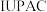 确认了四种新元素,其中之一为
确认了四种新元素,其中之一为 ,中文名为“镆”,位于第七周期ⅤA族,
,中文名为“镆”,位于第七周期ⅤA族,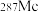 与
与 互为
互为(2)
 的同族元素氮的氧化物是大气中的主要污染物,常用氧化还原法消除,其中一种方法是:
的同族元素氮的氧化物是大气中的主要污染物,常用氧化还原法消除,其中一种方法是: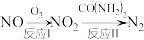
①
 的电子式为
的电子式为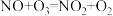 ,其中还原产物为
,其中还原产物为 ,转移电子
,转移电子 。
。②反应Ⅱ中氧化产物与还原产物的质量比为
(3)①三碘化磷(
 )是一种强还原剂和脱氧剂,它遇水能水解生成亚磷酸和氢碘酸。实验室中可由白磷(
)是一种强还原剂和脱氧剂,它遇水能水解生成亚磷酸和氢碘酸。实验室中可由白磷( )与
)与 在
在 溶剂中反应制得。该反应的化学方程式为
溶剂中反应制得。该反应的化学方程式为 ,其作用是
,其作用是②亚磷酸(
 )是一种中强酸,与足量的
)是一种中强酸,与足量的 溶液反应生成
溶液反应生成 和
和 。
。 属于
属于 属于
属于 溶液反应置换出
溶液反应置换出 ,写出其离子反应方程式
,写出其离子反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题:
(1)羟基-OH 电子式________________________________ 。
(2)在常压下,甲醇的沸点(65℃)比甲醛的沸点(-19℃)高。主要原因是________ 。
(1)羟基-OH 电子式
(2)在常压下,甲醇的沸点(65℃)比甲醛的沸点(-19℃)高。主要原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】食盐是一种重要的工业原料,可以制备多种物质。
(1)工业上用电解熔融氯化钠制取金属钠,其装置和电极上发生反应的原理示意图如图所示。

①熔融态氯化钠通电前离子的运动状态为___________ 。
②通电后阴极上发生的变化为___________ 。
③电解熔融氯化钠的化学方程式为___________ 。
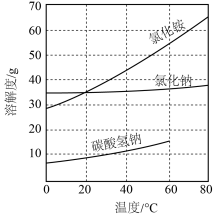
(2)“候氏制碱法”是将二氧化碳通入氨化的食盐饱和溶液中,使溶解度小的碳酸氢钠从溶液中析出: 。过滤得到的碳酸氢钠晶体,经洗涤、灼烧分解后生成碳酸钠。部分物质的溶解度曲线如图所示。
。过滤得到的碳酸氢钠晶体,经洗涤、灼烧分解后生成碳酸钠。部分物质的溶解度曲线如图所示。
①“候氏制碱法”的原料中除NaCl外,属于电解质的是___________ 。
②碳酸氢钠晶体受热分解后生成碳酸钠的化学方程式为___________ 。
③检验 洗涤干净的操作是
洗涤干净的操作是___________ 。
④滤液中除含有大量 外,还含有少量的NaCl和
外,还含有少量的NaCl和 。设计实验方案提纯
。设计实验方案提纯 样品:
样品:___________ ,冰水洗涤,低温干燥。(实验中必须用到的试剂:盐酸)
⑤图中碳酸氢钠的溶解度在60℃后无数据的原因可能是___________ 。
(1)工业上用电解熔融氯化钠制取金属钠,其装置和电极上发生反应的原理示意图如图所示。

①熔融态氯化钠通电前离子的运动状态为
②通电后阴极上发生的变化为
③电解熔融氯化钠的化学方程式为
(2)“候氏制碱法”是将二氧化碳通入氨化的食盐饱和溶液中,使溶解度小的碳酸氢钠从溶液中析出:
 。过滤得到的碳酸氢钠晶体,经洗涤、灼烧分解后生成碳酸钠。部分物质的溶解度曲线如图所示。
。过滤得到的碳酸氢钠晶体,经洗涤、灼烧分解后生成碳酸钠。部分物质的溶解度曲线如图所示。
①“候氏制碱法”的原料中除NaCl外,属于电解质的是
②碳酸氢钠晶体受热分解后生成碳酸钠的化学方程式为
③检验
 洗涤干净的操作是
洗涤干净的操作是④滤液中除含有大量
 外,还含有少量的NaCl和
外,还含有少量的NaCl和 。设计实验方案提纯
。设计实验方案提纯 样品:
样品:⑤图中碳酸氢钠的溶解度在60℃后无数据的原因可能是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】氮的化合物是重要的化工原料,其转化一直是化学研究的热点。
(1)氨催化氧化法是制硝酸的重要步骤,探究氨催化氧化反应的装置如图所示:
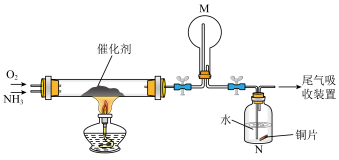
①氨催化氧化时会生成副产物N2O。生成含等物质的量氮元素的NO与N2O时,消耗的O2的物质的量之比为___________ 。
②一段时间后,观察到装置M中有白烟生成,该白烟成分是___________ (写化学式)。
(2)选择性催化还原法(SCR)工艺是以NH3 为还原剂,在催化剂作用下选择性地与NOx发生氧化还原反应生成无害化的N2和H2O。
已知:4NH3(g)+5O2(g)= 4NO(g)+6H2O(g) △H1=-905.8 kJ/mol
N2(g)+ O2(g)=2NO(g) △H2 = +180 kJ/mol
则NH3与NO反应的热化学方程式为:___________ 。
(3)可用ClO2将氮氧化物转化成 。向一定量ClO2的溶液中加入NaOH溶液调节至碱性,ClO2转化为去除氮氧化物效果更好的NaClO2,再通入NO气体进行反应。碱性条件下NaClO2去除NO反应的离子方程式为
。向一定量ClO2的溶液中加入NaOH溶液调节至碱性,ClO2转化为去除氮氧化物效果更好的NaClO2,再通入NO气体进行反应。碱性条件下NaClO2去除NO反应的离子方程式为___________ 。
(4)纳米铁粉可去除水体中的 。
。
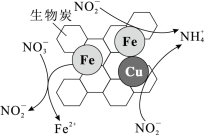
①将一定量纳米零价铁和少量铜粉附着在生物炭上,可用于去除水体中 ,其部分反应原理如图所示。与不添加铜粉相比,添加少量铜粉时去除
,其部分反应原理如图所示。与不添加铜粉相比,添加少量铜粉时去除 效率更高,其主要原因是
效率更高,其主要原因是___________ 。
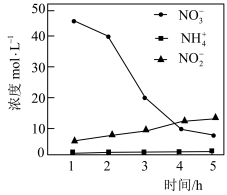
②控制其他条件不变,用纳米铁粉还原水体中的 ,测得溶液中含氮物质(
,测得溶液中含氮物质( 、
、 、
、 )浓度随时间变化如图所示。与初始溶液中
)浓度随时间变化如图所示。与初始溶液中 浓度相比,反应后溶液中所有含氮物质(
浓度相比,反应后溶液中所有含氮物质( 、
、 、
、 )总浓度减小,原因是
)总浓度减小,原因是___________ 。
(1)氨催化氧化法是制硝酸的重要步骤,探究氨催化氧化反应的装置如图所示:

①氨催化氧化时会生成副产物N2O。生成含等物质的量氮元素的NO与N2O时,消耗的O2的物质的量之比为
②一段时间后,观察到装置M中有白烟生成,该白烟成分是
(2)选择性催化还原法(SCR)工艺是以NH3 为还原剂,在催化剂作用下选择性地与NOx发生氧化还原反应生成无害化的N2和H2O。
已知:4NH3(g)+5O2(g)= 4NO(g)+6H2O(g) △H1=-905.8 kJ/mol
N2(g)+ O2(g)=2NO(g) △H2 = +180 kJ/mol
则NH3与NO反应的热化学方程式为:
(3)可用ClO2将氮氧化物转化成
 。向一定量ClO2的溶液中加入NaOH溶液调节至碱性,ClO2转化为去除氮氧化物效果更好的NaClO2,再通入NO气体进行反应。碱性条件下NaClO2去除NO反应的离子方程式为
。向一定量ClO2的溶液中加入NaOH溶液调节至碱性,ClO2转化为去除氮氧化物效果更好的NaClO2,再通入NO气体进行反应。碱性条件下NaClO2去除NO反应的离子方程式为(4)纳米铁粉可去除水体中的
 。
。①将一定量纳米零价铁和少量铜粉附着在生物炭上,可用于去除水体中
 ,其部分反应原理如图所示。与不添加铜粉相比,添加少量铜粉时去除
,其部分反应原理如图所示。与不添加铜粉相比,添加少量铜粉时去除 效率更高,其主要原因是
效率更高,其主要原因是
②控制其他条件不变,用纳米铁粉还原水体中的
 ,测得溶液中含氮物质(
,测得溶液中含氮物质( 、
、 、
、 )浓度随时间变化如图所示。与初始溶液中
)浓度随时间变化如图所示。与初始溶液中 浓度相比,反应后溶液中所有含氮物质(
浓度相比,反应后溶液中所有含氮物质( 、
、 、
、 )总浓度减小,原因是
)总浓度减小,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】化学物质在不同的领域发挥着重要的作用。根据要求回答下列问题:
(1)实验室需用Fe、C棒设计一套装置来电解饱和 溶液并检验两极生成的气体产物,则
溶液并检验两极生成的气体产物,则 棒应接直流电源的
棒应接直流电源的___________ (填“正极”或“负极”);电解开始后,阴极产物为___________ (填化学式)。
(2)将 溶液蒸干得到的物质是
溶液蒸干得到的物质是___________ ; 是一种液态化合物,遇水剧烈反应,产生白雾,同时生成能使品红溶液褪色的气体,其水解反应的化学方程式为
是一种液态化合物,遇水剧烈反应,产生白雾,同时生成能使品红溶液褪色的气体,其水解反应的化学方程式为___________ 。
(3)工业废水处理时向浓度均为 的
的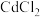 和
和 混合液中滴加碳酸铵溶液,当加入碳酸铵溶液至生成两种沉淀,则溶液中
混合液中滴加碳酸铵溶液,当加入碳酸铵溶液至生成两种沉淀,则溶液中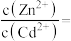
___________ 。[已知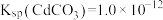 ,
,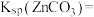
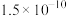 ]
]
(1)实验室需用Fe、C棒设计一套装置来电解饱和
 溶液并检验两极生成的气体产物,则
溶液并检验两极生成的气体产物,则 棒应接直流电源的
棒应接直流电源的(2)将
 溶液蒸干得到的物质是
溶液蒸干得到的物质是 是一种液态化合物,遇水剧烈反应,产生白雾,同时生成能使品红溶液褪色的气体,其水解反应的化学方程式为
是一种液态化合物,遇水剧烈反应,产生白雾,同时生成能使品红溶液褪色的气体,其水解反应的化学方程式为(3)工业废水处理时向浓度均为
 的
的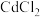 和
和 混合液中滴加碳酸铵溶液,当加入碳酸铵溶液至生成两种沉淀,则溶液中
混合液中滴加碳酸铵溶液,当加入碳酸铵溶液至生成两种沉淀,则溶液中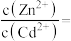
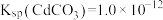 ,
,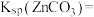
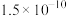 ]
]
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
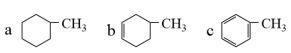
【推荐1】Ⅰ:下列有机物中属于苯的同系物的是________ (填字母),它的一氯代物有________ 种。
Ⅱ:A、B、C、D为常见物质且均含有同一种元素,它们之间的转化关系如图所示(反应条件及其他物质已经略去):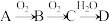
(1)若A是一种金属,C是淡黄色固体,写出C的电子式________ 。
(2)若常温下A为淡黄色固体单质,D为强酸,写出由弱酸H2S和CuSO4溶液制取D的离子方程式_____ 。
(3)若A是化合物,C是红棕色气体,D为强酸,已知A在转化为B反应中34克A完全反应生成相同条件下的液态水同时放出453 kJ的热量,则该反应的热化学方程式为________ 。
(4)若A有特殊香味的化合物,将上述转化中的H2O改为A,D为有水果香味的液体,则由C与A反应生成D的条件为______ 。

Ⅱ:A、B、C、D为常见物质且均含有同一种元素,它们之间的转化关系如图所示(反应条件及其他物质已经略去):
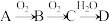
(1)若A是一种金属,C是淡黄色固体,写出C的电子式
(2)若常温下A为淡黄色固体单质,D为强酸,写出由弱酸H2S和CuSO4溶液制取D的离子方程式
(3)若A是化合物,C是红棕色气体,D为强酸,已知A在转化为B反应中34克A完全反应生成相同条件下的液态水同时放出453 kJ的热量,则该反应的热化学方程式为
(4)若A有特殊香味的化合物,将上述转化中的H2O改为A,D为有水果香味的液体,则由C与A反应生成D的条件为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】依据事实,写出下列反应的热化学方程式
(1)适量的N2和O2完全反应,每生成23 g NO2吸收16.95 kJ热量。N2与O2反应的热化学方程式为_______________________________________ 。
(2)18 g葡萄糖与适量O2反应,生成CO2和液态水,放出280.4 kJ热量。葡萄糖燃烧的热化学方程式为__________________________________________ 。
(3)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态H2O。已知室温下2 g SiH4自燃放出热量89.2 kJ。SiH4自燃的热化学方程式为____________________________________ 。
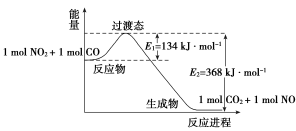
(4)如图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:____________________________________ 。
(5)直接排放煤燃烧产生的烟气会引起严重的环境问题。煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2Og)ΔH1=-867 kJ·mol-1①
2NO2(g) N2O4(g) ΔH2=-56.9 kJ·mol-1②
N2O4(g) ΔH2=-56.9 kJ·mol-1②
写出CH4(g)催化还原N2O4(g)生成N2(g)和H2O(g)的热化学方程式________________________ 。
(1)适量的N2和O2完全反应,每生成23 g NO2吸收16.95 kJ热量。N2与O2反应的热化学方程式为
(2)18 g葡萄糖与适量O2反应,生成CO2和液态水,放出280.4 kJ热量。葡萄糖燃烧的热化学方程式为
(3)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态H2O。已知室温下2 g SiH4自燃放出热量89.2 kJ。SiH4自燃的热化学方程式为
(4)如图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:

(5)直接排放煤燃烧产生的烟气会引起严重的环境问题。煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2Og)ΔH1=-867 kJ·mol-1①
2NO2(g)
 N2O4(g) ΔH2=-56.9 kJ·mol-1②
N2O4(g) ΔH2=-56.9 kJ·mol-1②写出CH4(g)催化还原N2O4(g)生成N2(g)和H2O(g)的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】按要求书写热化学方程式

(1)一定条件下,由SO2和CO反应生成S和CO2的能量变化如图所示,写出该反应的热化学方程式_________
(2)CO(g)和CH3OH(l)的燃烧热ΔH分别为- 283.0 kJ·mol -1和-726.5 kJ·mol-1。则甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为__________
(3)已知H2O(g)=H2O(l) ΔH = - 44 kJ·mol-1
则表示氢气燃烧热的热化学方程式为_____________________________

(1)一定条件下,由SO2和CO反应生成S和CO2的能量变化如图所示,写出该反应的热化学方程式
(2)CO(g)和CH3OH(l)的燃烧热ΔH分别为- 283.0 kJ·mol -1和-726.5 kJ·mol-1。则甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为
(3)已知H2O(g)=H2O(l) ΔH = - 44 kJ·mol-1
| 化学键 | O=O(g) | H—H | H—O |
| 键能/(kJ·mol-1) | 496 | 436 | 463 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)对于Ag2S(s)⇌2Ag+(aq)+S2-(aq),其Ksp的表达式为_______
(2)下列说法不正确的是_______ (填序号)。
①用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl少
②一般来说,物质的溶解度随温度的升高而增加,故物质的溶解过程大多是吸热过程
③对于Al(OH)3(s)⇌Al3+(aq)+3OH-(aq)和Al(OH)3⇌Al3++3OH-,前者为溶解平衡,后者为电离平衡
④除去溶液中的Mg2+,用OH-沉淀比用CO 好,说明Mg(OH)2的溶解度比MgCO3大
好,说明Mg(OH)2的溶解度比MgCO3大
⑤沉淀反应中常加入过量的沉淀剂,其目的是使沉淀更完全
(3)如何除去Mg(OH)2中混有的Ca(OH)2_______
(4)已知在25 ℃时Ksp[Mg(OH)2]=3.2×10-11,向0.02 mol·L-1的MgCl2溶液中加入NaOH固体,如要生成Mg(OH)2沉淀,应使溶液中的c(OH-)最小为_______ mol·L-1。
(2)下列说法不正确的是
①用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl少
②一般来说,物质的溶解度随温度的升高而增加,故物质的溶解过程大多是吸热过程
③对于Al(OH)3(s)⇌Al3+(aq)+3OH-(aq)和Al(OH)3⇌Al3++3OH-,前者为溶解平衡,后者为电离平衡
④除去溶液中的Mg2+,用OH-沉淀比用CO
 好,说明Mg(OH)2的溶解度比MgCO3大
好,说明Mg(OH)2的溶解度比MgCO3大⑤沉淀反应中常加入过量的沉淀剂,其目的是使沉淀更完全
(3)如何除去Mg(OH)2中混有的Ca(OH)2
(4)已知在25 ℃时Ksp[Mg(OH)2]=3.2×10-11,向0.02 mol·L-1的MgCl2溶液中加入NaOH固体,如要生成Mg(OH)2沉淀,应使溶液中的c(OH-)最小为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】I .(1)将等体积等物质的量浓度的醋酸和氢氧化钠溶液混合后,溶液呈___________ (填“酸性”,“中性”或“碱性”),溶液中c(Na+)___________ c(CH3COO-)(填“>”或“=”或“<”)。
(2)pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈___________ (填“酸性”,“中性”或“碱性”),溶液中c(Na+)___________ c(CH3COO-)(填“>”或“=”或“<”)。
(3)盐类水解的本质是___________ 水的电离,(填促进,抑制)。升高温度___________ 盐类的水解。(填促进,抑制)
(4)弱电解质的电离常数只受___________ 影响,升温电离常数___________ (填增大,减小或不变)
II.已知H2A在水中存在以下平衡: ,
, 
(1)常温下, 溶液的pH
溶液的pH___________ (填字母序号),原因是___________ (填离子方程式)。
A.大于7 B.小于7 C.等于7 D.无法确定
(2)常温下,若向0.1mol·L-1的H2A溶液中逐滴滴加0.1mol·L-1 NaOH溶液至溶液呈中性。此时该混合溶液中的下列关系一定正确的是___________ (填字母序号)。
A.c(H+ ). c(OH-)= 1.0×10-14 B.
C.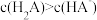 D.
D.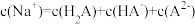
(3)常温下, 的饱和溶液中存在以下平衡:
的饱和溶液中存在以下平衡: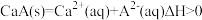 ,若要使该溶液中
,若要使该溶液中 浓度增大,可采取的措施有
浓度增大,可采取的措施有___________ (填字母序号)。
A.升高温度 B.降低温度 C.加入少量蒸馏水 D.加入 固体
固体
(2)pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈
(3)盐类水解的本质是
(4)弱电解质的电离常数只受
II.已知H2A在水中存在以下平衡:
 ,
, 
(1)常温下,
 溶液的pH
溶液的pHA.大于7 B.小于7 C.等于7 D.无法确定
(2)常温下,若向0.1mol·L-1的H2A溶液中逐滴滴加0.1mol·L-1 NaOH溶液至溶液呈中性。此时该混合溶液中的下列关系一定正确的是
A.c(H+ ). c(OH-)= 1.0×10-14 B.

C.
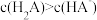 D.
D.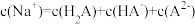
(3)常温下,
 的饱和溶液中存在以下平衡:
的饱和溶液中存在以下平衡: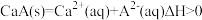 ,若要使该溶液中
,若要使该溶液中 浓度增大,可采取的措施有
浓度增大,可采取的措施有A.升高温度 B.降低温度 C.加入少量蒸馏水 D.加入
 固体
固体
您最近一年使用:0次