名校
解题方法
1 . T℃时, 和
和 的沉淀溶解平衡曲线如图所示。已知:
的沉淀溶解平衡曲线如图所示。已知: ,
, 或
或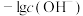 。下列说法正确的是
。下列说法正确的是

 和
和 的沉淀溶解平衡曲线如图所示。已知:
的沉淀溶解平衡曲线如图所示。已知: ,
, 或
或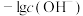 。下列说法正确的是
。下列说法正确的是
A.T℃时, |
B.Y点对应的 溶液是不饱和溶液 溶液是不饱和溶液 |
C.Z点对应的溶液中,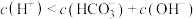 |
D.向 悬浊液中通入 悬浊液中通入 气体(忽略溶液体积的变化),溶液中 气体(忽略溶液体积的变化),溶液中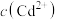 保持不变 保持不变 |
您最近一年使用:0次
名校
解题方法
2 . I.钴的配合物制取
实验室以活性炭为催化剂,用CoCl2制取[Co(NH3)6]Cl3,装置如图所示。

(1)仪器a的名称是___________ ;仪器b中的试剂是___________ ;冷凝管作用是___________ 。
II.将0.1 mol/L CoCl2、NH4Cl混合液在三颈烧瓶中混合,滴加浓氨水,溶液变为棕色。已知:①[Co(NH3)6]2+具有较强还原性;溶液呈棕色。②Ksp[Co(OH)2] = 6×10-15
(2)请计算常温下该混合液中Co2+开始沉淀的pH值(精确到0.01),列出必要过程________ 。NH4Cl的作用是___________ 。
(3)充分反应后缓慢滴加双氧水,水浴加热20 min(该过程生成OH-)。发生反应的离子方程式为___________ 。将反应后的混合液冷却后加入适量浓盐酸,过滤、洗涤、干燥,得到[Co(NH3)6]Cl3晶体。
III.已知[Co(NH3)6]Cl3可溶于热水,微溶于冷水,难溶于乙醇。
(4)请运用平衡移动原理解释加入浓盐酸的目的是_____________ 。
(5)[Co(NH3)6]3+ Co3+ + 6NH3 K1;
Co3+ + 6NH3 K1;
 NH3 + H+ K2,判断K1
NH3 + H+ K2,判断K1____ (K2)6。(填“>”“<”或“=”)
(6)洗涤[Co(NH3)6]Cl3时可用___________。
IV.测定产品中配体NH3与外界Cl-的物质的量之比。实验如下:
①蒸氨:取0.100 g样品加入三颈烧瓶中,再加入足量NaOH溶液并充分加热,蒸出的气体全部通入V1 mL c1 mol/L的H2SO4中。
②滴定:用c2 mol/L NaOH溶液滴定①中溶液,消耗V2 mL NaOH溶液。
③沉淀:另取0.100 g样品溶解,加入足量AgNO3溶液,过滤、洗涤、干燥、恒重,得到沉淀m3 g。(MAgCl = 143.5 g/mol)
(7)滴定时选用的指示剂为___________ 。
(8)测得产品中配体NH3与外界Cl-的物质的量比值为________ 。(用含c1、V1等数据的代数式表示)若测得n(NH3) : n(Cl-)比值偏小,可能的原因是________ 。
A.蒸氨结束时,未用蒸馏水洗涤冷凝管,并将洗涤液一并倒入H2SO4中
B.滴定步骤的NaOH溶液使用前敞口放置于空气中一段时间
C.滴定步骤中盛放NaOH溶液的滴定管未用NaOH溶液润洗
D.沉淀步骤中,沉淀未完全转移至漏斗中
实验室以活性炭为催化剂,用CoCl2制取[Co(NH3)6]Cl3,装置如图所示。

(1)仪器a的名称是
II.将0.1 mol/L CoCl2、NH4Cl混合液在三颈烧瓶中混合,滴加浓氨水,溶液变为棕色。已知:①[Co(NH3)6]2+具有较强还原性;溶液呈棕色。②Ksp[Co(OH)2] = 6×10-15
(2)请计算常温下该混合液中Co2+开始沉淀的pH值(精确到0.01),列出必要过程
(3)充分反应后缓慢滴加双氧水,水浴加热20 min(该过程生成OH-)。发生反应的离子方程式为
III.已知[Co(NH3)6]Cl3可溶于热水,微溶于冷水,难溶于乙醇。
(4)请运用平衡移动原理解释加入浓盐酸的目的是
(5)[Co(NH3)6]3+
 Co3+ + 6NH3 K1;
Co3+ + 6NH3 K1;
 NH3 + H+ K2,判断K1
NH3 + H+ K2,判断K1(6)洗涤[Co(NH3)6]Cl3时可用___________。
| A.蒸馏水 | B.冰水 | C.无水乙醇 | D.50%乙醇水溶液 |
IV.测定产品中配体NH3与外界Cl-的物质的量之比。实验如下:
①蒸氨:取0.100 g样品加入三颈烧瓶中,再加入足量NaOH溶液并充分加热,蒸出的气体全部通入V1 mL c1 mol/L的H2SO4中。
②滴定:用c2 mol/L NaOH溶液滴定①中溶液,消耗V2 mL NaOH溶液。
③沉淀:另取0.100 g样品溶解,加入足量AgNO3溶液,过滤、洗涤、干燥、恒重,得到沉淀m3 g。(MAgCl = 143.5 g/mol)
(7)滴定时选用的指示剂为
(8)测得产品中配体NH3与外界Cl-的物质的量比值为
A.蒸氨结束时,未用蒸馏水洗涤冷凝管,并将洗涤液一并倒入H2SO4中
B.滴定步骤的NaOH溶液使用前敞口放置于空气中一段时间
C.滴定步骤中盛放NaOH溶液的滴定管未用NaOH溶液润洗
D.沉淀步骤中,沉淀未完全转移至漏斗中
您最近一年使用:0次
名校
解题方法
3 . 门捷列夫最早预言了具有半导体特性类硅元素锗(32Ge),工业上用精硫锗矿(主要成分为 )制取高纯度锗,其工艺流程如图所示:
)制取高纯度锗,其工艺流程如图所示:
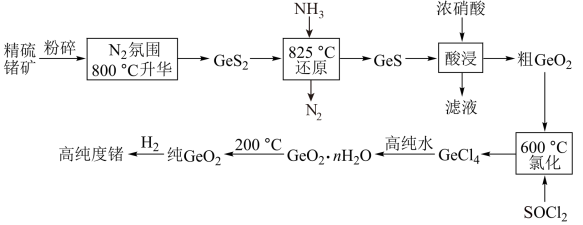
已知:①硅和锗是同主族相邻元素,结构和性质类似;
② 在
在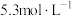 的盐酸中溶解度最小。
的盐酸中溶解度最小。
(1)基态锗原子的价层电子排布式为___________ ,晶体锗的晶体类型是___________ 。
(2)① ,使精硫锗矿在
,使精硫锗矿在 氛围中升华的原因是
氛围中升华的原因是___________ 。
②还原时发生反应:___________ ___________
___________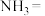 ___________
___________ ___________
___________ ___________
___________ 。配平上述反应的化学方程式,标出电子转移的方向和数目
。配平上述反应的化学方程式,标出电子转移的方向和数目______________ 。
③比较键角:
___________  (选填编号)。其原因是
(选填编号)。其原因是___________ 。
A.> B.< C.=
(3)酸浸时温度不能过高的原因是___________ 。氯化除生成 外,反应还生成一种V形分子,相应的化学方程式为
外,反应还生成一种V形分子,相应的化学方程式为___________ 。 水解得到
水解得到 ,该步骤高纯水不能过量,原因是
,该步骤高纯水不能过量,原因是___________ 。
(4) 与碱反应可生成锗酸盐,其中
与碱反应可生成锗酸盐,其中 是一种难溶电解质,一定温度下,
是一种难溶电解质,一定温度下, 在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是___________(选填编号)。
在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是___________(选填编号)。
 )制取高纯度锗,其工艺流程如图所示:
)制取高纯度锗,其工艺流程如图所示:
已知:①硅和锗是同主族相邻元素,结构和性质类似;
②
 在
在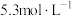 的盐酸中溶解度最小。
的盐酸中溶解度最小。(1)基态锗原子的价层电子排布式为
(2)①
 ,使精硫锗矿在
,使精硫锗矿在 氛围中升华的原因是
氛围中升华的原因是②还原时发生反应:___________
 ___________
___________ ___________
___________ ___________
___________ ___________
___________ 。配平上述反应的化学方程式,标出电子转移的方向和数目
。配平上述反应的化学方程式,标出电子转移的方向和数目③比较键角:

 (选填编号)。其原因是
(选填编号)。其原因是A.> B.< C.=
(3)酸浸时温度不能过高的原因是
 外,反应还生成一种V形分子,相应的化学方程式为
外,反应还生成一种V形分子,相应的化学方程式为 水解得到
水解得到 ,该步骤高纯水不能过量,原因是
,该步骤高纯水不能过量,原因是(4)
 与碱反应可生成锗酸盐,其中
与碱反应可生成锗酸盐,其中 是一种难溶电解质,一定温度下,
是一种难溶电解质,一定温度下, 在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是___________(选填编号)。
在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是___________(选填编号)。
A.n点与p点对应的 相等 相等 |
B.q点无 沉淀生成 沉淀生成 |
| C.通过蒸发可以使溶液由q点变到p点 |
D.加入 可以使溶液由n点变到m点 可以使溶液由n点变到m点 |
您最近一年使用:0次
4 . 在25℃时,有80g饱和Ba(OH)2溶液,向其中加入纯BaO粉末ag,反应后温度恢复到25℃,下列有关该溶液的说法正确的是( )
| A.溶液中c(Ba2+)将增大 | B.溶液的pH将增大 |
| C.溶液中Ba2+的物质的量将减少 | D.溶液中c(OH-)减少 |
您最近一年使用:0次
5 . 常温下,以MnO2为原料制得的MnCl2溶液中常合有Cu2+、Pb2+等,通过添加过量的难溶电解质MnS,可使这些金属离子形成硫化物沉淀并过滤除去,下列说法正确的是
| A.过滤后的溶液中一定没有S2- |
| B.MnS难溶于水,可溶于MnCl2溶液中 |
| C.常温时,CuS、PbS比MnS更难溶 |
| D.加入MnS后生成CuS的离子方程式是Cu2++S2-→CuS↓ |
您最近一年使用:0次
6 . 常温下,Ca(OH)2的溶解度为0.16克/100克水。向盛有50毫升水的烧杯中加入2克生石灰,搅拌后恢复到原温。下列说法正确的是
| A.在此过程中,水的Kw值始终保持不变 |
| B.在此过程中,Ca(OH)2的电离程度先变大后变小,最后不变 |
| C.反应结束后,溶液中水的电离程度比纯水小 |
| D.最后所得体系中的平衡状态只有水的电离平衡 |
您最近一年使用:0次
名校
7 . 已知溴酸银的溶解是吸热过程,在不同温度条件下,溴酸银的溶解平衡曲线如图所示,下列说法正确的是( )
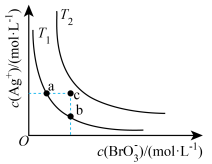

| A.T1>T2 |
| B.加入AgNO3固体,可从a点变到c点 |
| C.a点和b点的Ksp相等 |
| D.c点时,在T1、T2两个温度条件下均有固体析出 |
您最近一年使用:0次
2017-05-12更新
|
456次组卷
|
10卷引用:上海市嘉定区第二中学2022-2023学年高二下学期第一次质量检测化学试题
上海市嘉定区第二中学2022-2023学年高二下学期第一次质量检测化学试题宁夏银川市第一中学2016-2017学年高二下学期期中考试化学试题陕西省西安市长安区第一中学2017-2018学年高二上学期期中考试化学(重点、平行班)试题内蒙古翁牛特旗乌丹第二中学、呼和浩特市第二十一中学2017-2018学年高二上学期期末联考化学试题(已下线)二轮复习 专题11 水溶液中的离子平衡 押题专练【全国百强校】内蒙古第一机械制造(集团)有限公司第一中学2018-2019学年高二上学期期中考试化学试题辽宁省渤海大学附属高级中学2021-2022学年高二上学期第二次月考化学试题甘肃省民勤县第一中学2021-2022学年高二上学期期末考试化学试题山西省运城市教育发展联盟2021-2022学年高二上学期11月期中检测化学试题吉林省长春市朝阳区长春外国语学校2022-2023学年高二上学期11月期中化学试题
16-17高三上·江苏南通·阶段练习
名校
8 . 下列图示与对应的叙述相符的是
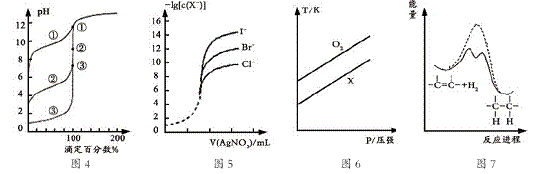

| A.用0.1000mol/L NaOH溶液分别滴定浓度相同的三种一元酸,由图4曲线确定①的酸性最强 |
| B.用0.0100mol/L硝酸银标准溶液,滴定浓度均为0.1000mol/L Cl-、Br-及I-的混合溶液,由图5曲线,可确定首先沉淀的是Cl- |
| C.在体积相同的两个密闭容器中,分别充入相同质量O2和X气体,由图6可确定X可能是CH4气体 |
| D.由图7可说明烯烃与H2加成反应是放热反应,虚线表示在有催化剂的条件下进行 |
您最近一年使用:0次
2016-12-09更新
|
337次组卷
|
4卷引用:上海建平高级中学 2012-2013学年高三下学期模拟化学试题
(已下线)上海建平高级中学 2012-2013学年高三下学期模拟化学试题2017届江苏省通州高级中学高三上第一次测试化学试卷2017届四川省绵阳市东辰国际学校高三上学期第四次月考理科综合化学试卷备考突破2020高三化学专题强化集训——酸碱中和滴定及其拓展



