常温下,Ca(OH)2的溶解度为0.16克/100克水。向盛有50毫升水的烧杯中加入2克生石灰,搅拌后恢复到原温。下列说法正确的是
| A.在此过程中,水的Kw值始终保持不变 |
| B.在此过程中,Ca(OH)2的电离程度先变大后变小,最后不变 |
| C.反应结束后,溶液中水的电离程度比纯水小 |
| D.最后所得体系中的平衡状态只有水的电离平衡 |
更新时间:2019-08-19 11:23:00
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】某温度下,由H2CO3与HCl或NaOH配制一组总含碳微粒浓度为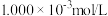 的混合溶液,混合体系中部分物种的浓度的负对数
的混合溶液,混合体系中部分物种的浓度的负对数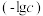 与pH关系如图所示。下列说法错误的是
与pH关系如图所示。下列说法错误的是

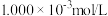 的混合溶液,混合体系中部分物种的浓度的负对数
的混合溶液,混合体系中部分物种的浓度的负对数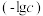 与pH关系如图所示。下列说法错误的是
与pH关系如图所示。下列说法错误的是
A.该溶液的温度为 |
B. 时,混合体系中浓度最高的含碳物种为 时,混合体系中浓度最高的含碳物种为 |
C.该条件下,H2CO3的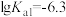 |
D. 的溶液中: 的溶液中: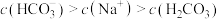 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】在某温度时,将nmol⋅L-1氨水滴入10mL1.0mol⋅L-1盐酸中,溶液pH和温度随加入氨水体积变化曲线如图所示,下列有关说法正确的是( )


| A.a点Kw=1.0×10-14 |
| B.水的电离程度:b>c>a>d |
| C.b点:c(NH4+)>c(Cl-)>c(H+)>c(OH-) |
| D.25℃时NH4Cl水解常数为(n-1)×10-7mol⋅L-1(用n表示) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】常温下,用pH传感器进行数字化实验,分别向两个盛50mL 0.100mol/L 盐酸的烧杯中匀速滴加50mL 去离子水、50mL 0.100mol/L 醋酸铵溶液,滴加过程进行磁力搅拌,测得溶液pH随时间变化如下图所示。已知常温下醋酸铵溶液pH=7,下列说法错误的是


| A.曲线X表示盐酸中加水稀释的pH变化 |
| B.曲线Y的pH变化主要是因为CH3COO-与H+结合成了弱电解质 |
| C.a点对应的溶液中c(Cl-)+c(CH3COO-)+c(CH3COOH)-c(NH4+)=0.01mol/L |
| D.b点对应的溶液中水电离的c(H+)=10-12.86mol/L |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】柠檬酸(2-羟基丙烷-1,2,3-三羧酸)是一种重要的有机弱酸(以下表示为 ),作为三羧酸循环(柠檬酸循环)的中间体,柠檬酸循环发生在所有需氧生物的新陈代谢中。现以酚酞作为指示剂,用0.1mol/L的NaOH滴定10mL0.1mol/L的柠檬酸,滴定过程中pH随NaOH体积的关系如图所示。已知柠檬酸
),作为三羧酸循环(柠檬酸循环)的中间体,柠檬酸循环发生在所有需氧生物的新陈代谢中。现以酚酞作为指示剂,用0.1mol/L的NaOH滴定10mL0.1mol/L的柠檬酸,滴定过程中pH随NaOH体积的关系如图所示。已知柠檬酸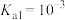 ,
,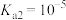 ,
,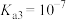 。下列说法正确的是
。下列说法正确的是
 ),作为三羧酸循环(柠檬酸循环)的中间体,柠檬酸循环发生在所有需氧生物的新陈代谢中。现以酚酞作为指示剂,用0.1mol/L的NaOH滴定10mL0.1mol/L的柠檬酸,滴定过程中pH随NaOH体积的关系如图所示。已知柠檬酸
),作为三羧酸循环(柠檬酸循环)的中间体,柠檬酸循环发生在所有需氧生物的新陈代谢中。现以酚酞作为指示剂,用0.1mol/L的NaOH滴定10mL0.1mol/L的柠檬酸,滴定过程中pH随NaOH体积的关系如图所示。已知柠檬酸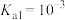 ,
, ,
,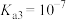 。下列说法正确的是
。下列说法正确的是
A.a点的溶液中: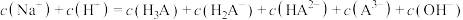 |
B.b点溶液中,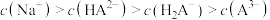 |
C.稀释b点对应的溶液,稀释过程中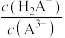 减小 减小 |
D.水的电离程度: |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】 时,用
时,用 溶液滴定同浓度的
溶液滴定同浓度的 溶液,
溶液, 被滴定分数
被滴定分数 与
与 及微粒分布分数
及微粒分布分数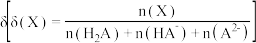 的关系如下图所示,下列说法错误的是
的关系如下图所示,下列说法错误的是
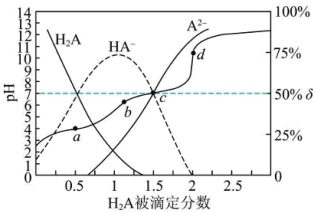
 时,用
时,用 溶液滴定同浓度的
溶液滴定同浓度的 溶液,
溶液, 被滴定分数
被滴定分数 与
与 及微粒分布分数
及微粒分布分数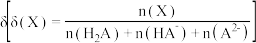 的关系如下图所示,下列说法错误的是
的关系如下图所示,下列说法错误的是
A. 时, 时, 第一步电离平衡常数 第一步电离平衡常数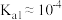 |
B. 点溶液中: 点溶液中: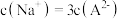 |
C.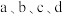 四点溶液中水的电离程度: 四点溶液中水的电离程度: |
D. 点溶液中: 点溶液中: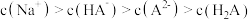 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】室温下,通过下列实验探究 溶液的性质。
溶液的性质。
实验1:用pH计测定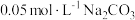 溶液的pH,测得pH约为10.3
溶液的pH,测得pH约为10.3
实验2:向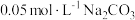 溶液中通入
溶液中通入 ,溶液pH从10.3下降到约为9
,溶液pH从10.3下降到约为9
实验3:向5mL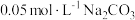 溶液中滴加等体积等浓度的盐酸,无气泡产生
溶液中滴加等体积等浓度的盐酸,无气泡产生
实验4:向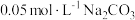 溶液中滴加过量饱和石灰水,产生白色沉淀
溶液中滴加过量饱和石灰水,产生白色沉淀
下列说法正确的是
 溶液的性质。
溶液的性质。实验1:用pH计测定
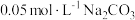 溶液的pH,测得pH约为10.3
溶液的pH,测得pH约为10.3实验2:向
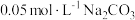 溶液中通入
溶液中通入 ,溶液pH从10.3下降到约为9
,溶液pH从10.3下降到约为9实验3:向5mL
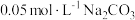 溶液中滴加等体积等浓度的盐酸,无气泡产生
溶液中滴加等体积等浓度的盐酸,无气泡产生实验4:向
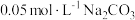 溶液中滴加过量饱和石灰水,产生白色沉淀
溶液中滴加过量饱和石灰水,产生白色沉淀下列说法正确的是
A.实验1中 溶液呈碱性的原因: 溶液呈碱性的原因: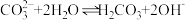 |
B.实验2反应过程中: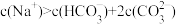 |
C.实验3滴加过程中: |
D.实验4静置后的上层清液中: |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】已知:某温度下,铁的难溶化合物FeS在溶液中存在溶解平衡FeS(s)⇌Fe2+ (aq) + S2-(aq),FeS在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是


| A.a点对应的Ksp(FeS)等于b点对应的Ksp(FeS) |
| B.c、d两点有沉淀析出的是c点 |
| C.向d点溶液中加入FeCl3溶液,溶液中的离子浓度可实现由d点到b点的变化 |
| D.该温度下,Ksp (FeS) =2×10-18 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】常温下,取一定量的PbI2固体配成饱和溶液,t时刻改变某一条件,离子浓度变化如右图所示。下列有关说法正确的是


| A.常温下,PbI2的Ksp为2×10-6 |
B.常温下,Ksp(PbS)=8×10-28,向PbI2的悬浊液中加入Na2S溶液,反应PbI2(s)+S2-(aq) PbS(s)+2I-(aq)的化学平衡常数为5×1018 PbS(s)+2I-(aq)的化学平衡常数为5×1018 |
| C.温度不变,t时刻改变的条件可能是向溶液中加入了KI固体,PbI2的Ksp增大 |
| D.温度不变,向PbI2饱和溶液中加入少量硝酸铅浓溶液,平衡向左移动,Pb2+的浓度减小 |
您最近一年使用:0次

 溶液,溶液中水电离出的
溶液,溶液中水电离出的 浓度与
浓度与


 为定值
为定值

