8. 为了研究Mg(OH)
2溶于铵盐溶液的原因,进行如下实验:
①向2mL 0.2mol/LMgCl
2溶液中滴加1mol/LNaOH溶液至不再产生沉淀,将浊液分为2等份。
②向一份中逐滴加入4mol/L NH
4Cl溶液,另一份中逐滴加入4mol/L CH
3COONH
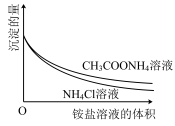
4溶液(pH≈7),边滴加边测定其中沉淀的量,沉淀的量与铵盐溶液的体积的关系如图。
③将①中的NaOH溶液用氨水替换,重复上述实验。
下列说法不正确的是
A.Mg(OH)2浊液中存在:Mg(OH)2(s) Mg2+(aq)+2OH﹣(aq) Mg2+(aq)+2OH﹣(aq) |
| B.②中两组实验中均存在反应:Mg(OH)2+2NH4+=Mg2++2NH3•H2O |
| C.H+可能参与了NH4Cl溶液溶解Mg(OH)2的过程 |
| D.③中获得的图像与②相同 |