下列说法正确的是
| A.在由水电离产生的氢离子浓度为10-13mol/L的溶液中,Ca2+、K+、Cl-、HCO3-四种离子能大量共存 |
| B.常温下,将0.2mol/L某一元碱ROH溶液和0.1mol/LHCl溶液等体积混合,混合后溶液pH<7,则该溶液c(ROH)>c(R+) |
C.反应 只在高温下自发进行 只在高温下自发进行 |
D.已知MgCO3的Ksp=6.82×10-6,则所有含有固体MgCO3的溶液中,都有: ,且 ,且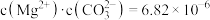 |
更新时间:2019-12-28 10:51:42
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】在强酸性无色溶液中,下列离子组能大量共存的是( )
| A.Na+、K+、OH-、Cl- | B.Na+、Cu2+、SO 、NO 、NO |
C.K+、Mg2+、SO 、Cl- 、Cl- | D.Ba2+、HCO 、NO 、NO 、K+ 、K+ |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】将足量CO2通入下列各溶液中,所含离子还能大量共存的是:
A. | B. |
C. | D.Na+、AlO 、CH3COO-、HCO 、CH3COO-、HCO |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】高温条件下,某反应机理和能量变化如下,下列说法正确的是

| A.图示反应历程包含2个基元反应 |
B.决速步骤的能垒为 |
C.总反应可表示为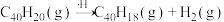 |
| D.反应在低温条件下自发 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是( )
| A.常温下,反应2Mg(s)+O2(g)=2MgO(s)能自发进行则△H>0 |
| B.反应N2(g)+3H2(g)⇌2NH3(g)△H<0达平衡后,降低温度,正反应速率增大、逆反应速率减小,平衡向正反应方向移动 |
| C.镀锌铁板是利用了牺牲阳极的阴极保护法来达到防止腐蚀的目的 |
| D.电解精炼铜时,阳极泥中含有Zn、Fe、Ag、Au等金属 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】把足量熟石灰放入蒸馏水中,一段时间后达到平衡:Ca(OH)2(s) Ca2+(aq)+2OH-(aq),下列叙述不正确的是( )
Ca2+(aq)+2OH-(aq),下列叙述不正确的是( )
 Ca2+(aq)+2OH-(aq),下列叙述不正确的是( )
Ca2+(aq)+2OH-(aq),下列叙述不正确的是( )| A.给溶液加热,Ca(OH)2的溶解度减小 |
| B.向溶液中加入少量CaO充分反应后,恢复到原温度,溶液的pH升高 |
| C.温度不变,向溶液中加入少量Na2CO3固体,充分反应后,Ksp[Ca(OH)2]不变 |
| D.向溶液中加入少量的NaOH固体,Ca(OH)2固体增多 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列图示与应叙述相符的是
A.图1表示向 氯水中逐滴加入 氯水中逐滴加入 醋酸,溶液导电性随加入酸体积的变化 醋酸,溶液导电性随加入酸体积的变化 |
B.图2表示酸性介质 原电池反应过程中的电流强度的变化,T时可能加入了 原电池反应过程中的电流强度的变化,T时可能加入了 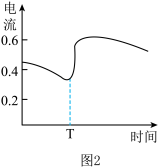 |
C.图3表示SO2与 反应过程中的能量变化,其中 反应过程中的能量变化,其中 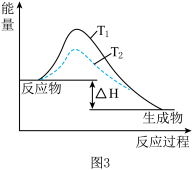 |
D.图4表示在饱和 溶液中逐步加 溶液中逐步加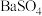 固体后,溶液中 固体后,溶液中 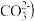 的浓度变化 的浓度变化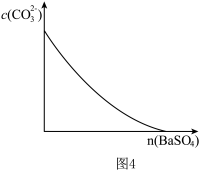 |
您最近半年使用:0次
单选题
|
适中
(0.65)
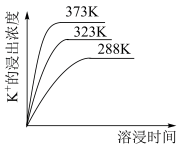
【推荐3】已知难溶性物质K2SO4·MgSO4·2CaSO4在水中存在如下平衡:K2SO4·MgSO4·2CaSO4(s) 2Ca2+(aq)+2K+(aq)+Mg2+(aq)+4
2Ca2+(aq)+2K+(aq)+Mg2+(aq)+4 (aq),不同温度下,K+的浸出浓度与溶浸时间的关系如图所示。则下列说法错误的是
(aq),不同温度下,K+的浸出浓度与溶浸时间的关系如图所示。则下列说法错误的是
 2Ca2+(aq)+2K+(aq)+Mg2+(aq)+4
2Ca2+(aq)+2K+(aq)+Mg2+(aq)+4 (aq),不同温度下,K+的浸出浓度与溶浸时间的关系如图所示。则下列说法错误的是
(aq),不同温度下,K+的浸出浓度与溶浸时间的关系如图所示。则下列说法错误的是
| A.向该体系中加入饱和NaOH溶液,沉淀溶解平衡向右移动 |
| B.向该体系中加入饱和碳酸钠溶液,沉淀溶解平衡均向右移动 |
C.该难溶性物质的Ksp=c(Ca2+)·c(K+)·c(Mg2+)·c( ) ) |
| D.升高温度,溶浸速率增大,平衡向右移动 |
您最近半年使用:0次

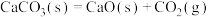 室温下不能自发进行,说明该反应的
室温下不能自发进行,说明该反应的

 ,
,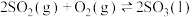
 ,则
,则
 (g)和1.5mol
(g)和1.5mol (g)反应生成
(g)反应生成 (g)放热QkJ,其热化学方程式为
(g)放热QkJ,其热化学方程式为

 、
、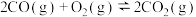 的平衡常数分别为
的平衡常数分别为 和
和 ,可推知平衡
,可推知平衡 的平衡常数为
的平衡常数为


