溴酸银(AgBrO3)和KNO3的溶解度随温度变化曲线如图所示:

下列分析错误的是( )

下列分析错误的是( )
| A.60℃时,AgBrO3,饱和溶液的浓度是0.596% |
| B.温度升高时AgBrO3,和KNO3溶解速度都加快 |
| C.温度对AgBrO3,溶解度的影响比对KNO3溶解度的影响大 |
| D.KNO3中少量AgBrO3可用重结晶的方法除去 |
更新时间:2019-11-08 13:02:04
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】根据如图所示溶解度曲线判断,下列说法正确的是( )
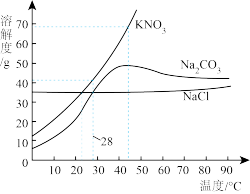

| A.28℃时,将40 g KNO3溶于100 g水得到饱和溶液 |
| B.将43℃的Na2CO3饱和溶液升高10℃,有晶体析出 |
| C.三种物质的饱和溶液由40℃降温至23℃,所得溶液中溶质质量:m(NaCl)=m(KNO3)>m(Na2CO3) |
| D.除去KNO3中混有的Na2CO3,可在40℃配成饱和溶液,再降温结晶、过滤 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】某些盐在溶液中结晶时,析出的晶体是结晶水合物.下表记录了t℃时向4份相同的硫酸铜溶液中加入的无水硫酸铜的质量以及析出硫酸铜晶体(CuSO4 •5H2O)的质量的实验数据:当4.6g无水硫酸铜时,析出硫酸铜晶体的质量为( )
| 硫酸铜溶液 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
| 加入的无水硫酸铜(g) | 2.5 | 4.0 | 6.0 | 8.0 |
| 析出的硫酸铜晶体(g) | 0.10 | 2.8 | 6.4 | 10.0 |
| A.2.56g | B.3.42g | C.3.88g | D.6.82g |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】在二氧化碳的水溶液中存在着如下平衡: CO2(g) CO2(aq)CO2(aq)+H2O
CO2(aq)CO2(aq)+H2O H2CO3(aq) H2CO3(aq)
H2CO3(aq) H2CO3(aq) H+(aq)+HCO3-(aq)HCO3-(aq)
H+(aq)+HCO3-(aq)HCO3-(aq)  H+(aq)+CO32-(aq)
H+(aq)+CO32-(aq)
下列有关说法正确的是( )
 CO2(aq)CO2(aq)+H2O
CO2(aq)CO2(aq)+H2O H2CO3(aq) H2CO3(aq)
H2CO3(aq) H2CO3(aq) H+(aq)+HCO3-(aq)HCO3-(aq)
H+(aq)+HCO3-(aq)HCO3-(aq)  H+(aq)+CO32-(aq)
H+(aq)+CO32-(aq) 下列有关说法正确的是( )
| A.水中溶解的二氧化碳的浓度,夏天时比冬天时高 |
| B.如果海水略呈碱性,海水中二氧化碳的浓度比纯水高 |
| C.气压升高,水中c(HCO3-)增大 |
| D.常温下,二氧化碳的水溶液中,由水电离出的c(H+)与c(OH-)的乘积等于1×l0-14 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】在一定温度下的氢氧化钙的悬浊液中,加入少量的氧化钙粉末,充分反应后恢复到原温度。下列叙述不正确的是
| A.溶液的pH不变 | B.溶液中钙离子数目减少 |
| C.溶液中钙离子浓度不变 | D.氢氧化钙的溶度积常数变小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
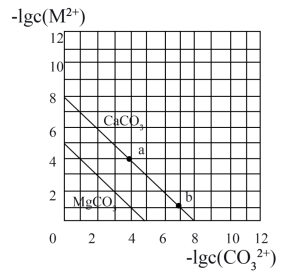
【推荐2】某温度下,两种碳酸盐 (M:
(M: 、
、 )饱和溶液中
)饱和溶液中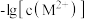 与
与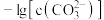 的关系如图所示。下列说法不正确的是
的关系如图所示。下列说法不正确的是
 (M:
(M: 、
、 )饱和溶液中
)饱和溶液中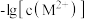 与
与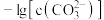 的关系如图所示。下列说法不正确的是
的关系如图所示。下列说法不正确的是
A.该温度下, 的 的 |
B.该温度下,溶解度: |
C.加入适量 固体可使溶液由a点变到b点 固体可使溶液由a点变到b点 |
D. 的平衡常数K=10-3 的平衡常数K=10-3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】一定温度下,向含Cu2+、Mn2+、Fe2+、Zn2+四种金属离子(M2+)的溶液中滴加Na2S溶液,生成硫化物沉淀所需S2−浓度的对数值lg c(S2-)与lg c(M2+)的关系如图所示。下列判断错误的是


| A.图中四条直线的斜率都是−1 |
| B.Ksp(FeS)=1.0×10−20 |
| C.向含等物质的量浓度的Mn2+、Zn2+稀溶液中滴加Na2S溶液,Mn2+先沉淀 |
| D.每条直线的上方都是该硫化物的沉淀区,每条直线的下方都是该硫化物沉淀的溶解区 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】室温下进行下列实验,根据实验操作和现象所得到的结论错误的是
| 选项 | 实验操作和现象 | 实验结论 |
| A | 向某溶液中滴加Ba(NO3)2溶液和盐酸,产生白色沉淀 | 不能确定原溶液一定含有 |
| B | 向盛有等物质的量浓度的NaI和NaCl的混合溶液中滴加AgNO3溶液,先出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| C | 蔗糖与浓硫酸反应所得刺激性气体使溴水和品红溶液颜色变为无色 | SO2具有还原性和漂白性 |
| D | 用pH计测得浓度均为0.01mol/L的NaX溶液和Na2CO3溶液的pH依次为10.9、11.1 | HX的酸性比碳酸酸性强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】根据下列实验操作和现象所得出的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 相同条件下,分别测量0.1mol·L-1和0.01mol·L-1醋酸溶液的导电性,前者的导电性强 | 醋酸浓度越大,电离程度越大 |
| B | 常温下,分别测定浓度均为0.1 mol·L-1 NaF和NaClO溶液的pH,后者的pH大 | 酸性:HF<HClO |
| C | 向 H2O2溶液中滴加 H2O2溶液中滴加 KMnO4溶液,溶液褪色 KMnO4溶液,溶液褪色 | H2O2具有还原性 |
| D | 向2mL 0.1 mol·L-1AgNO3溶液中,先滴加3滴0.1 mol·L-1NaCl溶液,有白色沉淀生成,再滴加5滴0.1 mol·L-1KI溶液,出现黄色沉淀 | Ksp(AgI)<Ksp(AgCl) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】某温度时,Ksp(CuS)=10-35,Ksp(ZnS)=2.5×10-22,Ksp(MnS)=2.5×10-13,KSP[Zn(OH)2]=5×10-17.下列说法正确的是
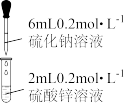
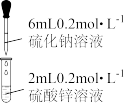
| A.向CuS悬浊液中加入少量水,沉淀溶解平衡向溶解的方向移动,c(S2-)增大 |
| B.可用MnS除去MnCl2溶液中混有的少量杂质ZnCl2 |
| C.分析以上数据可知,反应ZnS+2H2O=Zn(OH)2+H2S↑可以发生 |
| D.如图所示,向反应后的混合溶液中滴加少量的硫酸铜溶液,白色沉淀转变成黑色沉淀,证明Ksp(CuS)<Ksp(ZnS) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列实验方案能达到实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 比较KSP(BaCO3)<KSP(BaSO4) | 向BaSO4悬浊液中加入饱和Na2CO3溶液,充分搅拌,静置,过滤,洗涤。向滤渣中加入盐酸有气泡产生 |
| B | 配制480mL0.2mol·L-1CuSO4溶液 | 将24gCuSO4·5H2O溶于蒸馏水配成500mL溶液 |
| C | 比较非金属性强弱:C1>C | 向一定浓度的NaHCO3溶液中滴加稀盐酸,将产生的气体通入澄清石灰水 |
| D | 验证Na2SO3是否变质 | 向NaSO3溶液中滴入足量盐酸至不再产生气体,然后滴入BaCl2溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次


 、
、 、
、 、
、
 的溶液:
的溶液: 、
、 、
、 、
、
 、
、 、
、 、
、 、
、


