名校
解题方法
1 . I.钴的配合物制取
实验室以活性炭为催化剂,用CoCl2制取[Co(NH3)6]Cl3,装置如图所示。

(1)仪器a的名称是___________ ;仪器b中的试剂是___________ ;冷凝管作用是___________ 。
II.将0.1 mol/L CoCl2、NH4Cl混合液在三颈烧瓶中混合,滴加浓氨水,溶液变为棕色。已知:①[Co(NH3)6]2+具有较强还原性;溶液呈棕色。②Ksp[Co(OH)2] = 6×10-15
(2)请计算常温下该混合液中Co2+开始沉淀的pH值(精确到0.01),列出必要过程________ 。NH4Cl的作用是___________ 。
(3)充分反应后缓慢滴加双氧水,水浴加热20 min(该过程生成OH-)。发生反应的离子方程式为___________ 。将反应后的混合液冷却后加入适量浓盐酸,过滤、洗涤、干燥,得到[Co(NH3)6]Cl3晶体。
III.已知[Co(NH3)6]Cl3可溶于热水,微溶于冷水,难溶于乙醇。
(4)请运用平衡移动原理解释加入浓盐酸的目的是_____________ 。
(5)[Co(NH3)6]3+ Co3+ + 6NH3 K1;
Co3+ + 6NH3 K1;
 NH3 + H+ K2,判断K1
NH3 + H+ K2,判断K1____ (K2)6。(填“>”“<”或“=”)
(6)洗涤[Co(NH3)6]Cl3时可用___________。
IV.测定产品中配体NH3与外界Cl-的物质的量之比。实验如下:
①蒸氨:取0.100 g样品加入三颈烧瓶中,再加入足量NaOH溶液并充分加热,蒸出的气体全部通入V1 mL c1 mol/L的H2SO4中。
②滴定:用c2 mol/L NaOH溶液滴定①中溶液,消耗V2 mL NaOH溶液。
③沉淀:另取0.100 g样品溶解,加入足量AgNO3溶液,过滤、洗涤、干燥、恒重,得到沉淀m3 g。(MAgCl = 143.5 g/mol)
(7)滴定时选用的指示剂为___________ 。
(8)测得产品中配体NH3与外界Cl-的物质的量比值为________ 。(用含c1、V1等数据的代数式表示)若测得n(NH3) : n(Cl-)比值偏小,可能的原因是________ 。
A.蒸氨结束时,未用蒸馏水洗涤冷凝管,并将洗涤液一并倒入H2SO4中
B.滴定步骤的NaOH溶液使用前敞口放置于空气中一段时间
C.滴定步骤中盛放NaOH溶液的滴定管未用NaOH溶液润洗
D.沉淀步骤中,沉淀未完全转移至漏斗中
实验室以活性炭为催化剂,用CoCl2制取[Co(NH3)6]Cl3,装置如图所示。

(1)仪器a的名称是
II.将0.1 mol/L CoCl2、NH4Cl混合液在三颈烧瓶中混合,滴加浓氨水,溶液变为棕色。已知:①[Co(NH3)6]2+具有较强还原性;溶液呈棕色。②Ksp[Co(OH)2] = 6×10-15
(2)请计算常温下该混合液中Co2+开始沉淀的pH值(精确到0.01),列出必要过程
(3)充分反应后缓慢滴加双氧水,水浴加热20 min(该过程生成OH-)。发生反应的离子方程式为
III.已知[Co(NH3)6]Cl3可溶于热水,微溶于冷水,难溶于乙醇。
(4)请运用平衡移动原理解释加入浓盐酸的目的是
(5)[Co(NH3)6]3+
 Co3+ + 6NH3 K1;
Co3+ + 6NH3 K1;
 NH3 + H+ K2,判断K1
NH3 + H+ K2,判断K1(6)洗涤[Co(NH3)6]Cl3时可用___________。
| A.蒸馏水 | B.冰水 | C.无水乙醇 | D.50%乙醇水溶液 |
IV.测定产品中配体NH3与外界Cl-的物质的量之比。实验如下:
①蒸氨:取0.100 g样品加入三颈烧瓶中,再加入足量NaOH溶液并充分加热,蒸出的气体全部通入V1 mL c1 mol/L的H2SO4中。
②滴定:用c2 mol/L NaOH溶液滴定①中溶液,消耗V2 mL NaOH溶液。
③沉淀:另取0.100 g样品溶解,加入足量AgNO3溶液,过滤、洗涤、干燥、恒重,得到沉淀m3 g。(MAgCl = 143.5 g/mol)
(7)滴定时选用的指示剂为
(8)测得产品中配体NH3与外界Cl-的物质的量比值为
A.蒸氨结束时,未用蒸馏水洗涤冷凝管,并将洗涤液一并倒入H2SO4中
B.滴定步骤的NaOH溶液使用前敞口放置于空气中一段时间
C.滴定步骤中盛放NaOH溶液的滴定管未用NaOH溶液润洗
D.沉淀步骤中,沉淀未完全转移至漏斗中
您最近一年使用:0次
名校
2 . 25℃时,用 沉淀
沉淀 、
、 两种金属离子(
两种金属离子( ),所需
),所需 最低浓度的对数值
最低浓度的对数值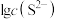 与
与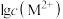 的关系如图所示,请回答:
的关系如图所示,请回答:

(1)25℃时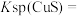
___________ 。
(2)25℃时向50mL的 、
、 浓度均为0.01mol/L的混合溶液中逐滴加入
浓度均为0.01mol/L的混合溶液中逐滴加入 溶液,当
溶液,当 溶液加到150mL时开始生成SnS沉淀,则此时溶液中
溶液加到150mL时开始生成SnS沉淀,则此时溶液中 浓度为
浓度为___________ mol/L。
 沉淀
沉淀 、
、 两种金属离子(
两种金属离子( ),所需
),所需 最低浓度的对数值
最低浓度的对数值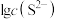 与
与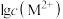 的关系如图所示,请回答:
的关系如图所示,请回答:
(1)25℃时
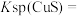
(2)25℃时向50mL的
 、
、 浓度均为0.01mol/L的混合溶液中逐滴加入
浓度均为0.01mol/L的混合溶液中逐滴加入 溶液,当
溶液,当 溶液加到150mL时开始生成SnS沉淀,则此时溶液中
溶液加到150mL时开始生成SnS沉淀,则此时溶液中 浓度为
浓度为
您最近一年使用:0次
3 . 工业产生的废气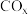 、
、 、
、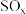 对环境有害,若能合理的利用吸收,可以减少污染,变废为宝。
对环境有害,若能合理的利用吸收,可以减少污染,变废为宝。
(1)光气 是一种重要的化工原料,用于农药、医药、聚酯类材料的生产,工业上通过
是一种重要的化工原料,用于农药、医药、聚酯类材料的生产,工业上通过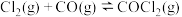 制备。图1为此反应的反应速率随温度变化的曲线,图2为某次模拟实验研究过程中容器内各物质的浓度随时间变化的曲线。回答下列问题:
制备。图1为此反应的反应速率随温度变化的曲线,图2为某次模拟实验研究过程中容器内各物质的浓度随时间变化的曲线。回答下列问题:
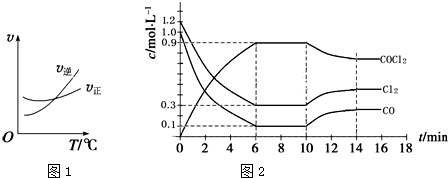
①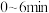 内,反应的平均速率
内,反应的平均速率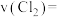
________ ;
② 改变的条件是
改变的条件是________ ,该反应平衡常数变化的趋势是________ (填“增大”、“减小”或“不变”)。
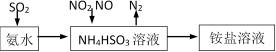
(2)利用氨水可以将 和
和 吸收,原理如下图所示:
吸收,原理如下图所示: 被吸收的离子方程式为
被吸收的离子方程式为________ 。
(3) 在自然界循环时可与
在自然界循环时可与 反应,
反应, 难溶于水,可溶于盐酸,请用平衡移动原理解释
难溶于水,可溶于盐酸,请用平衡移动原理解释 可溶于盐酸的原因
可溶于盐酸的原因________ 。
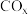 、
、 、
、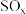 对环境有害,若能合理的利用吸收,可以减少污染,变废为宝。
对环境有害,若能合理的利用吸收,可以减少污染,变废为宝。(1)光气
 是一种重要的化工原料,用于农药、医药、聚酯类材料的生产,工业上通过
是一种重要的化工原料,用于农药、医药、聚酯类材料的生产,工业上通过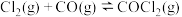 制备。图1为此反应的反应速率随温度变化的曲线,图2为某次模拟实验研究过程中容器内各物质的浓度随时间变化的曲线。回答下列问题:
制备。图1为此反应的反应速率随温度变化的曲线,图2为某次模拟实验研究过程中容器内各物质的浓度随时间变化的曲线。回答下列问题:
①
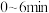 内,反应的平均速率
内,反应的平均速率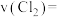
②
 改变的条件是
改变的条件是(2)利用氨水可以将
 和
和 吸收,原理如下图所示:
吸收,原理如下图所示: 被吸收的离子方程式为
被吸收的离子方程式为
(3)
 在自然界循环时可与
在自然界循环时可与 反应,
反应, 难溶于水,可溶于盐酸,请用平衡移动原理解释
难溶于水,可溶于盐酸,请用平衡移动原理解释 可溶于盐酸的原因
可溶于盐酸的原因
您最近一年使用:0次



