名校
解题方法
1 . 现有25℃时0.1mol•L-1的氨水,请回答以下问题:
(1)氨水呈碱性的原因为(用离子方程式表示)___ 。
(2)若向氨水中加入稀盐酸,使其恰好中和,写出反应的离子方程式___ ;若所得溶液的pH=5,则溶液中水所电离出的氢离子浓度为___ 。
(3)若向氨水中加入少量硫酸铵固体,此时溶液中
__ (填“增大”、“减小”或“不变”)。
(4)若向氨水中加入稀硫酸至溶液的pH=7,此时c(NH4+)=amol•L-1,则c(SO42-)=__ 。
(5)若向氨水中加入pH=1的硫酸,且氨水与硫酸的体积比为1∶1,则所得溶液中各离子的物质的量浓度由大到小的顺序是___ 。
(6)二氧化硫通入0.1mol/L的氯化钡溶液中至饱和,无现象,若继续加入氨水,产生白色沉淀,用电离平衡解释原因___ 。
(1)氨水呈碱性的原因为(用离子方程式表示)
(2)若向氨水中加入稀盐酸,使其恰好中和,写出反应的离子方程式
(3)若向氨水中加入少量硫酸铵固体,此时溶液中

(4)若向氨水中加入稀硫酸至溶液的pH=7,此时c(NH4+)=amol•L-1,则c(SO42-)=
(5)若向氨水中加入pH=1的硫酸,且氨水与硫酸的体积比为1∶1,则所得溶液中各离子的物质的量浓度由大到小的顺序是
(6)二氧化硫通入0.1mol/L的氯化钡溶液中至饱和,无现象,若继续加入氨水,产生白色沉淀,用电离平衡解释原因
您最近一年使用:0次
2 . 某温度下,硫酸钡与水组成的混合物中,存在下列过程:BaSO4(s)⇌Ba2++SO42﹣,向其中加入少量硫酸钠固体,下列说法错误的是( )
| A.BaSO4的电离程度减小 |
| B.BaSO4溶解的量减小 |
| C.c(Ba2+)与c(SO42﹣)的乘积增大 |
| D.溶液的导电能力增强 |
您最近一年使用:0次
3 . 在盛有硫酸铜饱和溶液的烧杯中,投入一块不规则的硫酸铜晶体,隔一段时间后,得到的结论是( )
| A.晶体部分溶解了 | B.晶体的形状和质量不变 |
| C.晶体的质量增加了,形状也发生了改变 | D.晶体的质量不变,形状改变了 |
您最近一年使用:0次
2019-11-07更新
|
107次组卷
|
2卷引用:上海市浦东新区2016-2017学年高一上学期期末考试化学试题
16-17高三上·江苏南通·阶段练习
名校
4 . 下列图示与对应的叙述相符的是
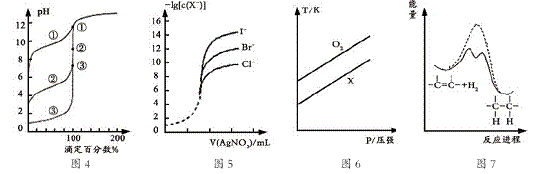

| A.用0.1000mol/L NaOH溶液分别滴定浓度相同的三种一元酸,由图4曲线确定①的酸性最强 |
| B.用0.0100mol/L硝酸银标准溶液,滴定浓度均为0.1000mol/L Cl-、Br-及I-的混合溶液,由图5曲线,可确定首先沉淀的是Cl- |
| C.在体积相同的两个密闭容器中,分别充入相同质量O2和X气体,由图6可确定X可能是CH4气体 |
| D.由图7可说明烯烃与H2加成反应是放热反应,虚线表示在有催化剂的条件下进行 |
您最近一年使用:0次
2016-12-09更新
|
337次组卷
|
4卷引用:上海建平高级中学 2012-2013学年高三下学期模拟化学试题
(已下线)上海建平高级中学 2012-2013学年高三下学期模拟化学试题2017届江苏省通州高级中学高三上第一次测试化学试卷2017届四川省绵阳市东辰国际学校高三上学期第四次月考理科综合化学试卷备考突破2020高三化学专题强化集训——酸碱中和滴定及其拓展
真题
名校
5 . 向饱和澄清石灰水中加入少量CaC2,充分反应后恢复到原来的温度,所得溶液中
| A.c(Ca2+)、c(OH-)均增大 | B.c(Ca2+)、c(OH-)均保持不变 |
| C.c(Ca2+)、c(OH-)均减小 | D.c(OH-)增大、c(H+)减小 |
您最近一年使用:0次
2016-12-09更新
|
1802次组卷
|
4卷引用:上海市实验学校2021-2022学年高三下学期4月月考化学试题
上海市实验学校2021-2022学年高三下学期4月月考化学试题2014年全国普通高等学校招生统一考试理科综合能力测试化学(上海卷)上海市虹口区2016届高三12月第二次分层练习化学试题(已下线)上海市宝山区行知中学2015届高三上学期第一次月考化学试题



