I.请回答。
(1)按照有机物的命名规则,下列命名正确的是___________ 。
A.3-乙基己烷 B.2-乙基戊烷, C.1,2-二甲基丁烷 D.4-甲基戊烷
写出该物质的结构简式:___________ 。
Ⅱ.如图所示,U形管的左端用橡胶塞封闭,充有甲烷和氯气(体积比为1:4)的混合气体,假定氯气在水中的溶解可以忽略不计。将封闭有甲烷和氯气混合气体的装置放置在有漫射光的地方让混合气体缓慢反应一段时间。
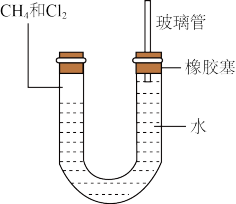
(2)经过几个小时的反应,U形管右端的水面变化是___________ (A升高;B降低;C不变);右端玻璃管的作用是___________ 。
(3)若水中含有Na2SiO3,则在U形管左端会观察到现象是___________ ;若水中含有AgNO3,则水中反应离子方程式___________ 。
(4)若题目中甲烷与氯气的体积比为1:1,则得到的产物为___________(填字母)。
(5)若把1体积CH4和4体积Cl2组成的混合气体充入大试管中,将此试管倒立在盛有饱和食盐水的水槽里,放在光亮处,试推测可观察到的现象是___________ 。
①黄绿色逐渐消失 ②试管壁上有黄色油珠出现
③水位在试管内上升到一定高度 ④水槽内有少量晶体析出
⑤液面上有白雾
(1)按照有机物的命名规则,下列命名正确的是
A.3-乙基己烷 B.2-乙基戊烷, C.1,2-二甲基丁烷 D.4-甲基戊烷
写出该物质的结构简式:
Ⅱ.如图所示,U形管的左端用橡胶塞封闭,充有甲烷和氯气(体积比为1:4)的混合气体,假定氯气在水中的溶解可以忽略不计。将封闭有甲烷和氯气混合气体的装置放置在有漫射光的地方让混合气体缓慢反应一段时间。

(2)经过几个小时的反应,U形管右端的水面变化是
(3)若水中含有Na2SiO3,则在U形管左端会观察到现象是
(4)若题目中甲烷与氯气的体积比为1:1,则得到的产物为___________(填字母)。
| A.CH3Cl、HCl | B.CCl4、HCl |
| C.CH3Cl、CH2Cl2 | D.CH3Cl、CH2Cl2、CHCl3、CCl4、HCl |
(5)若把1体积CH4和4体积Cl2组成的混合气体充入大试管中,将此试管倒立在盛有饱和食盐水的水槽里,放在光亮处,试推测可观察到的现象是
①黄绿色逐渐消失 ②试管壁上有黄色油珠出现
③水位在试管内上升到一定高度 ④水槽内有少量晶体析出
⑤液面上有白雾
更新时间:2024-02-20 20:50:45
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】完成下列情况下的离子方程式。
(1) 与醋酸反应:
与醋酸反应:___________ 。
(2)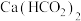 溶液与过量
溶液与过量 溶液反应
溶液反应_____ 。
(3)向 中加入盐酸:
中加入盐酸:___________ 。
(4)氯化铁溶液跟过量氨水反应:___________ 。
(5)向 溶液中逐滴加入
溶液中逐滴加入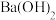 溶液至中性:
溶液至中性:___________ 。
(1)
 与醋酸反应:
与醋酸反应:(2)
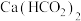 溶液与过量
溶液与过量 溶液反应
溶液反应(3)向
 中加入盐酸:
中加入盐酸:(4)氯化铁溶液跟过量氨水反应:
(5)向
 溶液中逐滴加入
溶液中逐滴加入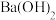 溶液至中性:
溶液至中性:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】化合物A(仅含三种元素,摩尔质量为198g·mol-1)具有高效的消毒作用,是一种新型非氮高效消毒剂。为探究化合物A的组成与性质,设计并完成以下实验:取3. 96g化合物A溶于水中,一段时间后全部转化为B(红褐色沉淀)、C(一种碱)和气体单质D(可使带火星的木条复燃),向溶液中加入100mL 0.6mol/L稀硫酸,再加入含有0.08mol KOH的溶液,恰好完全反应。过滤,将沉淀洗涤后充分灼烧,得到红棕色固体粉末1.60g。将所得溶液在一定条件下蒸发可得到一种纯净的不含结晶水的盐。
(1)化合物A所含有的元素:_______________ (用元素符号表示)。
(2)化合物A与H2O反应的离子方程式:__________________ 。
(3)化合物A可由FeCl3和KClO在强碱性条件下制得,其反应的离子方程式:_________________ 。
(1)化合物A所含有的元素:
(2)化合物A与H2O反应的离子方程式:
(3)化合物A可由FeCl3和KClO在强碱性条件下制得,其反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】已知0.1mol·L-1的NaHSO4溶液中H+浓度为0.1mol·L-1,请回答下列问题:
(1)写出NaHSO4在水溶液中的电离方程式:___________________ ;
(2)NaHSO4属于“酸”、“碱”、“盐”中的____________ ,理由是____________________ ;
(3)①若将NaHSO4与Ba(OH)2在溶液中按照物质的量之比为2∶1混合,反应的化学方程式为______________________ ;
②若将NaHSO4与Ba(OH)2在溶液中按照物质的量之比为1∶1混合,化学方程式为___________________________ 。
(1)写出NaHSO4在水溶液中的电离方程式:
(2)NaHSO4属于“酸”、“碱”、“盐”中的
(3)①若将NaHSO4与Ba(OH)2在溶液中按照物质的量之比为2∶1混合,反应的化学方程式为
②若将NaHSO4与Ba(OH)2在溶液中按照物质的量之比为1∶1混合,化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】纯碱工业是基本无机化工之一。完成下列填空:
(1)常温下向纯碱溶液中滴加酚酞试液,溶液变红,原因是___ (用离子方程式表示);继续滴加足量氯化钡溶液,可以看到__ 。
(2)最早的勒布朗法制碱涉及如下反应:Na2SO4+2C+CaCO3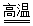 Na2CO3+CaS+2CO2↑。该反应中被还原的元素是
Na2CO3+CaS+2CO2↑。该反应中被还原的元素是___ 。若转移6.02×1024个电子,生成CO2在标准状况下的体积为__ L。
(3)索尔维法(氨碱法)是工业生产纯碱的主要方法,其主要原理可以表示为:NaCl(饱和)+H2O+CO2+NH3=NaHCO3↓+NH4Cl。该反应涉及的各物质中,属于弱电解质的是___ 。综合平衡理论解释通入CO2和NH3后为何会有NaHCO3析出___ 。
(4)侯德榜对索尔维法进行了改进,利用平衡移动原理从析出NaHCO3后的母液中提取NH4Cl产品,所需的物质有___ (填化学式)。
(5)纯碱厂在生产过程中要时刻关注设备的腐蚀情况。输送饱和食盐水的铸铁管道受到腐蚀时,正极的电极反应方程式为:___ 。为缓解腐蚀,可在铸铁管道上固定铝-锌-镉三元合金,该方法称为___ 。
(1)常温下向纯碱溶液中滴加酚酞试液,溶液变红,原因是
(2)最早的勒布朗法制碱涉及如下反应:Na2SO4+2C+CaCO3
 Na2CO3+CaS+2CO2↑。该反应中被还原的元素是
Na2CO3+CaS+2CO2↑。该反应中被还原的元素是(3)索尔维法(氨碱法)是工业生产纯碱的主要方法,其主要原理可以表示为:NaCl(饱和)+H2O+CO2+NH3=NaHCO3↓+NH4Cl。该反应涉及的各物质中,属于弱电解质的是
(4)侯德榜对索尔维法进行了改进,利用平衡移动原理从析出NaHCO3后的母液中提取NH4Cl产品,所需的物质有
(5)纯碱厂在生产过程中要时刻关注设备的腐蚀情况。输送饱和食盐水的铸铁管道受到腐蚀时,正极的电极反应方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】利用所学化学反应原理,解决以下问题:
(1)KAl(SO4)2·12H2O可做净水剂,其原理是____________________________________ (用离子方程式表示)
(2)碳酸氢钠溶液蒸干并灼烧得到的固体物质是__________ (填化学式)。
(3)向FeCl3溶液中滴加NaHCO3溶液,有沉淀和气体生成的离子方程式_____________ 。
(4)将AgCl分别放入①5 mL H2O ②10 mL 0.2 mol·L-1 MgCl2溶液 ③20 mL 0.5 mol·L-1 NaCl溶液④40 mL 0.1 mol·L-1 HCl溶液中溶解至饱和,各溶液中Ag+的浓度由大到小的顺序是______ (用序号填空)。
(5)常温下a mol/L CH3COOH稀溶液和b mol/L KOH稀溶液等体积混合:若c(K+)<c (CH3COO-),则a_____________ b(填>、<、=)。
(6)室温下,1 mol/L相同体积的下列四种溶液:①KCl②FeCl3③HF④Na2CO3中,所含阳离子数由少到多的顺序是_________________________ (用序号填空)。
(1)KAl(SO4)2·12H2O可做净水剂,其原理是
(2)碳酸氢钠溶液蒸干并灼烧得到的固体物质是
(3)向FeCl3溶液中滴加NaHCO3溶液,有沉淀和气体生成的离子方程式
(4)将AgCl分别放入①5 mL H2O ②10 mL 0.2 mol·L-1 MgCl2溶液 ③20 mL 0.5 mol·L-1 NaCl溶液④40 mL 0.1 mol·L-1 HCl溶液中溶解至饱和,各溶液中Ag+的浓度由大到小的顺序是
(5)常温下a mol/L CH3COOH稀溶液和b mol/L KOH稀溶液等体积混合:若c(K+)<c (CH3COO-),则a
(6)室温下,1 mol/L相同体积的下列四种溶液:①KCl②FeCl3③HF④Na2CO3中,所含阳离子数由少到多的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题:
(1)有下列几组物质,请将序号填入下列空格内:
A.CH2=CH-COOH和油酸(C17H33COOH) B.12C60和石墨 C.乙醇和乙二醇 D.35Cl和37Cl E.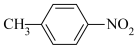 和
和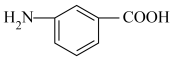
①互为同位素的是______ 。
②互为同分异构体的是______ 。
③互为同素异形体的是______ 。
④互为同系物的是______ 。
(2)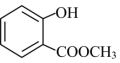 中含有的官能团的名称为
中含有的官能团的名称为______ 。
(3)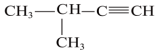 的系统命名是
的系统命名是______ 。
(4)有机物(CH3)3CCH2CH(C2H5)CH3系统命名为______ 。
(5)写出丙烯一定条件下发生加成聚合的反应方程式______ 。
(1)有下列几组物质,请将序号填入下列空格内:
A.CH2=CH-COOH和油酸(C17H33COOH) B.12C60和石墨 C.乙醇和乙二醇 D.35Cl和37Cl E.
 和
和
①互为同位素的是
②互为同分异构体的是
③互为同素异形体的是
④互为同系物的是
(2)
 中含有的官能团的名称为
中含有的官能团的名称为(3)
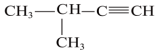 的系统命名是
的系统命名是(4)有机物(CH3)3CCH2CH(C2H5)CH3系统命名为
(5)写出丙烯一定条件下发生加成聚合的反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】有机物是生命产生的物质基础,所有的生命体都含有机化合物。有机化合物不仅与人类的衣、食、住、行密切相关,而且还是揭示生命现象及其规律的钥匙。
(1)下列物质属于有机物的是______ (填编号)。
①乙醇;②食盐;③石墨;④甲烷;⑤蔗糖:⑥水;⑦一氧化碳;⑧碳酸钙;⑨乙酸钠;⑩碳酸。
(2)有机物分子中的碳原子与其他原子的结合方式是______ (单选)。
(3)一款环保汽车使用的燃料是压缩甲烷气体。下列有关甲烷的叙述正确的是______ (单选)。
(4)现有新戊烷、异丁烷、异戊烷、正丁烷四种烷烃,沸点由高到低的顺序为______ (用结构简式表示)。
(5)随着碳原子数目的增加,普通命名已不能满足需求。下列烷烃的系统命名正确的是______ (单选)。
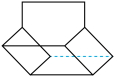
(6)如图为篮烷的键线式,则篮烷的分子式为______ ,篮烷______ (填“是”或“不是”)烷烃。假设篮烷分子中键角只有135°、90°两种,则它的一氯代物有______ 种(不考虑立体异构)。
(7)某烷烃蒸气的密度是相同状况下氢气密度的64倍,且不可能是烯烃与氢气加成的产物,该烷烃的结构简式为______ 。
(8)由两种气态链烃(其中一种是烷烃)组成的混合气体20mL,在足量的O2中燃烧。恢复到室温后,混合气体体积减少了35mL,再将剩余气体通过碱石灰吸收,体积又减少40mL。则混合气体的组成为______ 。
(1)下列物质属于有机物的是
①乙醇;②食盐;③石墨;④甲烷;⑤蔗糖:⑥水;⑦一氧化碳;⑧碳酸钙;⑨乙酸钠;⑩碳酸。
(2)有机物分子中的碳原子与其他原子的结合方式是
| A.只形成π键 | B.只形成非极性键 |
| C.一定形成四对共用电子对 | D.形成离子键和共价键 |
| A.甲烷点燃前必须验纯 |
| B.甲烷分子的空间构型是正四面体,所以CH2Cl2也是正四面体 |
| C.甲烷很稳定,不能分解 |
| D.甲烷可以与氯气发生取代反应,因此可以使氯水褪色 |
(5)随着碳原子数目的增加,普通命名已不能满足需求。下列烷烃的系统命名正确的是
| A.5-甲基-4-乙基己烷 | B.2,4,4-三甲基-3-乙基戊烷 |
| C.2,2,3-三甲基丁烷 | D.3,3-二甲基-4-乙基戊烷 |

(7)某烷烃蒸气的密度是相同状况下氢气密度的64倍,且不可能是烯烃与氢气加成的产物,该烷烃的结构简式为
(8)由两种气态链烃(其中一种是烷烃)组成的混合气体20mL,在足量的O2中燃烧。恢复到室温后,混合气体体积减少了35mL,再将剩余气体通过碱石灰吸收,体积又减少40mL。则混合气体的组成为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)按系统命名法填写下面有机物的名称: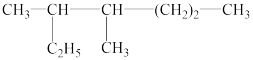
_________________
(2)2,6-二甲基-4-乙基辛烷的结构简式是______________________ ,1 mol该烃完全燃烧需消耗氧气________ mol。
(3)在烃的分子结构中,若每减少2个氢原子,则相当于碳碳间增加1对共用电子对。试完成下列问题:
①分子式为CnH2n+2的烃分子中碳碳间共用电子对数为________ 。
②符合该条件的单烯烃的分子式为________ 。
(4)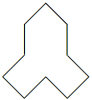 分子式为
分子式为________ ,按碳的骨架分,该有机物属于________ 。(填字母序号)
a. 环状化合物 b. 脂环烃 c. 芳香化合物 d. 苯的同系物
(5)2,2-二甲基丙烷的习惯命名为________ 。
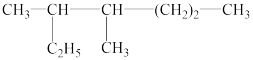
(2)2,6-二甲基-4-乙基辛烷的结构简式是
(3)在烃的分子结构中,若每减少2个氢原子,则相当于碳碳间增加1对共用电子对。试完成下列问题:
①分子式为CnH2n+2的烃分子中碳碳间共用电子对数为
②符合该条件的单烯烃的分子式为
(4)
 分子式为
分子式为a. 环状化合物 b. 脂环烃 c. 芳香化合物 d. 苯的同系物
(5)2,2-二甲基丙烷的习惯命名为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】下列各图均能表示甲烷的分子结构,按要求回答下列问题。
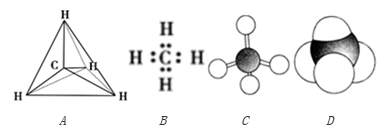
(1)甲烷的比例模型是________ ,甲烷的电子式是__________ (填序号)。
(2)写出甲烷与氯气发生反应的化学方程式_____________ (只写第一步),该反应的反应类型是________________ 。
(3)相对分子质量为100的烷烃的分子式是_______________ 。
(4)甲烷与丙烷互为________ 。
A. 同位素 B. 同素异形体 C. 同系物 D. 同分异构体

(1)甲烷的比例模型是
(2)写出甲烷与氯气发生反应的化学方程式
(3)相对分子质量为100的烷烃的分子式是
(4)甲烷与丙烷互为
A. 同位素 B. 同素异形体 C. 同系物 D. 同分异构体
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】近年来我市政府率先在公交车和出租车中推行用天然气代替汽油作燃料的改革,取得了显著进展。走上街头你会发现不少公交车和出租车上有“CNG”的标志,代表它们是以天然气作为燃气的汽车。试问:
(1)我市政府推广这一改革的主要目的是_______________________________ ;
(2)天然气是植物残体在隔绝空气的条件下,经过微生物的发酵作用而生成的,因此天然气中所贮藏的化学能最终来自于_________________________ ;
(3)写出天然气的主要成分和氯气发生一取代反应的化学方程式___________________
(4)天然气的主要成分是一种很好的燃料。已知4g该主要成分完全燃烧生成CO2气体和液态水时放出222.5kJ的热量,则上述成分燃烧的热化学方程式为___________________ ;
(1)我市政府推广这一改革的主要目的是
(2)天然气是植物残体在隔绝空气的条件下,经过微生物的发酵作用而生成的,因此天然气中所贮藏的化学能最终来自于
(3)写出天然气的主要成分和氯气发生一取代反应的化学方程式
(4)天然气的主要成分是一种很好的燃料。已知4g该主要成分完全燃烧生成CO2气体和液态水时放出222.5kJ的热量,则上述成分燃烧的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】“西气东输”是西部开发的重点工程,这里的“气”是指天然气,其主要成分是甲烷。
(1)甲烷分子具有________________ 结构,其结构式是_________________ 。
(2)通常情况下,甲烷比较稳定,但在特定条件下,甲烷也会发生某些反应,请写出甲烷在光照条件下与氯气反应生成一氯甲烷的化学方程式________________________ ,该反应属于____________ (填反应类型)。
(3)在一定条件下甲烷也可用于燃料电池。如图是甲烷燃料电池的原理示意图:
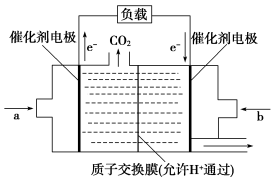
若正极的反应式为O2+4H++4e-=2H2O,则负极反应式为________________________________ ;该电池工作过程中,H+的移动方向为从________ 到________ (填“左”或“右”)。
(1)甲烷分子具有
(2)通常情况下,甲烷比较稳定,但在特定条件下,甲烷也会发生某些反应,请写出甲烷在光照条件下与氯气反应生成一氯甲烷的化学方程式
(3)在一定条件下甲烷也可用于燃料电池。如图是甲烷燃料电池的原理示意图:

若正极的反应式为O2+4H++4e-=2H2O,则负极反应式为
您最近一年使用:0次



