化合物A(仅含三种元素,摩尔质量为198g·mol-1)具有高效的消毒作用,是一种新型非氮高效消毒剂。为探究化合物A的组成与性质,设计并完成以下实验:取3. 96g化合物A溶于水中,一段时间后全部转化为B(红褐色沉淀)、C(一种碱)和气体单质D(可使带火星的木条复燃),向溶液中加入100mL 0.6mol/L稀硫酸,再加入含有0.08mol KOH的溶液,恰好完全反应。过滤,将沉淀洗涤后充分灼烧,得到红棕色固体粉末1.60g。将所得溶液在一定条件下蒸发可得到一种纯净的不含结晶水的盐。
(1)化合物A所含有的元素:_______________ (用元素符号表示)。
(2)化合物A与H2O反应的离子方程式:__________________ 。
(3)化合物A可由FeCl3和KClO在强碱性条件下制得,其反应的离子方程式:_________________ 。
(1)化合物A所含有的元素:
(2)化合物A与H2O反应的离子方程式:
(3)化合物A可由FeCl3和KClO在强碱性条件下制得,其反应的离子方程式:
更新时间:2019-02-05 20:24:38
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至中性,再向上述反应后的中性溶液中继续滴加 溶液,写出此步反应的离子方程式:
溶液,写出此步反应的离子方程式:__________________ 。
 溶液,写出此步反应的离子方程式:
溶液,写出此步反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】完成下列空白处
(1)热的 溶液可用于清洗油污,请用离子方程式解释原因
溶液可用于清洗油污,请用离子方程式解释原因___________ 。
(2)下列三种共价晶体:①金刚石、②晶体硅、③碳化硅,熔点从高到低的顺序是___________ (用序号表示)。
(3)对羟基苯甲醛(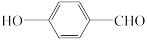 )沸点比邻羟基苯甲醛(
)沸点比邻羟基苯甲醛(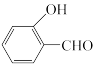 )高的原因是
)高的原因是___________ 。
(4)元素Mn与Fe的部分电离能数据如下表所示:
根据表中数据可知,气态 再失去1个电子比气态
再失去1个电子比气态 再失去1个电子难,其原因是
再失去1个电子难,其原因是___________ 。
(1)热的
 溶液可用于清洗油污,请用离子方程式解释原因
溶液可用于清洗油污,请用离子方程式解释原因(2)下列三种共价晶体:①金刚石、②晶体硅、③碳化硅,熔点从高到低的顺序是
(3)对羟基苯甲醛(
 )沸点比邻羟基苯甲醛(
)沸点比邻羟基苯甲醛( )高的原因是
)高的原因是(4)元素Mn与Fe的部分电离能数据如下表所示:
| 元素 | Mn | Fe | |
电离能/( ) ) |  | 717 | 759 |
 | 1509 | 1561 | |
 | 3248 | 2957 | |
根据表中数据可知,气态
 再失去1个电子比气态
再失去1个电子比气态 再失去1个电子难,其原因是
再失去1个电子难,其原因是
您最近一年使用:0次
【推荐1】高锰酸钾是一种典型的强氧化剂。完成下列填空:
Ⅰ:在用 酸性溶液处理
酸性溶液处理 和CuS的混合物时,发生的反应如下:
和CuS的混合物时,发生的反应如下:
①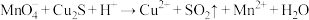 (未配平)
(未配平)
②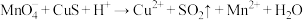 (未配平)
(未配平)
(1)下列关于反应①的说法中错误的是___________ (填字母序号)。
a.被氧化的元素是Cu和S
b.氧化剂与还原剂的物质的量之比为8:5
c.生成2.24L(标况下) ,转移电子的物质的量是0.8mol
,转移电子的物质的量是0.8mol
d.还原性的强弱关系是: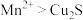
Ⅱ:在稀硫酸中, 与也能发生氧化还原反应。
与也能发生氧化还原反应。
(2)配平 与
与 反应的离子方程式:
反应的离子方程式:___________

(3)欲配制480mL0.1mol/L 溶液,需称取
溶液,需称取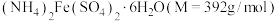 的质量为
的质量为___________ g,需要的玻璃仪器有___________ 。
Ⅲ:实验室可由软锰矿(主要成分为 )制备
)制备 ,方法如下:高温下使软锰矿与过量
,方法如下:高温下使软锰矿与过量 和
和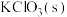 反应,生成
反应,生成 (锰酸钾)和KCl;用水溶解,滤去残渣;酸化滤液,
(锰酸钾)和KCl;用水溶解,滤去残渣;酸化滤液, 转化为
转化为 和
和 ;再滤去沉淀
;再滤去沉淀 ,浓缩结晶得到
,浓缩结晶得到 晶体。请回答:
晶体。请回答:
(4)用软锰矿制备 的化学方程式是:
的化学方程式是:___________ 。
(5) 转化为
转化为 的反应中氧化剂和还原剂的物质的量之比为
的反应中氧化剂和还原剂的物质的量之比为___________ 。
Ⅰ:在用
 酸性溶液处理
酸性溶液处理 和CuS的混合物时,发生的反应如下:
和CuS的混合物时,发生的反应如下:①
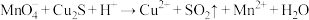 (未配平)
(未配平)②
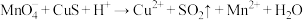 (未配平)
(未配平)(1)下列关于反应①的说法中错误的是
a.被氧化的元素是Cu和S
b.氧化剂与还原剂的物质的量之比为8:5
c.生成2.24L(标况下)
 ,转移电子的物质的量是0.8mol
,转移电子的物质的量是0.8mold.还原性的强弱关系是:
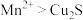
Ⅱ:在稀硫酸中,
 与也能发生氧化还原反应。
与也能发生氧化还原反应。(2)配平
 与
与 反应的离子方程式:
反应的离子方程式:
(3)欲配制480mL0.1mol/L
 溶液,需称取
溶液,需称取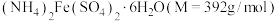 的质量为
的质量为Ⅲ:实验室可由软锰矿(主要成分为
 )制备
)制备 ,方法如下:高温下使软锰矿与过量
,方法如下:高温下使软锰矿与过量 和
和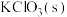 反应,生成
反应,生成 (锰酸钾)和KCl;用水溶解,滤去残渣;酸化滤液,
(锰酸钾)和KCl;用水溶解,滤去残渣;酸化滤液, 转化为
转化为 和
和 ;再滤去沉淀
;再滤去沉淀 ,浓缩结晶得到
,浓缩结晶得到 晶体。请回答:
晶体。请回答:(4)用软锰矿制备
 的化学方程式是:
的化学方程式是:(5)
 转化为
转化为 的反应中氧化剂和还原剂的物质的量之比为
的反应中氧化剂和还原剂的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】氮元素在地球上含量丰富,是构成生命体的基本元素之一、回答下列问题:
(1)N元素在元素周期表中的位置为_______ 。
(2)制备下列物质属于固氮的是 _______。
(3)受到阳光照射浓硝酸会变黄的原因是 _______ ( 用化学方程式表示)。
(4)近几年来关于氮污染的治理倍受关注,根据氮的性质回答以下问题;
①氮的氧化物是空气的主要污染物,下列环境问题与氮的氧化物排放有关的是_______ 。
A.酸雨 B.光化学烟雾
C.白色污染 D.水土流失
②向酸性工业废水中加入次氯酸钠溶液,可将其中的NH 完全转化为N2,而次氯酸钠被还原为NaCl。写出上述反应的离子方程式:
完全转化为N2,而次氯酸钠被还原为NaCl。写出上述反应的离子方程式: _______ 。
(5)潜艇中使用的液氨-液氧燃料电池工作原理如图所示:

①电极a名称是_______ 。
②电解质溶液中OH- 离子向_______ 移动 (填“电极a”或“电极b”)。
③电极b的电极反应式为_______ 。
(1)N元素在元素周期表中的位置为
(2)制备下列物质属于固氮的是 _______。
| A.用氮气和氢气合成氨 |
| B.分离液态空气获得氮气 |
| C.用NH4Cl和熟石灰制备氨气 |
| D.NO2溶于水得到HNO3 |
(4)近几年来关于氮污染的治理倍受关注,根据氮的性质回答以下问题;
①氮的氧化物是空气的主要污染物,下列环境问题与氮的氧化物排放有关的是
A.酸雨 B.光化学烟雾
C.白色污染 D.水土流失
②向酸性工业废水中加入次氯酸钠溶液,可将其中的NH
 完全转化为N2,而次氯酸钠被还原为NaCl。写出上述反应的离子方程式:
完全转化为N2,而次氯酸钠被还原为NaCl。写出上述反应的离子方程式: (5)潜艇中使用的液氨-液氧燃料电池工作原理如图所示:

①电极a名称是
②电解质溶液中OH- 离子向
③电极b的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】2019年5月12日是中国第11个全国防灾减灾日,中国地震局当天在北京正式启动2019年防震减灾千场科普讲座,并推出第三届全国防震减灾科普讲解大赛决赛。地震后的消毒工作至关重要,各种含氯消毒剂得到了广泛应用。被称为当今第四代消毒产品的二氧化氯。其属于A1级别安全高效消毒剂之一,并且可以在极低的浓度下对病菌有杀灭作用,功效显而易见。一起来看看它的使用方法吧。




请回答下列问题:
(1)工业上制备ClO2的化学反应方程式为NaClO3+Na2SO3+H2SO4=ClO2+Na2SO4+H2O,每生成1molClO2转移的电子的物质的量为_______ ,还原剂与氧化剂的物质的量之比为:_______ 。
(2)KClO3和浓盐酸在一定温度下反应生成黄绿色的易爆物二氧化氯和氯气。请完成该化学方程式并配平_______ 。
(3)浓盐酸在反应中显示出来的性质是_______ (填序号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(4)ClO2具有很强的氧化性,因此常被用作消毒剂,其消毒效率(以单位质量得到的电子数表示)是Cl2的_______ 倍(保留小数点后一位)。




请回答下列问题:
(1)工业上制备ClO2的化学反应方程式为NaClO3+Na2SO3+H2SO4=ClO2+Na2SO4+H2O,每生成1molClO2转移的电子的物质的量为
(2)KClO3和浓盐酸在一定温度下反应生成黄绿色的易爆物二氧化氯和氯气。请完成该化学方程式并配平
(3)浓盐酸在反应中显示出来的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(4)ClO2具有很强的氧化性,因此常被用作消毒剂,其消毒效率(以单位质量得到的电子数表示)是Cl2的
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑。
①该反应中的氧化剂是_____ ,还原剂是____ ,每生成1molNa2FeO4转移_______ mol电子。
②简要说明K2FeO4作为水处理剂时所起的作用:_________ 。
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO42—、Cl-、H2O。写出并配平湿法制备高铁酸钾的离子反应方程式:______________ 。
(1)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑。
①该反应中的氧化剂是
②简要说明K2FeO4作为水处理剂时所起的作用:
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO42—、Cl-、H2O。写出并配平湿法制备高铁酸钾的离子反应方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】金属及其化合物在人类生活、生产中发挥着重要的作用。
(1)钠、铝、铁三种金属元素所形成的各种氧化物中具有强氧化性的是______ (填化学式,下同);适宜做耐火材料的是______ 。
(2)若Na2CO3粉末中混有少量NaHCO3杂质,最适宜的除杂方法是__________ ,反应的化学方程式为______________________________ 。
(3)要除去铁粉中混有的少量铝粉,适宜的试剂是______________ ,发生反应的离子方程式为___________________________________________ 。
(4)取少量FeCl2溶液,按下图所示操作,使其跟NaOH溶液反应。可观察到的实验现象是______________ 。

(5)向盛有氯化铁、氯化亚铁、氯化铜混合溶液的烧杯中加入铁粉和铜粉,反应结束后,下列结果不可能出现的是___ (填序号)。
(1)钠、铝、铁三种金属元素所形成的各种氧化物中具有强氧化性的是
(2)若Na2CO3粉末中混有少量NaHCO3杂质,最适宜的除杂方法是
(3)要除去铁粉中混有的少量铝粉,适宜的试剂是
(4)取少量FeCl2溶液,按下图所示操作,使其跟NaOH溶液反应。可观察到的实验现象是

(5)向盛有氯化铁、氯化亚铁、氯化铜混合溶液的烧杯中加入铁粉和铜粉,反应结束后,下列结果不可能出现的是
| A.有铜无铁 | B.有铁无铜 | C.铁、铜都有 | D.铁、铜都无 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】Ⅰ.我国农业因遭受酸雨而造成的损失每年高达15亿多元。为了有效控制酸雨,目前国务院已批准了《酸雨控制区和二氧化硫污染控制区划分方案》等法规。
(1)现有雨水样品1份,每隔一段时间测定该雨水样品的pH所得数据如下:
分析数据,回答下列问题:
①雨水样品的pH变化的原因(用化学方程式表示)______________________
②如果将刚取样的上述雨水和用Cl2消毒的自来水混合,pH将变______ (填“大”.“小”或“不变”),用化学方程式解释原因:__________________________
(2)你认为减少酸雨产生的途径可采用的措施是_____________
①少用煤作燃料 ②把工厂烟囱建高 ③燃烧脱硫 ④在已酸化的土壤中加石灰⑤开发新能源
A.①②③ B.②③④⑤ C.①③⑤ D.①③④⑤
Ⅱ.(1)化学在新型药物的研究中贡献巨大。常见的药物:①阿司匹林(C9H8O4)②盘尼西林(C16H18N2O4S)③抗酸药【MgCO3.Mg(OH)2】④麻黄碱(C10H15NO)其中属于无机物的是______ (填序号)。
(2)蛋白质是生命的基础物质,其水解的最终产物是氨基酸。下列说法不正确的是________ (填序号)。
①氨基酸中含有氨基和羧基 ②富含蛋白质的食物大多为碱性食物 ③加热蛋白质而凝固的变化称为蛋白质的变性 ④血清、肌肉、毛发、指甲等都是由不同蛋白质组成的
(1)现有雨水样品1份,每隔一段时间测定该雨水样品的pH所得数据如下:
| 测试时间/h | 0 | 1 | 2 | 3 | 4 |
| 雨水的pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
分析数据,回答下列问题:
①雨水样品的pH变化的原因(用化学方程式表示)
②如果将刚取样的上述雨水和用Cl2消毒的自来水混合,pH将变
(2)你认为减少酸雨产生的途径可采用的措施是
①少用煤作燃料 ②把工厂烟囱建高 ③燃烧脱硫 ④在已酸化的土壤中加石灰⑤开发新能源
A.①②③ B.②③④⑤ C.①③⑤ D.①③④⑤
Ⅱ.(1)化学在新型药物的研究中贡献巨大。常见的药物:①阿司匹林(C9H8O4)②盘尼西林(C16H18N2O4S)③抗酸药【MgCO3.Mg(OH)2】④麻黄碱(C10H15NO)其中属于无机物的是
(2)蛋白质是生命的基础物质,其水解的最终产物是氨基酸。下列说法不正确的是
①氨基酸中含有氨基和羧基 ②富含蛋白质的食物大多为碱性食物 ③加热蛋白质而凝固的变化称为蛋白质的变性 ④血清、肌肉、毛发、指甲等都是由不同蛋白质组成的
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】中药常采用硫黄熏蒸法以达到防霉、防虫等目的。我国规定党参等中药 残留量不得超过
残留量不得超过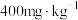 。某小组欲检测某药厂所售党参是否合格,查阅资料后得知:
。某小组欲检测某药厂所售党参是否合格,查阅资料后得知:
① 残留量是指残留硫的总量,以
残留量是指残留硫的总量,以 计;
计;
②中药中残留的 已大部分转化为
已大部分转化为 。
。
(1)将200g所售党参研碎,用 溶液充分浸泡,得无色浸泡液X,将X分成两等份。
溶液充分浸泡,得无色浸泡液X,将X分成两等份。
用 溶液浸泡的目的
溶液浸泡的目的______ (用化学方程式表示)。
(2)甲同学取一份X溶液采用如下方案测定党参中 残留量:
残留量:

判断 溶液已过量的操作为
溶液已过量的操作为______ ;
判断沉淀是否洗净所选用的试剂为______ ;党参中 残留量的表达式为
残留量的表达式为______ 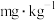 (用含m的式子表示)。
(用含m的式子表示)。
(3)乙同学取另一份X溶液采用如下方案进行测定(整个过程无气体放出),判断该党参______ (填“符合”或“不符合”)国家标准。

 残留量不得超过
残留量不得超过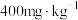 。某小组欲检测某药厂所售党参是否合格,查阅资料后得知:
。某小组欲检测某药厂所售党参是否合格,查阅资料后得知:①
 残留量是指残留硫的总量,以
残留量是指残留硫的总量,以 计;
计;②中药中残留的
 已大部分转化为
已大部分转化为 。
。(1)将200g所售党参研碎,用
 溶液充分浸泡,得无色浸泡液X,将X分成两等份。
溶液充分浸泡,得无色浸泡液X,将X分成两等份。用
 溶液浸泡的目的
溶液浸泡的目的(2)甲同学取一份X溶液采用如下方案测定党参中
 残留量:
残留量:
判断
 溶液已过量的操作为
溶液已过量的操作为判断沉淀是否洗净所选用的试剂为
 残留量的表达式为
残留量的表达式为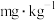 (用含m的式子表示)。
(用含m的式子表示)。(3)乙同学取另一份X溶液采用如下方案进行测定(整个过程无气体放出),判断该党参

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某无色溶液,由Na+、Ba2+、Al3+、Cl-、MnO4-、CO32-、NO3-中的若干种组成。,现取两份100 mL溶液进行如下实验:
① 第一份小心蒸发得溶质3.08g;
② 第二份加足量AgNO3溶液后,得干燥沉淀5.63g,向沉淀中加入足量盐酸,生成标准状况下气体0.224L。
根据上述实验回答下列问题:
(1)第二份溶液所得沉淀的成分是__________ ,其物质的量分别是_________________ 。
(2)写出步骤②中所发生的所有反应的离子方程式_____________________________________________________________________________________________________________ 。
(3)一定存在的离子是____________ ,其浓度分别是_____________________________ 。
① 第一份小心蒸发得溶质3.08g;
② 第二份加足量AgNO3溶液后,得干燥沉淀5.63g,向沉淀中加入足量盐酸,生成标准状况下气体0.224L。
根据上述实验回答下列问题:
(1)第二份溶液所得沉淀的成分是
(2)写出步骤②中所发生的所有反应的离子方程式
(3)一定存在的离子是
您最近一年使用:0次

 恰好完全沉淀,写出反应的离子方程式:
恰好完全沉淀,写出反应的离子方程式:

