利用所学化学反应原理,解决以下问题:
(1)KAl(SO4)2·12H2O可做净水剂,其原理是____________________________________ (用离子方程式表示)
(2)碳酸氢钠溶液蒸干并灼烧得到的固体物质是__________ (填化学式)。
(3)向FeCl3溶液中滴加NaHCO3溶液,有沉淀和气体生成的离子方程式_____________ 。
(4)将AgCl分别放入①5 mL H2O ②10 mL 0.2 mol·L-1 MgCl2溶液 ③20 mL 0.5 mol·L-1 NaCl溶液④40 mL 0.1 mol·L-1 HCl溶液中溶解至饱和,各溶液中Ag+的浓度由大到小的顺序是______ (用序号填空)。
(5)常温下a mol/L CH3COOH稀溶液和b mol/L KOH稀溶液等体积混合:若c(K+)<c (CH3COO-),则a_____________ b(填>、<、=)。
(6)室温下,1 mol/L相同体积的下列四种溶液:①KCl②FeCl3③HF④Na2CO3中,所含阳离子数由少到多的顺序是_________________________ (用序号填空)。
(1)KAl(SO4)2·12H2O可做净水剂,其原理是
(2)碳酸氢钠溶液蒸干并灼烧得到的固体物质是
(3)向FeCl3溶液中滴加NaHCO3溶液,有沉淀和气体生成的离子方程式
(4)将AgCl分别放入①5 mL H2O ②10 mL 0.2 mol·L-1 MgCl2溶液 ③20 mL 0.5 mol·L-1 NaCl溶液④40 mL 0.1 mol·L-1 HCl溶液中溶解至饱和,各溶液中Ag+的浓度由大到小的顺序是
(5)常温下a mol/L CH3COOH稀溶液和b mol/L KOH稀溶液等体积混合:若c(K+)<c (CH3COO-),则a
(6)室温下,1 mol/L相同体积的下列四种溶液:①KCl②FeCl3③HF④Na2CO3中,所含阳离子数由少到多的顺序是
更新时间:2019-01-27 17:31:08
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】按要求填写下列空白:
(1)FeCl2溶液呈_______ 性(填“酸”“中”或“碱”),原因是(用离子方程式表示)_______ ,实验室在配制FeCl2溶液时,常将FeCl2固体先溶于较浓的盐酸中,以_______ 其水解(填“促进”或“抑制”),然后再用蒸馏水稀释到所需的浓度,再加入铁粉,其目的是_______ 。
(2)把AlCl3、NaHCO3、Na2SO3溶液蒸干、灼烧,最后得到的主要固体产物是_______ 、_______ 、_______ (填化学式)。
(3)泡沫灭火器内装有NaHCO3饱和溶液,该溶液呈碱性的原因是_______ (用离子方程式表示);灭火器内另一容器中装有Al2(SO4)3溶液,该溶液呈酸性的原因是_______ (用离子方程式表示);当意外失火时,使泡沫灭火器倒过来摇动即可使药液混合,喷出大量的白色泡沫,阻止火势蔓延,其相关的离子方程式为_______ 。
(4)写出(NH4)2SO4溶液中各粒子浓度关系。
①大小关系(离子):_______ 。
②物料守恒:_______ 。
③电荷守恒:_______ 。
④质子守恒:_______ 。
(1)FeCl2溶液呈
(2)把AlCl3、NaHCO3、Na2SO3溶液蒸干、灼烧,最后得到的主要固体产物是
(3)泡沫灭火器内装有NaHCO3饱和溶液,该溶液呈碱性的原因是
(4)写出(NH4)2SO4溶液中各粒子浓度关系。
①大小关系(离子):
②物料守恒:
③电荷守恒:
④质子守恒:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】现有下列几种物质:①CH3COONa ② NaClO ③ Na2CO3④ 明矾⑤ HCl⑥ Mg(OH)2,回答下列问题:
(1)已知相同条件下,同浓度的CH3COOH和HClO的pH前者小,则同浓度的①和②溶液的pH相比:①___ ②(填“>”“<”或“=”)
(2)写出③的溶液中电荷守恒关系式___ 。
(3)用离子方程式说明④能净水的原理___ 。
(4)常温下,0.1 mol/L HCl 溶液中,水电离出的c(OH-) =___ mol/L。
(5)向①的酚酞溶液中加入少量的NaCl固体,则溶液颜色__ (填“变深”“变浅”或“不变”)。向⑥的饱和溶液中加入少量的MgCl2固体,则⑥的Ksp____ (填“增大”“减小”或“不变”)。该溶液的pH___ (填“增大”“减小”或“不变”)。
(6)上述几种物质中,属于弱电解质的是___ (填序号)。
(1)已知相同条件下,同浓度的CH3COOH和HClO的pH前者小,则同浓度的①和②溶液的pH相比:①
(2)写出③的溶液中电荷守恒关系式
(3)用离子方程式说明④能净水的原理
(4)常温下,0.1 mol/L HCl 溶液中,水电离出的c(OH-) =
(5)向①的酚酞溶液中加入少量的NaCl固体,则溶液颜色
(6)上述几种物质中,属于弱电解质的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题
(1)已知80℃时,水的离子积常数KW=2.5×10-13。该温度下,0.1mol/L某一元酸(HA)溶液中 =108,该溶液中由水电离的c(H+)为
=108,该溶液中由水电离的c(H+)为_______
(2)25℃时,向 溶液中逐滴加入等浓度的
溶液中逐滴加入等浓度的 溶液至
溶液至 恰好沉淀完全。
恰好沉淀完全。
①此过程中水的电离平衡_______ (填“正向”、“逆向”或“不”)移动。
②写出该过程发生反应的离子方程式_______ ;若反应前后溶液体积的变化忽略不计,则反应后所得溶液的pH值为_______ (已知 )。
)。
(3)盐类水解原理在生产生活中有着广泛的应用根据盐类水解的知识回答下列问题:
①灭火器中分隔放置Al2(SO4)3溶液和NaHCO3溶液,灭火时使两种试剂混合,立即喷出大量泡沫,发生反应的离子方程式为_______ 。
②把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是_______ (写化学式)。
③配制保存FeCl3溶液经常会出现颜色变深甚至浑浊的现象,为防止此现象发生,常采取的措施是_______ 。
④25℃时,pH=11的KOH溶液和pH=11的K2CO3溶液中,由水电离出的c(OH﹣)的比值为_______ 。
(1)已知80℃时,水的离子积常数KW=2.5×10-13。该温度下,0.1mol/L某一元酸(HA)溶液中
 =108,该溶液中由水电离的c(H+)为
=108,该溶液中由水电离的c(H+)为(2)25℃时,向
 溶液中逐滴加入等浓度的
溶液中逐滴加入等浓度的 溶液至
溶液至 恰好沉淀完全。
恰好沉淀完全。①此过程中水的电离平衡
②写出该过程发生反应的离子方程式
 )。
)。(3)盐类水解原理在生产生活中有着广泛的应用根据盐类水解的知识回答下列问题:
①灭火器中分隔放置Al2(SO4)3溶液和NaHCO3溶液,灭火时使两种试剂混合,立即喷出大量泡沫,发生反应的离子方程式为
②把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是
③配制保存FeCl3溶液经常会出现颜色变深甚至浑浊的现象,为防止此现象发生,常采取的措施是
④25℃时,pH=11的KOH溶液和pH=11的K2CO3溶液中,由水电离出的c(OH﹣)的比值为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】工业制胆矾时,将粗制CuO粉末(含杂质FeO、Fe2O3)慢慢加入适量的稀H2SO4中完全溶解,除去杂质离子后,再经过一系列操作可得纯净的胆矾晶体。已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;pH接近4时,Fe3+以Fe(OH)3的形式完全沉淀。回答下列问题:
(1)为除去溶液中的Fe2+,可先加入_______ ,(从下面四个选项选择)将Fe2+氧化为Fe3+,反应的离子方程式为_______ ,然后加入适量的_______ ,(从下面四个选项选择)调整溶液的pH使Fe3+转化为Fe(OH)3沉淀。
A.CuO B.Cl2 C.Cu(OH)2 D.H2O2
(2)“再经过一系列操作可得纯净的胆矾晶体”,一系列操作是指_______ 、_______ 、_______ 。
(3)CuSO4 溶液显酸性的原因为_______ (用离子方程式表示)。
(4)pH=6,CuSO4溶液中由水电离出的c(H+)是_______ 。
(1)为除去溶液中的Fe2+,可先加入
A.CuO B.Cl2 C.Cu(OH)2 D.H2O2
(2)“再经过一系列操作可得纯净的胆矾晶体”,一系列操作是指
(3)CuSO4 溶液显酸性的原因为
(4)pH=6,CuSO4溶液中由水电离出的c(H+)是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】中学常用淡黄色的pH试纸测定溶液的酸碱性。在25℃时,若溶液的pH=7,试纸不变色;若pH< 7 ,试纸变红色;若pH > 7,试纸变蓝色。
⑴已知水中存在如下平衡: H2O + H2O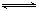 H3O+ + OH-。现要使平衡向右移动,且所得的溶液呈酸性,选择的方法是
H3O+ + OH-。现要使平衡向右移动,且所得的溶液呈酸性,选择的方法是_________
A.向水中加入NaHSO4 B.向水中加入Cu(NO3)2
C.加热至100℃ D.向水中加入(NH4)2SO4
⑵现要用pH试纸测定100℃沸水的pH。若则试纸显___ 色,溶液呈_____ 性(填酸、碱或中)。
⑶纯碱因水溶液显碱性而得名。请用离子方程式表示显碱性的原因:______________ 。
⑴已知水中存在如下平衡: H2O + H2O
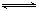 H3O+ + OH-。现要使平衡向右移动,且所得的溶液呈酸性,选择的方法是
H3O+ + OH-。现要使平衡向右移动,且所得的溶液呈酸性,选择的方法是A.向水中加入NaHSO4 B.向水中加入Cu(NO3)2
C.加热至100℃ D.向水中加入(NH4)2SO4
⑵现要用pH试纸测定100℃沸水的pH。若则试纸显
⑶纯碱因水溶液显碱性而得名。请用离子方程式表示显碱性的原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氮及其化合物在工农业生产、生活中有着重要作用。请回答下列问题:
(1)图1是1molNO2和1molCO反应生成CO2和NO过程中能量变化示意图(a、b均大于0),且已知:2CO(g)+2NO(g)=N2(g)+2CO2(g) △H=-ckJ·mol-1(c>0),请写出CO将NO2还原至N2时的热化学方程式____ 。

(2)图2是实验室在三个不同条件的密闭容器中合成氨时,N2的浓度随时间的变化曲线(以a、b、c表示)。已知三个条件下起始加入浓度均为:c(N2)=0.1mol·L-1,c(H2)=0.3mol·L-1;合成氨的反应:N2(g)+3H2(g) 2NH3(g) △H<0。
2NH3(g) △H<0。

①计算在曲线a达平衡时H2的转化率为____ 。
②由图2可知,b、c各有一个条件与a不同,则c的条件改变可能是____ ;写出判断b与a条件不同的理由____ 。
(3)利用图2中c条件下合成氨(容积固定)。已知化学平衡常数K与温度(T)的关系如表:
①试确定K1的相对大小,K1____ 4.1×106(填写“>”、“=”或“<”)
②恒温恒容时,下列各项能作为判断该反应达到化学平衡状态的依据的是____ 。
A.容器内NH3的浓度保持不变 B.2v(N2)正=v(H2)逆
C.容器内压强保持不变 D.混合气体的密度保持不变
(4)明矾[KAl(SO4)2·12H2O]可用作净水剂,是因为水解生成氢氧化铝胶体吸附水中的悬浮杂质。写出水解反应的离子方程式____
(1)图1是1molNO2和1molCO反应生成CO2和NO过程中能量变化示意图(a、b均大于0),且已知:2CO(g)+2NO(g)=N2(g)+2CO2(g) △H=-ckJ·mol-1(c>0),请写出CO将NO2还原至N2时的热化学方程式

(2)图2是实验室在三个不同条件的密闭容器中合成氨时,N2的浓度随时间的变化曲线(以a、b、c表示)。已知三个条件下起始加入浓度均为:c(N2)=0.1mol·L-1,c(H2)=0.3mol·L-1;合成氨的反应:N2(g)+3H2(g)
 2NH3(g) △H<0。
2NH3(g) △H<0。
①计算在曲线a达平衡时H2的转化率为
②由图2可知,b、c各有一个条件与a不同,则c的条件改变可能是
(3)利用图2中c条件下合成氨(容积固定)。已知化学平衡常数K与温度(T)的关系如表:
| T/(K) | 298 | 398 | 498 | …… |
| K | 4.1×106 | K1 | K2 | …… |
②恒温恒容时,下列各项能作为判断该反应达到化学平衡状态的依据的是
A.容器内NH3的浓度保持不变 B.2v(N2)正=v(H2)逆
C.容器内压强保持不变 D.混合气体的密度保持不变
(4)明矾[KAl(SO4)2·12H2O]可用作净水剂,是因为水解生成氢氧化铝胶体吸附水中的悬浮杂质。写出水解反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】电解质水溶液中存在电离平衡,水解平衡、沉淀溶解平衡。请回答下列问题:
(1)常温下,部分弱酸的电离平衡常数如表:
①等浓度CH3COONa、NaClO、 Na2CO3和NaHCO3溶液中,碱性最强的是_______ 。
②等浓度的CH3COONa与NaClO混合溶液中离子浓度由大到小的顺序为_______
(2)室温下,用0.10mol•L−1盐酸溶液滴定20mL 0.1mol•L−1氨水溶液,滴定曲线如图所示。

①该中和滴定选用_______ (填“甲基橙”或“酚酞”)作指示剂。
②室温下,0.10mol•L−1氨水溶液中NH3•H2O的电离平衡常数约为_______ mol·L−1
③b点所示的溶液中c(NH )+c(NH3•H2O)=
)+c(NH3•H2O)=_______ (用溶液的其它离子浓度表示)。
(3)工业上向锅炉里注入所得到的Na2CO3溶液浸泡,将水垢中的CaSO4转化为CaCO3,而后用醋酸除去。当把水垢中CaSO4完全转化时,混合溶液中的c(CO )=1.0×10−3mol·L−1,则c(SO
)=1.0×10−3mol·L−1,则c(SO )=
)=_______ 。Ksp(CaSO4)=9.1×10−6 Ksp(CaCO3)=3.4×10−9(保留小数点后一位)
(1)常温下,部分弱酸的电离平衡常数如表:
| 弱酸 | CH3COOH | HClO | H2CO3 |
| 电离平衡常数 | Ka=1.8×10-5 | Ka=3.1×10-8 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
②等浓度的CH3COONa与NaClO混合溶液中离子浓度由大到小的顺序为
(2)室温下,用0.10mol•L−1盐酸溶液滴定20mL 0.1mol•L−1氨水溶液,滴定曲线如图所示。

①该中和滴定选用
②室温下,0.10mol•L−1氨水溶液中NH3•H2O的电离平衡常数约为
③b点所示的溶液中c(NH
 )+c(NH3•H2O)=
)+c(NH3•H2O)=(3)工业上向锅炉里注入所得到的Na2CO3溶液浸泡,将水垢中的CaSO4转化为CaCO3,而后用醋酸除去。当把水垢中CaSO4完全转化时,混合溶液中的c(CO
 )=1.0×10−3mol·L−1,则c(SO
)=1.0×10−3mol·L−1,则c(SO )=
)=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题:
(1)写出氯原子的基态原子核外电子排布式:____ 。
(2)已知CO与N2结构相似,CO分子内σ键与π键个数之比为:____ 。
(3)0.1mol·L-1NaHCO3溶液中,含碳元素粒子浓度的大小顺序为:____ 。
(1)写出氯原子的基态原子核外电子排布式:
(2)已知CO与N2结构相似,CO分子内σ键与π键个数之比为:
(3)0.1mol·L-1NaHCO3溶液中,含碳元素粒子浓度的大小顺序为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】常温下,用0.01mol/L的NaOH溶液滴定 溶液,测得溶液pH与NaOH溶液体积的关系如图所示。
溶液,测得溶液pH与NaOH溶液体积的关系如图所示。

(1)c点时溶液中各离子浓度由大到小的顺序为___________ 。
(2)b点时溶液显___________ 性,(填“酸”“碱”“中”性)原因是:___________ (用离子方程式解释);此时溶液中的质子守恒式为:___________ 。
(3)a点时溶液中电荷守恒式为:___________ 。
(4)硝酸银溶液和硫酸钠溶液混合,可以得到白色的硫酸银沉淀,向该分散系中滴加铬酸钠溶液,当白色沉淀和红色沉淀(铬酸银为红色沉淀)共存时,分散系中 =
=___________ [已知 ,
, ]。
]。
 溶液,测得溶液pH与NaOH溶液体积的关系如图所示。
溶液,测得溶液pH与NaOH溶液体积的关系如图所示。
(1)c点时溶液中各离子浓度由大到小的顺序为
(2)b点时溶液显
(3)a点时溶液中电荷守恒式为:
(4)硝酸银溶液和硫酸钠溶液混合,可以得到白色的硫酸银沉淀,向该分散系中滴加铬酸钠溶液,当白色沉淀和红色沉淀(铬酸银为红色沉淀)共存时,分散系中
 =
= ,
, ]。
]。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答问题:
Ⅰ.常温下,CaS的Ksp=10-8,饱和溶液中存在平衡: CaS(s) Ca2+(aq)+S2-(aq)
Ca2+(aq)+S2-(aq)
(1)①该温度下,将10-4mol/L氯化钙溶液与2×10-4mol/L硫化钠溶液等体积混合,能否产生沉淀?答___ ;温度升高时,Ksp__ (填“增大”、“减小”或“不变”下同)。
②滴加少量浓盐酸,c(Ca2+)___ ,原因是___ (用文字和离子方程式说明)。
(2)若向CaS悬浊液中加入CuSO4溶液,生成一种黑色固体物质,写出该过程中反应的离子方程式___ 。
Ⅱ.(已知Ksp[Fe(OH)3]=10-38)若0.01mol/L FeCl3溶液中,如果要生成Fe(OH)3沉淀,应调整溶液pH,使pH___ ,若要使其沉淀完全,pH应___ 。(提示:填数据时,要有>,<,=)
Ⅰ.常温下,CaS的Ksp=10-8,饱和溶液中存在平衡: CaS(s)
 Ca2+(aq)+S2-(aq)
Ca2+(aq)+S2-(aq)(1)①该温度下,将10-4mol/L氯化钙溶液与2×10-4mol/L硫化钠溶液等体积混合,能否产生沉淀?答
②滴加少量浓盐酸,c(Ca2+)
(2)若向CaS悬浊液中加入CuSO4溶液,生成一种黑色固体物质,写出该过程中反应的离子方程式
Ⅱ.(已知Ksp[Fe(OH)3]=10-38)若0.01mol/L FeCl3溶液中,如果要生成Fe(OH)3沉淀,应调整溶液pH,使pH
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】一定温度下,在氯化银悬浊液中,存在如下平衡:AgCl(s)⇌Ag+(aq)+Cl-(aq),判断下表中加入不同物质的平衡移动情况及溶液中各项的变化。
| 外界条件 | 移动方向 | c(Ag+) | Ksp |
| 升高温度 | |||
| 加入少量AgNO3 | |||
| 加入Na2S | |||
| 通入HCl |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)对于Ag2S(s)⇌2Ag+(aq)+S2-(aq),其Ksp的表达式为_______
(2)下列说法不正确的是_______ (填序号)。
①用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl少
②一般来说,物质的溶解度随温度的升高而增加,故物质的溶解过程大多是吸热过程
③对于Al(OH)3(s)⇌Al3+(aq)+3OH-(aq)和Al(OH)3⇌Al3++3OH-,前者为溶解平衡,后者为电离平衡
④除去溶液中的Mg2+,用OH-沉淀比用CO 好,说明Mg(OH)2的溶解度比MgCO3大
好,说明Mg(OH)2的溶解度比MgCO3大
⑤沉淀反应中常加入过量的沉淀剂,其目的是使沉淀更完全
(3)如何除去Mg(OH)2中混有的Ca(OH)2_______
(4)已知在25 ℃时Ksp[Mg(OH)2]=3.2×10-11,向0.02 mol·L-1的MgCl2溶液中加入NaOH固体,如要生成Mg(OH)2沉淀,应使溶液中的c(OH-)最小为_______ mol·L-1。
(2)下列说法不正确的是
①用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl少
②一般来说,物质的溶解度随温度的升高而增加,故物质的溶解过程大多是吸热过程
③对于Al(OH)3(s)⇌Al3+(aq)+3OH-(aq)和Al(OH)3⇌Al3++3OH-,前者为溶解平衡,后者为电离平衡
④除去溶液中的Mg2+,用OH-沉淀比用CO
 好,说明Mg(OH)2的溶解度比MgCO3大
好,说明Mg(OH)2的溶解度比MgCO3大⑤沉淀反应中常加入过量的沉淀剂,其目的是使沉淀更完全
(3)如何除去Mg(OH)2中混有的Ca(OH)2
(4)已知在25 ℃时Ksp[Mg(OH)2]=3.2×10-11,向0.02 mol·L-1的MgCl2溶液中加入NaOH固体,如要生成Mg(OH)2沉淀,应使溶液中的c(OH-)最小为
您最近一年使用:0次



