2024高三·全国·专题练习
解题方法
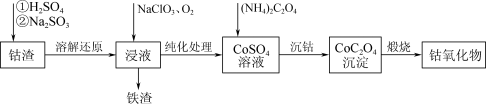
1 . Co3O4在磁性材料、电化学领域应用广泛,实验室中可以用CoCO3或CoC2O4煅烧后制得。利用钴渣[含Co(OH)3、Fe(OH)3等]制备钴氧化物的流程如下:
(1)“溶解还原”过程中Co(OH)3发生反应的离子方程式为_______ 。
(2)“沉钴”时,不能用Na2C2O4溶液代替(NH4)2C2O4溶液,原因是_______ 。
(3)检验CoC2O4固体是否洗净的实验操作是_______ 。
(4)为测定某草酸钴样品中草酸钴晶体(CoC2O4·2H2O)的质量分数进行如下实验:
①取草酸钴(CoC2O4·2H2O,摩尔质量为183g·mol-1)样品3.660g,加入100.00mL0.1000mol·L-1酸性KMnO4溶液,加热(该条件下Co2+不被氧化)。
②充分反应后将溶液冷却至室温,加入250mL容量瓶中,定容。
③取25.00mL溶液,用0.1000mol·L-1FeSO4溶液滴定。
④重复步骤③的实验两次,三次测定数据如下:
计算样品中草酸钴晶体(CoC2O4·2H2O)的质量分数_______ (写出计算过程)。
(5)以尿素为原料可获得CoCO3并制备Co3O4.已知:尿素水溶液在70℃以上能缓慢水解产生 ,在pH为1~3时水解速率对生成CoCO3沉淀较为适宜。设计以CoCl2溶液、尿素粉末、盐酸为原料,制备Co3O4的实验方案:取一定体积CoCl2溶液,
,在pH为1~3时水解速率对生成CoCO3沉淀较为适宜。设计以CoCl2溶液、尿素粉末、盐酸为原料,制备Co3O4的实验方案:取一定体积CoCl2溶液,_______ 。
(1)“溶解还原”过程中Co(OH)3发生反应的离子方程式为
(2)“沉钴”时,不能用Na2C2O4溶液代替(NH4)2C2O4溶液,原因是
(3)检验CoC2O4固体是否洗净的实验操作是
(4)为测定某草酸钴样品中草酸钴晶体(CoC2O4·2H2O)的质量分数进行如下实验:
①取草酸钴(CoC2O4·2H2O,摩尔质量为183g·mol-1)样品3.660g,加入100.00mL0.1000mol·L-1酸性KMnO4溶液,加热(该条件下Co2+不被氧化)。
②充分反应后将溶液冷却至室温,加入250mL容量瓶中,定容。
③取25.00mL溶液,用0.1000mol·L-1FeSO4溶液滴定。
④重复步骤③的实验两次,三次测定数据如下:
| 实验序号 | 1 | 2 | 3 |
| 消耗FeSO4标准溶液体积/mL | 18.32 | 18.02 | 17.98 |
(5)以尿素为原料可获得CoCO3并制备Co3O4.已知:尿素水溶液在70℃以上能缓慢水解产生
 ,在pH为1~3时水解速率对生成CoCO3沉淀较为适宜。设计以CoCl2溶液、尿素粉末、盐酸为原料,制备Co3O4的实验方案:取一定体积CoCl2溶液,
,在pH为1~3时水解速率对生成CoCO3沉淀较为适宜。设计以CoCl2溶液、尿素粉末、盐酸为原料,制备Co3O4的实验方案:取一定体积CoCl2溶液,
您最近半年使用:0次
2024高三·全国·专题练习
2 . 室温下,下列实验探究方案、现象得出的结论错误的是
| 选项 | 探究方案 | 现象 | 结论 |
| A | 向5mL0.1mol·L-1KI溶液中加入1mL0.1mol·L-1FeCl3溶液,充分反应后用苯萃取2~3次,取水层滴加KSCN溶液 | 溶液变红色 | 反应:2Fe3++2I-=2Fe2++I2有一定限度 |
| B | 将Na[Al(OH)4]溶液与NaHCO3溶液混合,观察现象 | 产生白色沉淀 | 结合质子能力:[Al(OH)4]-> |
| C | 向Fe(NO3)2溶液中滴入硫酸酸化的H2O2溶液,观察溶液颜色变化 | 溶液变黄色 | 氧化性:H2O2>Fe3+ |
| D | 用pH计测量等温等浓度的CH3COONa和HCOONa溶液的pH | pH:前者更大 | Kh(CH3COO-)>Kh(HCOO-) |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
3 . 室温下,通过下列实验探究某些碳酸盐溶液及碳酸氢盐溶液的性质。
已知: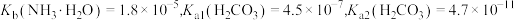 。
。
下列有关说法正确的是
已知:
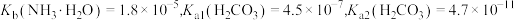 。
。| 实验 | 实验操作和现象 |
| 1 | 测量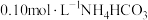 溶液的 溶液的 ,测得 ,测得 为 为 |
| 2 | 测量某浓度的 溶液的 溶液的 ,测得 ,测得 约为9.4 约为9.4 |
| 3 | 将两种浓度均为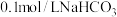 和 和 溶液等体积混合,测量其 溶液等体积混合,测量其 |
A.实验1溶液中: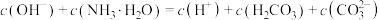 |
B.实验1测得的 值 值 |
C.实验2溶液中: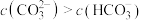 |
D.实验3所得溶液中: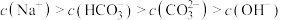 |
您最近半年使用:0次
2024高三·全国·专题练习
解题方法
4 . 通过下列实验操作和实验现象,得到的结论正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 用pH试纸测溶液pH | NaHCO3显蓝色,NaHSO3显红色 | H2CO3、H2SO3均是弱酸 |
| B | 向钾盐溶液中滴加浓盐酸 | 产生的无色气体使品红溶液褪色 | 该钾盐一定是K2SO3或KHSO3 |
| C | 向含有等量KBr、KI混合溶液中依次加入少量新制氯水和CCl4,振荡、静置 | 溶液分层,下层呈紫红色 | 氧化性:Cl2>Br2>I2 |
| D | 在火焰上灼烧搅拌过某无色溶液的玻璃棒 | 火焰出现黄色 | 不能确定溶液中含有Na元素 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
5 . 25℃时,向 的
的 溶液(
溶液( )中通入HCl或加入NaOH调节pH,不考虑溶液体积变化且过程中无气体逸出。含碳(或氮)微粒的分布分数
)中通入HCl或加入NaOH调节pH,不考虑溶液体积变化且过程中无气体逸出。含碳(或氮)微粒的分布分数 [如:
[如: ]与pH关系如图。下列说法错误的是
]与pH关系如图。下列说法错误的是
 的
的 溶液(
溶液( )中通入HCl或加入NaOH调节pH,不考虑溶液体积变化且过程中无气体逸出。含碳(或氮)微粒的分布分数
)中通入HCl或加入NaOH调节pH,不考虑溶液体积变化且过程中无气体逸出。含碳(或氮)微粒的分布分数 [如:
[如: ]与pH关系如图。下列说法错误的是
]与pH关系如图。下列说法错误的是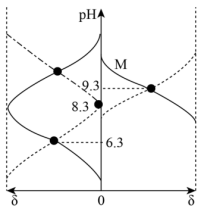
A. 溶液在 溶液在 时存在: 时存在: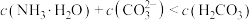 |
B.曲线M表示 的分布分数随pH变化 的分布分数随pH变化 |
C. 的 的 |
D.该体系在 时,溶液中 时,溶液中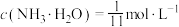 |
您最近半年使用:0次
6 . 草酸是植物(特别是草本植物)常具有的成分,有广泛的用途。草酸晶体( )无色,熔点为101℃,易溶于水。常温下草酸的电离常数
)无色,熔点为101℃,易溶于水。常温下草酸的电离常数 ,
, 。
。
(1)写出草酸第一步电离方程式:______
(2)草酸具有很强的还原性,与氧化剂作用易被氧化成二氧化碳和水,可以使酸性高锰酸钾( )溶液褪色,写出发生反应的离子方程式:
)溶液褪色,写出发生反应的离子方程式:______ 。为了探究浓度对化学反应速率的影响,相同温度条件下,分别用2支试管设计了如下实验:
此实验中,加入 溶液的体积应为
溶液的体积应为______ mL。
(3)结合题干所给的电离平衡常数,判断 溶液的酸碱性,应显
溶液的酸碱性,应显______ 性(填“酸”或“碱”)。
(4)设计实验证明草酸为弱酸的方案及其现象均正确的有______(填序号)。
(5)为测定某 溶液的浓度,取20.00mL
溶液的浓度,取20.00mL 溶液于锥形瓶中,滴入2~3滴指示剂,用0.1000mol/L的NaOH溶液进行滴定,并进行3次平行实验,所用NaOH溶液体积分别为19.98mL、20.02mL和22.02mL。
溶液于锥形瓶中,滴入2~3滴指示剂,用0.1000mol/L的NaOH溶液进行滴定,并进行3次平行实验,所用NaOH溶液体积分别为19.98mL、20.02mL和22.02mL。
①若所用指示剂为酚酞,则滴定终点时的现象为______ ;
② 溶液物质的量浓度为
溶液物质的量浓度为______ mol/L;
③下列操作会引起测定结果偏高的是______ (填序号)。
A.滴定管在盛装NaOH溶液前未润洗
B.滴定过程中,锥形瓶震荡的太剧烈,以致部分液体溅出
C.锥形瓶水洗后未干燥
D.滴定前读数正确,滴定终点时仰视读数
 )无色,熔点为101℃,易溶于水。常温下草酸的电离常数
)无色,熔点为101℃,易溶于水。常温下草酸的电离常数 ,
, 。
。(1)写出草酸第一步电离方程式:
(2)草酸具有很强的还原性,与氧化剂作用易被氧化成二氧化碳和水,可以使酸性高锰酸钾(
 )溶液褪色,写出发生反应的离子方程式:
)溶液褪色,写出发生反应的离子方程式:试管 | A | B |
加入试剂 | 4mL 0.01moL/L | ______0.02moL/L |
1mL 0.1moL/L | 1mL 0.1moL/L | |
2mL 0.1moL/L | 2mL 0.1moL/L |
 溶液的体积应为
溶液的体积应为(3)结合题干所给的电离平衡常数,判断
 溶液的酸碱性,应显
溶液的酸碱性,应显(4)设计实验证明草酸为弱酸的方案及其现象均正确的有______(填序号)。
A.室温下,取0.01mol/L 溶液,测其pH=2; 溶液,测其pH=2; |
B.室温下,取0.01mol/L 溶液,测其pH>7; 溶液,测其pH>7; |
C.室温下,取pH=a( )的 )的 溶液稀释100倍后,测其 溶液稀释100倍后,测其 ; ; |
D.标况下,取0.1moL/L的 溶液100mL与足量锌粉反应,收集到 溶液100mL与足量锌粉反应,收集到 体积为224mL; 体积为224mL; |
 溶液的浓度,取20.00mL
溶液的浓度,取20.00mL 溶液于锥形瓶中,滴入2~3滴指示剂,用0.1000mol/L的NaOH溶液进行滴定,并进行3次平行实验,所用NaOH溶液体积分别为19.98mL、20.02mL和22.02mL。
溶液于锥形瓶中,滴入2~3滴指示剂,用0.1000mol/L的NaOH溶液进行滴定,并进行3次平行实验,所用NaOH溶液体积分别为19.98mL、20.02mL和22.02mL。①若所用指示剂为酚酞,则滴定终点时的现象为
②
 溶液物质的量浓度为
溶液物质的量浓度为③下列操作会引起测定结果偏高的是
A.滴定管在盛装NaOH溶液前未润洗
B.滴定过程中,锥形瓶震荡的太剧烈,以致部分液体溅出
C.锥形瓶水洗后未干燥
D.滴定前读数正确,滴定终点时仰视读数
您最近半年使用:0次
名校
解题方法
7 . 常温下,下列有关叙述不正确的是
A.若 溶液的 溶液的 ,则 ,则 |
B.0.2mol/L的亚硫酸氢钠溶液中: |
C. 和 和 混合溶液中: 混合溶液中: |
D.已知 的 的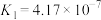 , , ,则NaHA溶液呈碱性 ,则NaHA溶液呈碱性 |
您最近半年使用:0次
名校
解题方法
8 . 在不同温度下,水溶液中 与
与 有如图所示关系。下列说法正确的是
有如图所示关系。下列说法正确的是
 与
与 有如图所示关系。下列说法正确的是
有如图所示关系。下列说法正确的是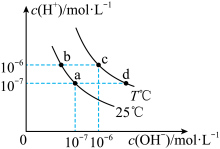
A.c点对应的溶液 ,溶液呈弱酸性 ,溶液呈弱酸性 |
B.b点对应的溶液中可以大量共存: 、 、 、 、 、 、 |
C.若a点表示 和 和 的混合溶液,则该溶液中的离子浓度大小为: 的混合溶液,则该溶液中的离子浓度大小为: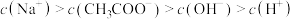 |
D.若d点表示某等浓度、等体积的 和 和 混合溶液,则溶液中的离子浓度存在如下关系: 混合溶液,则溶液中的离子浓度存在如下关系: |
您最近半年使用:0次
名校
解题方法
9 . 下列物质的电离方程式或水解方程式书写正确的是
A. | B.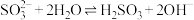 |
C.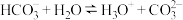 | D. |
您最近半年使用:0次
10 . 已知 为二元弱酸,且
为二元弱酸,且 ,向
,向 溶液中逐滴加入一元弱酸HB溶液,溶液中的离子浓度变化关系如图所示:
溶液中逐滴加入一元弱酸HB溶液,溶液中的离子浓度变化关系如图所示:
 为二元弱酸,且
为二元弱酸,且 ,向
,向 溶液中逐滴加入一元弱酸HB溶液,溶液中的离子浓度变化关系如图所示:
溶液中逐滴加入一元弱酸HB溶液,溶液中的离子浓度变化关系如图所示:
A. 为 为 随 随 的变化关系 的变化关系 |
B.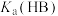 的数量级为 的数量级为 |
C.NaHA溶液中: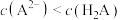 |
D.向 溶液中滴入足量HB溶液的离子方程式为 溶液中滴入足量HB溶液的离子方程式为 |
您最近半年使用:0次




