金属铬坚硬,耐腐蚀,可做镀层金属,并且在制皮革,羊毛,火柴,颜料等方面均有其应用。但是 致癌,因而工业废水中如果含有
致癌,因而工业废水中如果含有 需要处理后再排放。
需要处理后再排放。
已知: ,
,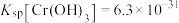 ,
, 完全沉淀时的
完全沉淀时的 约为5.6。
约为5.6。
(1)沉淀法
利用 试剂可处理含
试剂可处理含 废水,离子方程式为
废水,离子方程式为_______ 。
(2)还原法
①可以选择还原剂 ,对酸性含铬废水进行处理。将下述反应的离子方程式补充完整:
,对酸性含铬废水进行处理。将下述反应的离子方程式补充完整:_______ 。

②可以选择焦亚硫酸钠( )处理含铬
)处理含铬 废水,处理费用低。其工艺流程如图:
废水,处理费用低。其工艺流程如图:

资料:焦亚硫酸钠 为白色或黄色结晶粉末,遇强酸放出
为白色或黄色结晶粉末,遇强酸放出 。
。
ⅰ反应池中发生反应的离子方程式_______ 。
ⅱ 在酸性条件下氧化性强,在实际工业中
在酸性条件下氧化性强,在实际工业中 过低,则需要的焦亚硫酸钠的量比理论值高出许多,结合化学用语解释可能的原因是
过低,则需要的焦亚硫酸钠的量比理论值高出许多,结合化学用语解释可能的原因是_______ 。
(3) /纳米
/纳米 去除法
去除法
①某研究小组经查阅资料,发现磁铁矿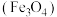 辅助纳米
辅助纳米 可能会降解含
可能会降解含 的废水。为探究其真实性,进行了如下实验,相同时间内得到如下实验结果,请补全实验结论。
的废水。为探究其真实性,进行了如下实验,相同时间内得到如下实验结果,请补全实验结论。
结论ⅰ:单独使用纳米铁可以降解
ⅱ:单独使用 可以降解
可以降解 ,降解率偏低
,降解率偏低
ⅲ:_______ 。
②经查阅资料,依据如下两个图示信息,上述实验3降解 效率增大的原因是
效率增大的原因是_______ 。

 致癌,因而工业废水中如果含有
致癌,因而工业废水中如果含有 需要处理后再排放。
需要处理后再排放。已知:
 ,
,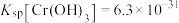 ,
, 完全沉淀时的
完全沉淀时的 约为5.6。
约为5.6。(1)沉淀法
利用
 试剂可处理含
试剂可处理含 废水,离子方程式为
废水,离子方程式为(2)还原法
①可以选择还原剂
 ,对酸性含铬废水进行处理。将下述反应的离子方程式补充完整:
,对酸性含铬废水进行处理。将下述反应的离子方程式补充完整:
②可以选择焦亚硫酸钠(
 )处理含铬
)处理含铬 废水,处理费用低。其工艺流程如图:
废水,处理费用低。其工艺流程如图:
资料:焦亚硫酸钠
 为白色或黄色结晶粉末,遇强酸放出
为白色或黄色结晶粉末,遇强酸放出 。
。ⅰ反应池中发生反应的离子方程式
ⅱ
 在酸性条件下氧化性强,在实际工业中
在酸性条件下氧化性强,在实际工业中 过低,则需要的焦亚硫酸钠的量比理论值高出许多,结合化学用语解释可能的原因是
过低,则需要的焦亚硫酸钠的量比理论值高出许多,结合化学用语解释可能的原因是(3)
 /纳米
/纳米 去除法
去除法①某研究小组经查阅资料,发现磁铁矿
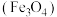 辅助纳米
辅助纳米 可能会降解含
可能会降解含 的废水。为探究其真实性,进行了如下实验,相同时间内得到如下实验结果,请补全实验结论。
的废水。为探究其真实性,进行了如下实验,相同时间内得到如下实验结果,请补全实验结论。| 实验编号 | 纳米 |  |  实际降解率 实际降解率 |
| 1 | 0.05 | 0 |  |
| 2 | 0 | 2 |  |
| 3 | 0.05 | 2 |  |

ⅱ:单独使用
 可以降解
可以降解 ,降解率偏低
,降解率偏低ⅲ:
②经查阅资料,依据如下两个图示信息,上述实验3降解
 效率增大的原因是
效率增大的原因是
更新时间:2022-09-01 19:39:05
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】将一定量铝粉和铁粉的混合物加入一定量极稀的硝酸中,充分反应,反应过程中无气体放出。向反应结束后的溶液中,逐滴加入 的
的 溶液,所加
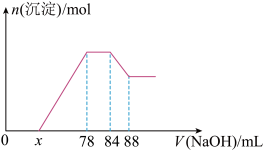
溶液,所加 溶液的体积与产生沉淀的物质的量关系如图所示:
溶液的体积与产生沉淀的物质的量关系如图所示:
已知:ⅰ.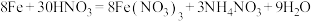
ⅱ.
ⅲ.
ⅳ.不考虑水的电离及物质与水发生的反应;
ⅴ.不考虑空气对反应的影响。
回答下列问题:
(1)“0”点时,溶液中所含的溶质为 、
、 、
、 和
和_______ (填化学式)。
(2)在反应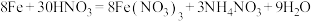 中:
中:
①该反应出现的物质中属于盐的是_______ (填化学式)。
②检验 溶液中
溶液中 的方法为
的方法为_______ 。
③化合物 中,氮元素的化合价为
中,氮元素的化合价为_______ 。
(3)反应ⅱ的离子方程式为_______ 。
(4)原混合物中,铁粉的总质量为_______ g。
(5)“x”点对应的溶液中:
①
_______ 。
②该点对应的溶液中,所含 的总物质的量为
的总物质的量为_______ mol。(不考虑 、
、 和
和 与
与 发生的反应)
发生的反应)
 的
的 溶液,所加
溶液,所加 溶液的体积与产生沉淀的物质的量关系如图所示:
溶液的体积与产生沉淀的物质的量关系如图所示:
已知:ⅰ.
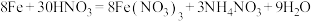
ⅱ.

ⅲ.

ⅳ.不考虑水的电离及物质与水发生的反应;
ⅴ.不考虑空气对反应的影响。
回答下列问题:
(1)“0”点时,溶液中所含的溶质为
 、
、 、
、 和
和(2)在反应
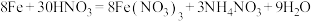 中:
中:①该反应出现的物质中属于盐的是
②检验
 溶液中
溶液中 的方法为
的方法为③化合物
 中,氮元素的化合价为
中,氮元素的化合价为(3)反应ⅱ的离子方程式为
(4)原混合物中,铁粉的总质量为
(5)“x”点对应的溶液中:
①

②该点对应的溶液中,所含
 的总物质的量为
的总物质的量为 、
、 和
和 与
与 发生的反应)
发生的反应)
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】已知A、B、C、D四种可溶性盐,它们的阳离子分别是Ba2+、Ag+、Cu2+、Na+中的一种,阴离子分别是CO 、NO
、NO 、SO
、SO 、Cl-中的一种(离子不能重复),进行如下实验:①分别溶于水,只有C溶液呈蓝色;②若把足量盐酸分别加入到上述四溶液,B中出现沉淀,D溶液有无色无味的气体放出;根据①②的实验事实,可推断它们的化学式为:
、Cl-中的一种(离子不能重复),进行如下实验:①分别溶于水,只有C溶液呈蓝色;②若把足量盐酸分别加入到上述四溶液,B中出现沉淀,D溶液有无色无味的气体放出;根据①②的实验事实,可推断它们的化学式为:
(1)A___________ ;B___________ ;C___________ ;D___________ 。
(2)加入足量盐酸后D中反应的离子方程式:___________ 。
(3)写出C与NaOH溶液反应的离子方程式:___________ 。
 、NO
、NO 、SO
、SO 、Cl-中的一种(离子不能重复),进行如下实验:①分别溶于水,只有C溶液呈蓝色;②若把足量盐酸分别加入到上述四溶液,B中出现沉淀,D溶液有无色无味的气体放出;根据①②的实验事实,可推断它们的化学式为:
、Cl-中的一种(离子不能重复),进行如下实验:①分别溶于水,只有C溶液呈蓝色;②若把足量盐酸分别加入到上述四溶液,B中出现沉淀,D溶液有无色无味的气体放出;根据①②的实验事实,可推断它们的化学式为:(1)A
(2)加入足量盐酸后D中反应的离子方程式:
(3)写出C与NaOH溶液反应的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】甲、乙两个实验小组同学分别用酸性KMnO4和H2C2O4(草酸)溶液反应来探究影响反应速率的因素:
Ⅰ.甲组同学欲通过如图装置探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):

(1)写出酸性KMnO4溶液和H2C2O4(草酸)溶液反应的离子方程式___________ 。
(2)相同时间内针筒中所得CO2的体积大小关系是①___________ ②(填“>”、“<”或“=”)。
(3)该小组同学发现反应速率总是如下图所示,其中t1~t2时间内速率变快的主要原因可能是:①产物Mn2+对该反应有催化作用;②___________ 。

Ⅱ.乙组同学设计了如下实验
实验室中可供选择的试剂为:0.02mol·L-1酸性KMnO4溶液、0.1mol·L-1酸性KMnO4溶液、0.01mol·L-1H2C2O4溶液、0.1mol·L-1H2C2O4溶液。试回答下列问题:
(4)依据该组同学的设计思路,表中数据a=___________ 、b=___________ (在所给试剂中选择)
(5)根据实验A和B可探究___________ (填外部因素)对化学反应速率的影响,则V1=___________ 、V2=___________ 、T1=___________
(6)若t2<8,则由此实验可以得出的结论是___________ 。
Ⅰ.甲组同学欲通过如图装置探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):

| 实验序号 | A溶液 | B溶液 |
| ① | 20mL0.1mol/LH2C2O4溶液 | 30mL0.01mol/LKMnO4溶液 |
| ② | 20mL0.2mol/LH2C2O4溶液 | 30mL0.01mol/LKMnO4溶液 |
(2)相同时间内针筒中所得CO2的体积大小关系是①
(3)该小组同学发现反应速率总是如下图所示,其中t1~t2时间内速率变快的主要原因可能是:①产物Mn2+对该反应有催化作用;②

Ⅱ.乙组同学设计了如下实验
| 实验序号 | 实验温度/K | 酸性KMnO4溶液 | H2C2O4溶液 | H2O | 溶液颜色褪至无色所需时间/s | ||
| V/mL | c/mol·L-1 | V/mL | c/mol·L-1 | V/mL | |||
| A | 293 | 2 | a | 4 | b | 0 | t1 |
| B | T1 | 2 | a | 3 | b | V1 | 8 |
| C | 313 | 2 | a | V2 | b | 1 | t2 |
(4)依据该组同学的设计思路,表中数据a=
(5)根据实验A和B可探究
(6)若t2<8,则由此实验可以得出的结论是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】ZnS可用作分析试剂、荧光粉的基质、光导体材料。25℃时,实验室以含锌废液(主要成分为 ,含少量的
,含少量的 、
、 )为原料制备活性ZnS的流程如图所示:
)为原料制备活性ZnS的流程如图所示:

已知:①25℃时溶液中金属离子开始沉淀和完全沉淀的pH如表所示:
②25℃时,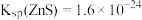 、
、 、
、 。
。
请回答下列问题:
(1)“氧化除锰”阶段生成 的离子方程式为
的离子方程式为______ ;不能用 代替
代替 的原因为
的原因为______ 。
(2)“除铁”时需调节溶液的pH。调pH时Zn不能代替ZnO,原因是______ 。
(3)“沉锌”时若用 代替
代替 可能导致的后果是
可能导致的后果是______ 。
(4)理论计算说明,“沉锌”时用 代替
代替 具有可行性,则用
具有可行性,则用 代替
代替 时,反应的平衡常数为
时,反应的平衡常数为______ 。
 ,含少量的
,含少量的 、
、 )为原料制备活性ZnS的流程如图所示:
)为原料制备活性ZnS的流程如图所示:
已知:①25℃时溶液中金属离子开始沉淀和完全沉淀的pH如表所示:
物质 |
|
|
|
开始沉淀的pH | 1.9 | 6.8 | 6.2 |
完全沉淀的pH | 3.2 | 8.3 | 8.2 |
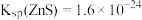 、
、 、
、 。
。请回答下列问题:
(1)“氧化除锰”阶段生成
 的离子方程式为
的离子方程式为 代替
代替 的原因为
的原因为(2)“除铁”时需调节溶液的pH。调pH时Zn不能代替ZnO,原因是
(3)“沉锌”时若用
 代替
代替 可能导致的后果是
可能导致的后果是(4)理论计算说明,“沉锌”时用
 代替
代替 具有可行性,则用
具有可行性,则用 代替
代替 时,反应的平衡常数为
时,反应的平衡常数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】碲化钠(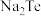 )可用作有机合成试剂及缩合反应中的催化剂。以碲铅矿(主要成分为
)可用作有机合成试剂及缩合反应中的催化剂。以碲铅矿(主要成分为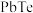 )和粗盐(含
)和粗盐(含 、
、 及一些硫酸盐、泥沙)为原料制备碲化钠的工艺流程如下。
及一些硫酸盐、泥沙)为原料制备碲化钠的工艺流程如下。
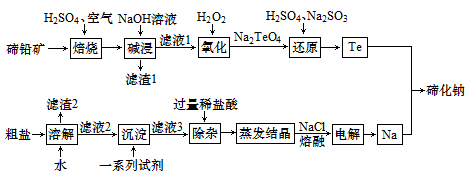
(1)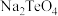 中Te的化合价为
中Te的化合价为________ 。
(2)铅的质子数为82,则铅在元素周期表中的位置是________ 。
(3)“蒸发结晶”时,用到的仪器有________ 、________ 、酒精灯、铁架台。
(4)“焙烧”后,碲主要以 的形式存在,写出“焙烧”时反应的化学方程式
的形式存在,写出“焙烧”时反应的化学方程式________________ 。
(5)根据“氧化”和“还原”两步反应, 、
、 、
、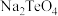 的氧化性由弱到强的顺序为
的氧化性由弱到强的顺序为________ ,“还原”步骤中还原剂与氧化剂的物质的量之比为________ 。
(6)若制得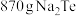 ,理论上“电解”产生
,理论上“电解”产生 的体积为
的体积为________ (标准状况下)。
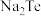 )可用作有机合成试剂及缩合反应中的催化剂。以碲铅矿(主要成分为
)可用作有机合成试剂及缩合反应中的催化剂。以碲铅矿(主要成分为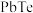 )和粗盐(含
)和粗盐(含 、
、 及一些硫酸盐、泥沙)为原料制备碲化钠的工艺流程如下。
及一些硫酸盐、泥沙)为原料制备碲化钠的工艺流程如下。
(1)
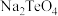 中Te的化合价为
中Te的化合价为(2)铅的质子数为82,则铅在元素周期表中的位置是
(3)“蒸发结晶”时,用到的仪器有
(4)“焙烧”后,碲主要以
 的形式存在,写出“焙烧”时反应的化学方程式
的形式存在,写出“焙烧”时反应的化学方程式(5)根据“氧化”和“还原”两步反应,
 、
、 、
、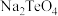 的氧化性由弱到强的顺序为
的氧化性由弱到强的顺序为(6)若制得
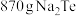 ,理论上“电解”产生
,理论上“电解”产生 的体积为
的体积为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】氯化铬晶体(CrCl3•6H2O)是一种重要的工业原料,某实验小组用甲醇在酸性条件下还原工业铬酸钠(Na2CrO4)制备CrCl3•6H2O,实验装置(夹持装置略)和步骤如下:

Ⅰ.将1mol工业铬酸钠、1mol甲醇、400mL水依次加入三口烧瓶中;
Ⅱ.升温至120℃时,缓慢滴加足量盐酸,保持温度在100℃反应三小时;
Ⅲ.待反应液冷却后,用NaOH溶液调节pH为6.5~7.5,得到Cr(OH)3沉淀;
Ⅳ.多次洗涤沉淀后加入过量(理论用量的1.1倍)盐酸溶解……洗涤干燥得到CrCl3•6H2O晶体。
已知:①CrCl3•6H2O不溶于乙醚,易溶于水、乙醇,易水解;
②甲醇是无色液体,有毒,沸点64.7℃,易燃。
回答下列问题:
(1)仪器a的名称为___________ ,仪器 b的主要作用除导气外,还有 ___________ 。
(2)步骤Ⅱ的反应会有CO2产生,请写出反应的离子方程式:___________ 。
(3)步骤Ⅳ中盐酸需要过量的原因是___________ 。
(4)补充完整步骤IV中加盐酸后从溶液中获得CrCl3•6H2O晶体的实验操作:___________ 、洗涤、干燥。
(5)产品中CrCl3•6H2O纯度的测定:
(ⅰ)称取0.50000 g产品溶于水并于250 mL容量瓶中定容;
(ⅱ)取25.00mL(ⅰ)中溶液于锥形瓶中,加入稍过量的Na2O2,适当稀释,再加入过量的H2SO4酸化,充分反应后加热至沸腾,Cr3+完全氧化为Cr2O ;再加入过量的KI固体,加塞摇匀,使铬完全以Cr3+形式存在;
;再加入过量的KI固体,加塞摇匀,使铬完全以Cr3+形式存在;
(ⅲ)加入适量淀粉溶液,用0.02000 mol•L﹣1 Na2S2O3标准溶液滴定至终点,平行测定三次,平均消耗Na2S2O3标准溶液24.00 mL(已知:2Na2S2O3+I2 Na2S4O6+2NaI)。
Na2S4O6+2NaI)。
①(ⅱ)中加入KI固体前要将溶液加热煮沸,其主要原因是___________ 。
②产品中CrCl3•6H2O(M=266.5 g/mol)的质量分数为___________ (保留三位有效数字)。
③(ⅲ)中未用标准液润洗滴定管,结果将___________ (填“偏大”“偏小”或“无影响”)。

Ⅰ.将1mol工业铬酸钠、1mol甲醇、400mL水依次加入三口烧瓶中;
Ⅱ.升温至120℃时,缓慢滴加足量盐酸,保持温度在100℃反应三小时;
Ⅲ.待反应液冷却后,用NaOH溶液调节pH为6.5~7.5,得到Cr(OH)3沉淀;
Ⅳ.多次洗涤沉淀后加入过量(理论用量的1.1倍)盐酸溶解……洗涤干燥得到CrCl3•6H2O晶体。
已知:①CrCl3•6H2O不溶于乙醚,易溶于水、乙醇,易水解;
②甲醇是无色液体,有毒,沸点64.7℃,易燃。
回答下列问题:
(1)仪器a的名称为
(2)步骤Ⅱ的反应会有CO2产生,请写出反应的离子方程式:
(3)步骤Ⅳ中盐酸需要过量的原因是
(4)补充完整步骤IV中加盐酸后从溶液中获得CrCl3•6H2O晶体的实验操作:
(5)产品中CrCl3•6H2O纯度的测定:
(ⅰ)称取0.50000 g产品溶于水并于250 mL容量瓶中定容;
(ⅱ)取25.00mL(ⅰ)中溶液于锥形瓶中,加入稍过量的Na2O2,适当稀释,再加入过量的H2SO4酸化,充分反应后加热至沸腾,Cr3+完全氧化为Cr2O
 ;再加入过量的KI固体,加塞摇匀,使铬完全以Cr3+形式存在;
;再加入过量的KI固体,加塞摇匀,使铬完全以Cr3+形式存在;(ⅲ)加入适量淀粉溶液,用0.02000 mol•L﹣1 Na2S2O3标准溶液滴定至终点,平行测定三次,平均消耗Na2S2O3标准溶液24.00 mL(已知:2Na2S2O3+I2
 Na2S4O6+2NaI)。
Na2S4O6+2NaI)。①(ⅱ)中加入KI固体前要将溶液加热煮沸,其主要原因是
②产品中CrCl3•6H2O(M=266.5 g/mol)的质量分数为
③(ⅲ)中未用标准液润洗滴定管,结果将
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】硫化物是自然界硫循环中的重要物质。回答下列问题:
(1)反应2H2S(g)=2H2(g)+S2(g) △H>0在______ (填“高温”“低温”或“任何温度”)下能自发进行。
(2)闪锌矿转化为CuS矿的反应为ZnS(s)+Cu2+(aq)=CuS(s)+Zn2+(aq),该反应的平衡常数K=__________ [用含Ksp(CuS)、Ksp(ZnS)的代数式表示]。
(3)25℃时,某混合溶液中c(H2S)+c(HS-)+c(S2-)=0.01 mol·L-1,Ka1、Ka2分别为H2S的一级电离常数和二级电离常数;lgc(H2S)、lgc(HS-)、lgc(S2-)随pH变化的关系如图所示:

①在水溶液中H2S的电离方程式为__________ 、__________ 。
②图中c表示的含硫微粒是____________ (填离子符号)。
③H2S的Ka1=______ mol·L-1。
④图中M点的pH=______ (用含lgKa1、lgKa2的代数式表示)。
(1)反应2H2S(g)=2H2(g)+S2(g) △H>0在
(2)闪锌矿转化为CuS矿的反应为ZnS(s)+Cu2+(aq)=CuS(s)+Zn2+(aq),该反应的平衡常数K=
(3)25℃时,某混合溶液中c(H2S)+c(HS-)+c(S2-)=0.01 mol·L-1,Ka1、Ka2分别为H2S的一级电离常数和二级电离常数;lgc(H2S)、lgc(HS-)、lgc(S2-)随pH变化的关系如图所示:

①在水溶液中H2S的电离方程式为
②图中c表示的含硫微粒是
③H2S的Ka1=
④图中M点的pH=
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】锰及其化合物间的转化如下图。

请回答下列问题:
(1)反应①发生的主要化学反应的方程式为:___________ 。反应③发生的主要化学反应的方程式为:___________ 。
(2)粗KMnO4晶体中含有少量的K2CO3,检验其中的少量CO32-用______ 试剂;为了得到纯的KMnO4晶体,操作Ⅲ的名称为___________ 。
(3)测定高锰酸钾样品纯度采用硫酸锰滴定:向高锰酸钾溶液中滴加硫酸锰溶液,产生黑色沉淀。当高锰酸钾溶液由紫红色刚好褪色且半分钟不恢复,表明达到滴定终点。写出该反应的离子方程式:___________ 。
(4)已知:常温下,Ksp[Mn(OH)2]=2.4×10-13。工业上,调节pH可以沉淀废水中Mn2+,当pH=10时,溶液中c(Mn2+)=___________________ 。
(5)如图,用Fe、C作电极电解含MnO4-的污水,使之转化为沉淀除去。A电极是_____ (填“Fe”或“C”),污水中MnO4-转化为沉淀除去的离子方程式为___________ 。

请回答下列问题:
(1)反应①发生的主要化学反应的方程式为:
(2)粗KMnO4晶体中含有少量的K2CO3,检验其中的少量CO32-用
(3)测定高锰酸钾样品纯度采用硫酸锰滴定:向高锰酸钾溶液中滴加硫酸锰溶液,产生黑色沉淀。当高锰酸钾溶液由紫红色刚好褪色且半分钟不恢复,表明达到滴定终点。写出该反应的离子方程式:
(4)已知:常温下,Ksp[Mn(OH)2]=2.4×10-13。工业上,调节pH可以沉淀废水中Mn2+,当pH=10时,溶液中c(Mn2+)=
(5)如图,用Fe、C作电极电解含MnO4-的污水,使之转化为沉淀除去。A电极是

您最近一年使用:0次
【推荐3】某科研机构用NaOH溶液吸收硫酸工业废气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到某种副产物,其原理如图所示(电极材料为石墨)。

(1) 当有1 mol Na+通过阳离子交换膜时,a极生成气体____ L(标准状况),阳极的电极反应式是_____ 。
(2)稀NaOH溶液的作用是________ ,B处流出较浓的NaOH溶液,C处流出的是___________ 。
(3)在标准状况下,若用甲烷-空气燃料电池做电源,处理含SO2 20%(体积分数)的废气40 m3,理论上需要消耗甲烷_______ m3。
已知:Ksp[Fe(OH)2]=8×10-16,Ksp[Fe(OH)3]=1×10-38,Ksp[Zn(OH)2]=4×10-17,回答下列问题:
(4)Fe(OH)3溶解平衡常数表达式Ksp[Fe(OH)3]=___________________ 。
(5)向等物质的量浓度的Zn2+、Fe3+的混合溶液中逐滴加入NaOH溶液,最先产生的沉淀是______ 。常温下,若使0.4 mol·L-1的ZnCl2溶液中的Zn2+开始沉淀,应加入NaOH溶液调整溶液的pH为______ 。
(6)要除去ZnCl2酸性溶液中混有的少量Fe2+,应先向混合溶液中加入适量_________ 溶液,再加入________ (填下列选项序号)调节溶液的pH,最后过滤。
a. NH3·H2O b. Na2CO3 c. ZnO d. ZnCO3

(1) 当有1 mol Na+通过阳离子交换膜时,a极生成气体
(2)稀NaOH溶液的作用是
(3)在标准状况下,若用甲烷-空气燃料电池做电源,处理含SO2 20%(体积分数)的废气40 m3,理论上需要消耗甲烷
已知:Ksp[Fe(OH)2]=8×10-16,Ksp[Fe(OH)3]=1×10-38,Ksp[Zn(OH)2]=4×10-17,回答下列问题:
(4)Fe(OH)3溶解平衡常数表达式Ksp[Fe(OH)3]=
(5)向等物质的量浓度的Zn2+、Fe3+的混合溶液中逐滴加入NaOH溶液,最先产生的沉淀是
(6)要除去ZnCl2酸性溶液中混有的少量Fe2+,应先向混合溶液中加入适量
a. NH3·H2O b. Na2CO3 c. ZnO d. ZnCO3
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】钠是活泼的碱金属元素,钠及其化合物在生产和生活中有广泛的应用。叠氮化钠(NaN3)被广泛应用于汽车安全气囊,某化学小组同学对其进行下列研究。
[查阅资料]
i.NaN3受撞击会生成Na、N2。
ii.NaN3遇盐酸、H2SO4溶液无气体生成。
iii.叠氮化钠(NaN3)的一种生产工艺流程如下:

[问题探究]
(1)汽车受撞击后,30毫秒内引发NaN3迅速分解,该反应的化学方程式为_______ ;
(2)①反应器(Ⅰ)发生反应的基本反应类型为_______ ;液态氨需过量,其原因是________ 。
②反应器(Ⅱ)中反应的化学方程式为_______ 。
(3)工业级NaN3中常含有少量的Na2CO3,其原因是_______ (用化学方程式表示)。
[查阅资料]
i.NaN3受撞击会生成Na、N2。
ii.NaN3遇盐酸、H2SO4溶液无气体生成。
iii.叠氮化钠(NaN3)的一种生产工艺流程如下:

[问题探究]
(1)汽车受撞击后,30毫秒内引发NaN3迅速分解,该反应的化学方程式为
(2)①反应器(Ⅰ)发生反应的基本反应类型为
②反应器(Ⅱ)中反应的化学方程式为
(3)工业级NaN3中常含有少量的Na2CO3,其原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】Na2S2O3俗称大苏打(海波),是重要的化工原料,无色易溶于水,不溶于乙醇,在中性或碱性环境中稳定,在40~45℃熔化,48℃分解。实验室用Na2SO3和过量硫粉(不溶于水,可溶于乙醇)在水溶液中加热反应制取Na2S2O3•5H2O晶体的步骤如下:
(图1是有关物质的溶解度曲线)[反应原理:Na2SO3(aq)+S(s) Na2S2O3(aq)]
Na2S2O3(aq)]
①称取一定量的Na2SO3于烧杯中,溶于水。
②另取过量的硫粉,用少许乙醇润湿后,加到上述溶液中。
③如图2所示(部分装置略去),水浴加热,微沸,反应后趁热过滤。
④滤液在经过相关实验操作后析出Na2S2O3•5H2O晶体。
⑤进行减压过滤并低温干燥。

(1)Na2S2O3是一种强碱弱酸盐,则其溶液显________ (填“酸性”、“中性”、“碱性”),原因是________ (用离子方程式表示)。
(2)图2中,仪器B的名称是________ 。
(3)实验步骤②中,加入的硫粉用乙醇润湿的目的是________ 。
(4)实验步骤③中,趁热过滤的原因是________ 。
(5)实验步骤④中,应采取的相关实验操作为________ 。
(6)实验步骤⑤中,采用低温干燥的目的是________ 。
(7)产品中除了有未反应的Na2SO3外,最可能存在的无机杂质是________ 。
(图1是有关物质的溶解度曲线)[反应原理:Na2SO3(aq)+S(s)
 Na2S2O3(aq)]
Na2S2O3(aq)]①称取一定量的Na2SO3于烧杯中,溶于水。
②另取过量的硫粉,用少许乙醇润湿后,加到上述溶液中。
③如图2所示(部分装置略去),水浴加热,微沸,反应后趁热过滤。
④滤液在经过相关实验操作后析出Na2S2O3•5H2O晶体。
⑤进行减压过滤并低温干燥。

(1)Na2S2O3是一种强碱弱酸盐,则其溶液显
(2)图2中,仪器B的名称是
(3)实验步骤②中,加入的硫粉用乙醇润湿的目的是
(4)实验步骤③中,趁热过滤的原因是
(5)实验步骤④中,应采取的相关实验操作为
(6)实验步骤⑤中,采用低温干燥的目的是
(7)产品中除了有未反应的Na2SO3外,最可能存在的无机杂质是
您最近一年使用:0次