实验室用浓盐酸和 制
制 ,并以干燥的
,并以干燥的 为原料制备
为原料制备 ,装置如下图所示。回答下列问题:
,装置如下图所示。回答下列问题:
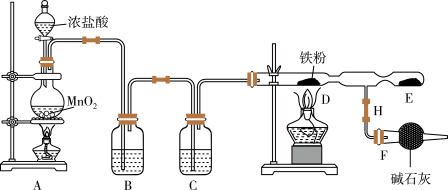
已知: 固体易升华,易吸收水分而潮解变质。请回答下列问题:
固体易升华,易吸收水分而潮解变质。请回答下列问题:
(1)连接好仪器后首先应进行的操作是_______ ;图中盛放碱石灰的仪器是_______ 。
(2)写出装置A中发生的离子方程式_______ 。
(3)装置B中盛放的试剂是_______ 。F装置所起的作用是_______ 。
(4)实验时,先点燃_______ 处的酒精灯,再点燃_______ 处酒精灯,D处发生的现象是_______ 。
(5)已知 与浓盐酸在常温下反应就可制取氯气:_______
与浓盐酸在常温下反应就可制取氯气:_______ _______
_______ (浓)= _______
(浓)= _______ _______
_______ _______
_______ _______
_______
①配平上述化学方程式,并用单线桥标出电子转移的情况。_________
②当生成标准状况下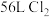 时对应转移的电子数为
时对应转移的电子数为_______ 。
 制
制 ,并以干燥的
,并以干燥的 为原料制备
为原料制备 ,装置如下图所示。回答下列问题:
,装置如下图所示。回答下列问题:
已知:
 固体易升华,易吸收水分而潮解变质。请回答下列问题:
固体易升华,易吸收水分而潮解变质。请回答下列问题:(1)连接好仪器后首先应进行的操作是
(2)写出装置A中发生的离子方程式
(3)装置B中盛放的试剂是
(4)实验时,先点燃
(5)已知
 与浓盐酸在常温下反应就可制取氯气:_______
与浓盐酸在常温下反应就可制取氯气:_______ _______
_______ (浓)= _______
(浓)= _______ _______
_______ _______
_______ _______
_______
①配平上述化学方程式,并用单线桥标出电子转移的情况。
②当生成标准状况下
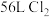 时对应转移的电子数为
时对应转移的电子数为
更新时间:2023-01-09 23:40:26
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】实验室里除了用二氧化锰和浓盐酸加热制取氯气,也可以在常温下利用反应: 制取并收集纯净、干燥的氯气,装置如图所示:
制取并收集纯净、干燥的氯气,装置如图所示:
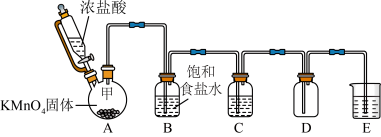
(1)①装置A中甲仪器的名称是_______ 。
②装置B的作用是_______ 。
③装置C中盛装的药品是_______ 。
④装置E中发生反应的化学方程是_______ 。
(2) 。若产生
。若产生 ,则转移的电子数目为
,则转移的电子数目为_______ ,浓盐酸体现了_______ 性质(选填字母编号)。
A.酸性 B.碱性 C.氧化性 D.还原性
(3)在该反应中,被还原的元素是_______ ,氧化剂与还原剂的物质的量之比为_______ 。
 制取并收集纯净、干燥的氯气,装置如图所示:
制取并收集纯净、干燥的氯气,装置如图所示:
(1)①装置A中甲仪器的名称是
②装置B的作用是
③装置C中盛装的药品是
④装置E中发生反应的化学方程是
(2)
 。若产生
。若产生 ,则转移的电子数目为
,则转移的电子数目为A.酸性 B.碱性 C.氧化性 D.还原性
(3)在该反应中,被还原的元素是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】 常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。
常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。 和
和 (亚氯酸钠)均具有漂白性,工业上由
(亚氯酸钠)均具有漂白性,工业上由 气体制取
气体制取 固体的工艺流程如图所示:
固体的工艺流程如图所示:

请回答下列问题:
(1)吸收器中生成 的离子方程式为(补充完整):
的离子方程式为(补充完整):_____ 。
①______ ______
______ ______=______
______=______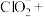 ______
______ ______
______
②此氧化还原反应中,双氧水表现______ 性;若 完全反应,
完全反应,______ (填“得到”或“失去”)的电子数为______ 个,生成的气体产物的体积为__________ (标况下)。
(2)为了探究 和
和 的氧化性或还原性,某兴趣小组进行下列2个实验,请完成实验报告。实验②可供选用的试剂有:
的氧化性或还原性,某兴趣小组进行下列2个实验,请完成实验报告。实验②可供选用的试剂有: 溶液、KI溶液、淀粉溶液、
溶液、KI溶液、淀粉溶液、 酸性溶液
酸性溶液
(3)工业上可以用草酸( ,二元弱酸)还原
,二元弱酸)还原 的方法生产
的方法生产 ,草酸被氧化为
,草酸被氧化为 ,请写出该反应的离子方程式
,请写出该反应的离子方程式__________________ 。
(4)工业上制取 (亚氯酸钠)固体,理论上至少需要常温常压下
(亚氯酸钠)固体,理论上至少需要常温常压下 气体的体积为
气体的体积为______ L。(常温常压下,气体摩尔体积为24.5L/mol,计算结果保留两位小数)。
 常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。
常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。 和
和 (亚氯酸钠)均具有漂白性,工业上由
(亚氯酸钠)均具有漂白性,工业上由 气体制取
气体制取 固体的工艺流程如图所示:
固体的工艺流程如图所示:
请回答下列问题:
(1)吸收器中生成
 的离子方程式为(补充完整):
的离子方程式为(补充完整):①______
 ______
______ ______=______
______=______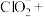 ______
______ ______
______②此氧化还原反应中,双氧水表现
 完全反应,
完全反应,(2)为了探究
 和
和 的氧化性或还原性,某兴趣小组进行下列2个实验,请完成实验报告。实验②可供选用的试剂有:
的氧化性或还原性,某兴趣小组进行下列2个实验,请完成实验报告。实验②可供选用的试剂有: 溶液、KI溶液、淀粉溶液、
溶液、KI溶液、淀粉溶液、 酸性溶液
酸性溶液序号 | 实验操作 | 实验现象 | 实验结论 |
① | 将 通入足量KI溶液中,加入稀硫酸,再加入几滴淀粉溶液 通入足量KI溶液中,加入稀硫酸,再加入几滴淀粉溶液 | ||
② |  溶液 溶液 |
|
 ,二元弱酸)还原
,二元弱酸)还原 的方法生产
的方法生产 ,草酸被氧化为
,草酸被氧化为 ,请写出该反应的离子方程式
,请写出该反应的离子方程式(4)工业上制取
 (亚氯酸钠)固体,理论上至少需要常温常压下
(亚氯酸钠)固体,理论上至少需要常温常压下 气体的体积为
气体的体积为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】(Ⅰ)按要求回答下列问题:
(1)实验室制备氨气,下列方法中可以选用的是___________ ;
a.固态氯化铵加热分解 b.浓氨水中加入固体氢氧化钠
c.加热浓氨水 d.固态氯化铵与氢氧化钙混合加热
(2)氨的水溶液叫做氨水,用离子方程式表示氨水呈碱性的原因___________ ;
(3)NH3常用于检验氯气管道是否泄漏,写出反应的化学方程式___________ 。
(Ⅱ)A、B、C、D、E为中学化学常见的单质或化合物,相互转化关系如图所示(部分产物略去)。
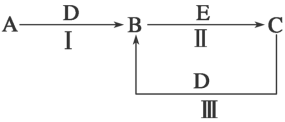
已知:A是能使湿润红色石蕊试纸变蓝的气体;C、D均为空气的主要成分;E是一种有毒气体。 回答下列问题:
(1)C的电子式为___________ ;
(2)写出反应I的化学方程式___________ ;
(3)写出反应Ⅱ的化学方程式___________ 。
(Ⅲ)将57.6克的铜投入200毫升的硝酸溶液中恰好反应完全,产生标准状况下的NO2、NO共1.4 mol。
(1)写出刚开始反应的化学方程式___________ ;
(2)求硝酸的浓度___________ mol·L-1;
(3)将生成的气体收集在大试管中,然后倒扣在水中,写出二氧化氮与水反应的化学方程式___________ ,若往试管中通入氧气让液体充满试管,则通入氧气的物质的量___________ mol。
(1)实验室制备氨气,下列方法中可以选用的是
a.固态氯化铵加热分解 b.浓氨水中加入固体氢氧化钠
c.加热浓氨水 d.固态氯化铵与氢氧化钙混合加热
(2)氨的水溶液叫做氨水,用离子方程式表示氨水呈碱性的原因
(3)NH3常用于检验氯气管道是否泄漏,写出反应的化学方程式
(Ⅱ)A、B、C、D、E为中学化学常见的单质或化合物,相互转化关系如图所示(部分产物略去)。

已知:A是能使湿润红色石蕊试纸变蓝的气体;C、D均为空气的主要成分;E是一种有毒气体。 回答下列问题:
(1)C的电子式为
(2)写出反应I的化学方程式
(3)写出反应Ⅱ的化学方程式
(Ⅲ)将57.6克的铜投入200毫升的硝酸溶液中恰好反应完全,产生标准状况下的NO2、NO共1.4 mol。
(1)写出刚开始反应的化学方程式
(2)求硝酸的浓度
(3)将生成的气体收集在大试管中,然后倒扣在水中,写出二氧化氮与水反应的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】铅酸蓄电池在生产、生活中使用广泛,其放电过程中,发生反应的化学方程式为 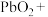
 废铅酸蓄电池中回收铅的一种工艺流程如图。
废铅酸蓄电池中回收铅的一种工艺流程如图。

回答下列问题:
(1)对于反应 该反应中Pb体现了
该反应中Pb体现了_______ (填“还原性”或“氧化性”)。
(2)Na2CO3在水中的电离方程式为_______ 。
(3)废硫酸直接排放会污染环境:
①可用氟磷灰石[Ca5(PO4)3F]进行处理,反应的化学方程式为
 相对分子质量:H2SO4
相对分子质量:H2SO4_______ (填“>”或“<”)HF。
②也可用烧碱溶液来处理废硫酸,发生反应的离子方程式为_______ ,该反应的基本反应类型为_______ 。
(4)若滤渣的主要成分为PbCO3,则PbCO3与焦炭反应的化学方程式为_______ (假设杂质不参与反应)。
(5)写出铅在生活中的一种用途:_______ 。
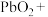
 废铅酸蓄电池中回收铅的一种工艺流程如图。
废铅酸蓄电池中回收铅的一种工艺流程如图。
回答下列问题:
(1)对于反应
 该反应中Pb体现了
该反应中Pb体现了(2)Na2CO3在水中的电离方程式为
(3)废硫酸直接排放会污染环境:
①可用氟磷灰石[Ca5(PO4)3F]进行处理,反应的化学方程式为

 相对分子质量:H2SO4
相对分子质量:H2SO4②也可用烧碱溶液来处理废硫酸,发生反应的离子方程式为
(4)若滤渣的主要成分为PbCO3,则PbCO3与焦炭反应的化学方程式为
(5)写出铅在生活中的一种用途:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】X、Y、Z和W代表原子序数依次增大的四种短周期元素,它们满足以下条件
①元素周期表中,Z与Y相邻,Z与W相邻;
②X分别与Y、Z、W可组成化学式为YX3,X2Z和X2W三种共价化合物
请填空:
(1)X2W的结构式是___________
(2)X、Y和Z组成的一种化合物是强酸。写出该酸的稀溶液与铜反应的离子方程式是___________ ,由H、N、O组成一种离子化合物其化学式为___________ 。
(3)X、Y、Z和W组成一种化合物,其原子个数之比为5∶1∶3∶1;该物质有还原性。
①写出该化合物与少量稀NaOH溶液反应的离子方程式是___________ 。
②请设计实验证明该化合物具有还原性___________ 。
①元素周期表中,Z与Y相邻,Z与W相邻;
②X分别与Y、Z、W可组成化学式为YX3,X2Z和X2W三种共价化合物
请填空:
(1)X2W的结构式是
(2)X、Y和Z组成的一种化合物是强酸。写出该酸的稀溶液与铜反应的离子方程式是
(3)X、Y、Z和W组成一种化合物,其原子个数之比为5∶1∶3∶1;该物质有还原性。
①写出该化合物与少量稀NaOH溶液反应的离子方程式是
②请设计实验证明该化合物具有还原性
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】利用制硫酸产生的矿渣(主要成分为 、
、 、
、 、
、 、
、 等)制备高纯氧化铁和副产品硫酸铵的流程如下:
等)制备高纯氧化铁和副产品硫酸铵的流程如下:

已知硫酸铵在水中的溶解度: 时
时 ,
, 时
时
(1)矿渣酸浸时需加适当过量的稀硫酸的目的是___________ 。
(2)“滤液2”中加入碳酸氢铵溶液,写出生成 的离子方程式
的离子方程式___________ ,获得的 需要用水洗涤,检验沉淀是否洗涤干净的方法是
需要用水洗涤,检验沉淀是否洗涤干净的方法是___________ 。
(3)“滤渣2”的成分为铁粉和___________ 。
(4)“滤液3”中持续通入空气并调 的目的是“除杂”,持续入空气的作用是
的目的是“除杂”,持续入空气的作用是____ 。
(5)“滤液4”经过_____ 、过滤得到粗产品,浓缩时若温度过高,产品中将混有少量 ,试用化学平衡移动原理解释其原因
,试用化学平衡移动原理解释其原因___________ 。
 、
、 、
、 、
、 、
、 等)制备高纯氧化铁和副产品硫酸铵的流程如下:
等)制备高纯氧化铁和副产品硫酸铵的流程如下:
已知硫酸铵在水中的溶解度:
 时
时 ,
, 时
时
(1)矿渣酸浸时需加适当过量的稀硫酸的目的是
(2)“滤液2”中加入碳酸氢铵溶液,写出生成
 的离子方程式
的离子方程式 需要用水洗涤,检验沉淀是否洗涤干净的方法是
需要用水洗涤,检验沉淀是否洗涤干净的方法是(3)“滤渣2”的成分为铁粉和
(4)“滤液3”中持续通入空气并调
 的目的是“除杂”,持续入空气的作用是
的目的是“除杂”,持续入空气的作用是(5)“滤液4”经过
 ,试用化学平衡移动原理解释其原因
,试用化学平衡移动原理解释其原因
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】如图是硫铁矿烧渣(主要成分为Fe2O3、Fe3O4、FeO、SiO2)为原料制备高纯氧化铁的生产流程示意图:

请回答下列问题:
(1)酸浸时,将硫铁矿烧渣粉碎的原因是___________ 。
(2)酸浸、过滤后滤液A中的金属阳离子是___________ 。
(3)煅烧FeCO3生成产品I的化学方程式为___________ 。
(4)产品Ⅱ的化学式为___________ 。
(5)写出步骤Ⅳ反应的离子方程式___________ 。

请回答下列问题:
(1)酸浸时,将硫铁矿烧渣粉碎的原因是
(2)酸浸、过滤后滤液A中的金属阳离子是
(3)煅烧FeCO3生成产品I的化学方程式为
(4)产品Ⅱ的化学式为
(5)写出步骤Ⅳ反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】二氧化氯常用作氧化剂、脱臭剂、保鲜剂、漂白剂等。因其具有对人体及动物无害以及对环境不造成二次污染等特点备受人们青睐。某实验室设计如图装置制取并收集 且探究其性质。
且探究其性质。
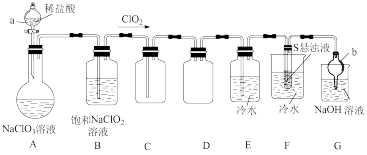
已知:
① 是一种易溶于水的黄绿色气体,与冷水几乎不反应,与热水能反应,其熔点
是一种易溶于水的黄绿色气体,与冷水几乎不反应,与热水能反应,其熔点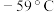 ,沸点
,沸点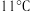 ,受热易分解;
,受热易分解;
②稀盐酸与 反应或
反应或 与
与 溶液反应均可制取
溶液反应均可制取 。
。
回答下列问题:
(1)仪器b的名称是___________ 。
(2)装置A中发生反应: +
+___________ 
 ,滴加稀盐酸时,应缓慢滴加,其主要原因是
,滴加稀盐酸时,应缓慢滴加,其主要原因是___________ 。
(3)根据(2)试分析装置B的作用:___________ (用化学方程式说明)。
(4)装置F中可得到两种强酸的混合溶液,该装置中的现象为___________ ,反应的化学方程式为___________ 。
(5)已知在酸性条件下 可发生反应生成
可发生反应生成 并释放出
并释放出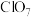 ,向
,向 溶液中滴加盐酸,反应剧烈,若将盐酸换成等
溶液中滴加盐酸,反应剧烈,若将盐酸换成等 的硫酸,开始反应缓慢,稍后一段时间产生气体速率迅速加快,产生气体速率迅速加快的原因是
的硫酸,开始反应缓慢,稍后一段时间产生气体速率迅速加快,产生气体速率迅速加快的原因是___________ 。
 且探究其性质。
且探究其性质。
已知:
①
 是一种易溶于水的黄绿色气体,与冷水几乎不反应,与热水能反应,其熔点
是一种易溶于水的黄绿色气体,与冷水几乎不反应,与热水能反应,其熔点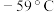 ,沸点
,沸点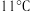 ,受热易分解;
,受热易分解;②稀盐酸与
 反应或
反应或 与
与 溶液反应均可制取
溶液反应均可制取 。
。回答下列问题:
(1)仪器b的名称是
(2)装置A中发生反应:
 +
+
 ,滴加稀盐酸时,应缓慢滴加,其主要原因是
,滴加稀盐酸时,应缓慢滴加,其主要原因是(3)根据(2)试分析装置B的作用:
(4)装置F中可得到两种强酸的混合溶液,该装置中的现象为
(5)已知在酸性条件下
 可发生反应生成
可发生反应生成 并释放出
并释放出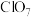 ,向
,向 溶液中滴加盐酸,反应剧烈,若将盐酸换成等
溶液中滴加盐酸,反应剧烈,若将盐酸换成等 的硫酸,开始反应缓慢,稍后一段时间产生气体速率迅速加快,产生气体速率迅速加快的原因是
的硫酸,开始反应缓慢,稍后一段时间产生气体速率迅速加快,产生气体速率迅速加快的原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】氯气的发现者是瑞典化学家舍勒。1774年,他正在研究软锰矿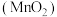 ,当他使软锰矿与浓盐酸混合并加热时,产生了一种黄绿色的气体。
,当他使软锰矿与浓盐酸混合并加热时,产生了一种黄绿色的气体。
I.为了进一步了解氯气的性质,同学甲提出可以在实验室中仿照舍勒的方法制备纯净的氯气,并设计了以下实验装置:

(1)发生装置中,反应的化学方程式为___________ 。
(2)为了在装置C中测试干燥氯气的漂白性,装置A中盛放的液体是___________ ,装置B中盛放的液体是___________ 。
(3)装置C中为干燥的红色布条,装置D中是湿润的红色布条,通入氯气后,布条颜色出现明显变化的装置为___________ ,因此,具有漂白性的物质是___________ ,其结构式为___________ 。
(4)若装置E中盛放的液体是 试液,该装置中发生反应的离子方程式为
试液,该装置中发生反应的离子方程式为___________ 、___________ 。
(5)若装置F中盛放的液体是淀粉碘化钾溶液,则实验现象为___________ ,反应的离子方程式为___________ 。
(6)同学乙认为同学甲的装置存在一定的问题,存在的问题和改进的方案为___________ 。
Ⅱ.同学乙查询了工业生产氯气的方法:先通过粗盐的提纯制得较为纯净的氯化钠,再通过电解精制饱和食盐水获得氯气,并且生产的氯气可以作为非常重要的工业原料。
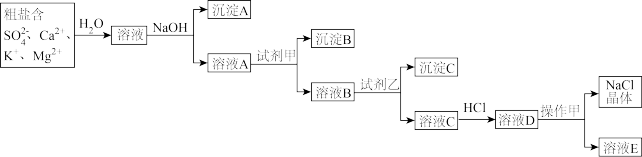
第一步:粗盐(含 、、
、、 、)的提纯
、)的提纯
(7) 、
、 、
、 的半径从大到小的顺序为
的半径从大到小的顺序为___________ 。(用离子符号表示)
(8)试剂乙的化学式为___________ ,目的是除去溶液B中的___________ (用离子符号表示)。
(9)用离子方程式表示溶液C中加入HCl后发生的化学反应:___________ 、___________ 。
第二步:用提纯后的食盐晶体制备化工产品烧碱和产品甲。

(10)设备甲中发生的反应的化学方程式为:___________ ,某电极生成的气体为一种无色气体,请写出此电极上发生的电极反应式___________ 。
(11)设备乙中发生的反应的火焰颜色为___________ ,产品甲为___________ 。
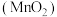 ,当他使软锰矿与浓盐酸混合并加热时,产生了一种黄绿色的气体。
,当他使软锰矿与浓盐酸混合并加热时,产生了一种黄绿色的气体。I.为了进一步了解氯气的性质,同学甲提出可以在实验室中仿照舍勒的方法制备纯净的氯气,并设计了以下实验装置:

(1)发生装置中,反应的化学方程式为
(2)为了在装置C中测试干燥氯气的漂白性,装置A中盛放的液体是
(3)装置C中为干燥的红色布条,装置D中是湿润的红色布条,通入氯气后,布条颜色出现明显变化的装置为
(4)若装置E中盛放的液体是
 试液,该装置中发生反应的离子方程式为
试液,该装置中发生反应的离子方程式为(5)若装置F中盛放的液体是淀粉碘化钾溶液,则实验现象为
(6)同学乙认为同学甲的装置存在一定的问题,存在的问题和改进的方案为
Ⅱ.同学乙查询了工业生产氯气的方法:先通过粗盐的提纯制得较为纯净的氯化钠,再通过电解精制饱和食盐水获得氯气,并且生产的氯气可以作为非常重要的工业原料。
第一步:粗盐(含
 、、
、、 、)的提纯
、)的提纯
(7)
 、
、 、
、 的半径从大到小的顺序为
的半径从大到小的顺序为(8)试剂乙的化学式为
(9)用离子方程式表示溶液C中加入HCl后发生的化学反应:
第二步:用提纯后的食盐晶体制备化工产品烧碱和产品甲。

(10)设备甲中发生的反应的化学方程式为:
(11)设备乙中发生的反应的火焰颜色为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】用MnO2和浓盐酸制取纯净干燥的氯气,并让氯气与铜粉反应制取纯净的无水CuCl2,装置如下图所示。
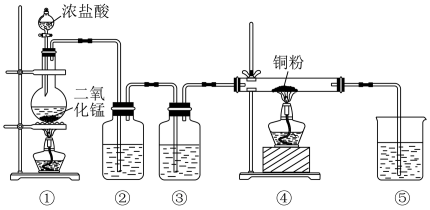
回答下列问题:
(1)写出盛放浓盐酸仪器的名称:_______ 。写出在①中发生反应的化学方程式为_______ 。甲同学用87gMnO2与足量浓盐酸反应制氯气,乙同学用足量MnO2与含146gHCl的浓盐酸反应制氯气,两者制得氯气_______ (填“甲多”,“乙多”,“一样多”)
(2)②中选用试剂是_______ ;③中选用试剂是_______ ;
(3)用如图装置验证氯气漂白性,图中B为开关。先打开B,在A处通入干燥氯气,C中红色布条颜色无变化;当关闭B时,C处红色布条颜色褪去。则D瓶中盛有的溶液可能是_______ 。
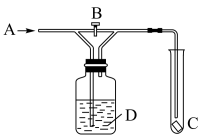
A.浓硫酸 B.浓NaOH溶液 C.饱和食盐水
(4)④中反应的化学方程式是_______ 。
(5)实验室用一种常见的碱溶液吸收氯气,写出⑤中反应的离子方程式是_______ 。

回答下列问题:
(1)写出盛放浓盐酸仪器的名称:
(2)②中选用试剂是
(3)用如图装置验证氯气漂白性,图中B为开关。先打开B,在A处通入干燥氯气,C中红色布条颜色无变化;当关闭B时,C处红色布条颜色褪去。则D瓶中盛有的溶液可能是

A.浓硫酸 B.浓NaOH溶液 C.饱和食盐水
(4)④中反应的化学方程式是
(5)实验室用一种常见的碱溶液吸收氯气,写出⑤中反应的离子方程式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】实验室利用如图所示的装置制备干燥、纯净的氯气。
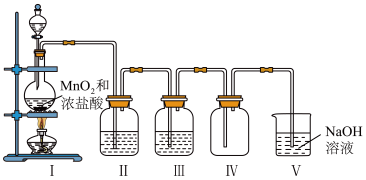
(1)写出装置I中制备氯气的化学方程式:_______ ,其中氧化剂与还原剂的个数比是_______ 。
(2)装置III中的药品是浓硫酸,其作用是_______ 。
(3)若用湿润的淀粉-KI试纸检验装置IV中收集的氯气,实验现象是_______ 。
(4)装置Ⅴ的作用是_______ ,发生反应的离子方程式为_______ ,当1个氯气分子参加反应时,转移的电子数是_______ 。
(5)若用10.0克软锰矿(主要成分是二氧化锰)与足量的浓盐酸反应制得7.1克氯气,则软锰矿中二氧化锰的质量分数是_______ 。

(1)写出装置I中制备氯气的化学方程式:
(2)装置III中的药品是浓硫酸,其作用是
(3)若用湿润的淀粉-KI试纸检验装置IV中收集的氯气,实验现象是
(4)装置Ⅴ的作用是
(5)若用10.0克软锰矿(主要成分是二氧化锰)与足量的浓盐酸反应制得7.1克氯气,则软锰矿中二氧化锰的质量分数是
您最近一年使用:0次




