解答题-实验探究题
|
较易(0.85)
|
解题方法
1 . 无土栽培试验需要用到 营养液,现配制
营养液,现配制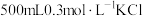 溶液。
溶液。
(1)根据计算,需用托盘天平称量 固体的质量为
固体的质量为___________ g。
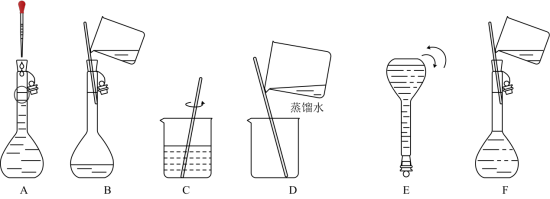
(2)如图所示的仪器中,配制溶液肯定不需要的是___________ (填标号),容量瓶除刻度线外还标有以下四项中的___________ (填序号)。
①温度②浓度③容积④压强___________ (填标号)
C→___________⟶___________→___________⟶___________⟶E___________ (填“偏大”“偏小”或“无影响”)。
(5)现需要配制两份成分完全 相同的某营养液各 ,配方如下表。
,配方如下表。
所配制的溶液中, 的物质的量浓度为
的物质的量浓度为___________  。
。
 营养液,现配制
营养液,现配制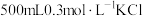 溶液。
溶液。(1)根据计算,需用托盘天平称量
 固体的质量为
固体的质量为(2)如图所示的仪器中,配制溶液肯定不需要的是
①温度②浓度③容积④压强

C→___________⟶___________→___________⟶___________⟶E
(5)现需要配制两份
 ,配方如下表。
,配方如下表。| 溶质 |  |  |  |
物质的量浓度 | 0.3 | 0.2 | 0.1 |
 的物质的量浓度为
的物质的量浓度为 。
。
您最近一年使用:0次
名校
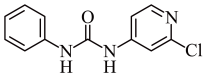
2 . 氯吡苯脲是一种常用的膨大剂,是经过国家批准的植物生长调节剂,实践证明长期使用对人体无害。其结构简式如图:
(1)按照核外电子的排布,氯吡苯脲中涉及的元素属于元素周期表的s区和_______ 区。
(2)氯吡苯脲的晶体中,氮原子的杂化轨道类型为_______ ,H原子可以与Cl原子通过_______ (填“s-pσ键”或“p-pσ键”)形成H-Cl共价键。
(3)氯吡苯脲晶体中,微粒间的作用力类型有_______ (填字母)。
A.离子键 B.极性键 C.非极性键 D.π键 E.氢键
(4)查文献可知,可用2-氯-4-氨基吡啶与异氰酸苯酯反应,生成氯吡苯脲。_______ 个σ键、断裂_______ 个π键。
(5)膨大剂能在动物体内代谢,其产物较为复杂,其中有H2O、NH3、CO2等,请用共价键理论解释H2O分子比NH3分子稳定的原因:_______ 。
(1)按照核外电子的排布,氯吡苯脲中涉及的元素属于元素周期表的s区和
(2)氯吡苯脲的晶体中,氮原子的杂化轨道类型为
(3)氯吡苯脲晶体中,微粒间的作用力类型有
A.离子键 B.极性键 C.非极性键 D.π键 E.氢键
(4)查文献可知,可用2-氯-4-氨基吡啶与异氰酸苯酯反应,生成氯吡苯脲。
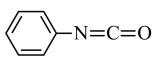 +
+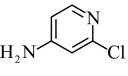 →
→
(5)膨大剂能在动物体内代谢,其产物较为复杂,其中有H2O、NH3、CO2等,请用共价键理论解释H2O分子比NH3分子稳定的原因:
您最近一年使用:0次
名校
3 . 下表列出了某短周期元素M的各级电离能数据(用I1、I2…表示,单位为kJ/mol)。
下列关于元素M的判断中一定正确的是
| I1 | I2 | I3 | I4 | I5 | …… | |
| R | 740 | 1500 | 7700 | 10500 | 13600 | …… |
| A.M的最高正价为+3价 |
| B.M元素的原子最外层共有4个电子 |
| C.M元素位于元素周期表中第VA族 |
| D.M元素基态原子的价电子排布式为3s2 |
您最近一年使用:0次
名校
4 . W、R、X、Y、Z是原子序数依次增大的前四周期元素,其元素性质或原子结构如表:
回答下列问题:
(1)W的基态原子有_______ 种不同运动状态的电子,Z的价电子排布图为_______ 。
(2)W、R、X的简单氢化物中,三元素的原子的轨道杂化方式均为_______ ,键角由大到小的顺序是_______ (用对应的分子式表示),原因是_______ 。
(3)已知:羧酸的酸性可用pKa(pKa= -lg Ka)的大小来衡量,pKa越小,酸性越强。
由表可见,酸性:三氯乙酸_______ 三氟乙酸(填“大于”“小于”或“等于”),从键的极性角度解释原因:_______ 。
(4)联氨(N2H4)也叫肼,常用于火箭推进剂。N2H4_______ (填“难”或“易”)溶于水,原因_______ 。
| 元素 | 元素性质或原子结构 |
| W | 基态原子L能层所有能级上电子数相同 |
| R | 第二周期元素基态原子中未成对电子最多 |
| X | 基态原子核外s能级上电子总数与p能级上电子总数相等,且第一电离能低于同周期相邻元素 |
| Y | 最外层电子数是次外层电子数的一半 |
| Z | 最外层只有1个电子,其他内层各能级所有轨道电子均成对 |
(1)W的基态原子有
(2)W、R、X的简单氢化物中,三元素的原子的轨道杂化方式均为
(3)已知:羧酸的酸性可用pKa(pKa= -lg Ka)的大小来衡量,pKa越小,酸性越强。
| 羧酸 | pKa |
| 三氯乙酸(CCl3COOH) | 0.65 |
| 三氟乙酸(CF3COOH) | 0. 23 |
(4)联氨(N2H4)也叫肼,常用于火箭推进剂。N2H4
您最近一年使用:0次
名校
5 . 在1778年,法国马厚比无意中发现用硫酸钠、木炭和铁(后改用氧化铁)一起灼烧,再用水滗取可得到纯碱。这一发明使他建立起世界上第一座纯碱工厂。
2Fe2O3+3NazSO4+16C Na6Fe4S3+ 14CO↑+2CO2↑
Na6Fe4S3+ 14CO↑+2CO2↑
Na6Fe4S3+O2+2CO2 Na2Fe4S3+2Na2CO3
Na2Fe4S3+2Na2CO3
回答下列问题:
(1)基态铁原子的价层电子排布式为_______ ,其3d能级上有_______ 个运动状态不同的电子。
(2)基态 原子核外有
原子核外有_______ 对自旋方向相反的电子对。基态钠原子核外电子占据能量最高的能级符号是_______ 。
(3)在氧、硫、钠、碳、铁元素中,金属性最强的元素与非金属性最强的元素组成的化合物是_______ (填化学式)。C、O、F三种元素中,电负性由大到小的顺序为_______ 。
(4)某同学书写的基态碳原子轨道表示式为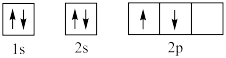 ,他违背了
,他违背了_______ 。
2Fe2O3+3NazSO4+16C
 Na6Fe4S3+ 14CO↑+2CO2↑
Na6Fe4S3+ 14CO↑+2CO2↑Na6Fe4S3+O2+2CO2
 Na2Fe4S3+2Na2CO3
Na2Fe4S3+2Na2CO3回答下列问题:
(1)基态铁原子的价层电子排布式为
(2)基态
 原子核外有
原子核外有(3)在氧、硫、钠、碳、铁元素中,金属性最强的元素与非金属性最强的元素组成的化合物是
(4)某同学书写的基态碳原子轨道表示式为
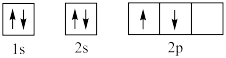 ,他违背了
,他违背了
您最近一年使用:0次
名校
6 . 铜的化合物用途非常广泛。已知下列反应:[Cu(NH3)2]++NH3+CO [Cu(NH3)3CO]+,2CH3COOH+2CH2=CH2+O2
[Cu(NH3)3CO]+,2CH3COOH+2CH2=CH2+O2 2CH3COOCH=CH2+2H2O。
2CH3COOCH=CH2+2H2O。
(1)Cu2+基态核外电子排布式为_______ 。H2O中中心原子上的孤电子对数为_______ 。
(2)NH3分子的空间结构为_______ ,其中心原子的杂化类型是_______ 。
(3)CH3COOCH=CH2分子中碳原子的杂化类型是_______ ,1 mol CH3COOCH=CH2中含σ键的数目为_______ 。
(4)相同条件下,CO2与SO2在水中的溶解度较大的是_______ (填分子式), 中的O-C-O键角
中的O-C-O键角_______ (填“>”“<”或“=”)  中的O-S-O键角。
中的O-S-O键角。
 [Cu(NH3)3CO]+,2CH3COOH+2CH2=CH2+O2
[Cu(NH3)3CO]+,2CH3COOH+2CH2=CH2+O2 2CH3COOCH=CH2+2H2O。
2CH3COOCH=CH2+2H2O。(1)Cu2+基态核外电子排布式为
(2)NH3分子的空间结构为
(3)CH3COOCH=CH2分子中碳原子的杂化类型是
(4)相同条件下,CO2与SO2在水中的溶解度较大的是
 中的O-C-O键角
中的O-C-O键角 中的O-S-O键角。
中的O-S-O键角。
您最近一年使用:0次
名校
7 . 短周期主族元素X、Y、Z、W的原子半径依次增大,且原子最外层电子数之和为15.基态Y原子的最外层电子数是其内层电子数的3倍,Y与Z同主族,Z与W同周期。下列说法正确的是
| A.简单氢化物的沸点:H2Z>H2Y |
| B.电负性由大到小的顺序是Y>Z>X |
| C.化合物WX2中既存在离子键,又存在共价键 |
| D.W元素基态原子核外M层电子的自旋状态相同 |
您最近一年使用:0次
名校
8 . 我国科学家发现了一类由Fe-Se-As-F-O组成的磁性超导材料。下列说法正确的是
A.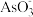 的空间构型为平面三角形 的空间构型为平面三角形 |
| B.Fe变成Fe3+时首先失去3d轨道电子 |
| C.基态F原子的核外电子有7种空间运动状态 |
D.通过化学变化可以实现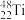 与 与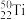 的相互转化 的相互转化 |
您最近一年使用:0次
9 . 下列说法正确的是
| A.各能层含有的能级数为n-1 |
| B.3d3表示3d能级有3个轨道 |
| C.2px、2py、2pz三个轨道相互垂直 |
| D.Mg原子核外电子占据的最高能级的轨道形状为哑铃形 |
您最近一年使用:0次
名校
10 . 下列分子的VSEPR模型与其空间结构不一致的是
| A.CO2 | B.H2S | C.SO3 | D.BCl3 |
您最近一年使用:0次



